Сонографическая картина при заболеваниях почек
Сонографическая картина при заболеваниях почек
Почки и паранефрий в норме
Почки располагаются по обе стороны позвоночного столба. Верхняя их треть прикрывается ребрами, которые проходят над ними кпереди, опускаясь книзу. При рассмотрении сзади и сбоку продольные оси почек образуют с позвоночником острый угол. Поперечные оси почек образуют с сагиттальной плоскостью угол, равный приблизительно 45°. Почки расположены забрюшинно. Правая почка — на уровне Th-12-L-4, левая почка расположена выше — на уровне Th-11-L3 позвонка. Однако определять положение почки относительно позвонков достаточно неудобно, поэтому в эхографической практике в качестве ориентира для определения положения почки используются гипоэхогенная акустическая "тень” от двенадцатого ребра, купол диафрагмы (или диафрагмальный контур печени), ворота селезенки, контрлатеральная почка. В норме акустическая "тень" от двенадцатого ребра пересекает (при продольном сканировании со стороны спины параллельно длинной оси почки) правую почку на уровне границ верхней и средней трети, левую почку — на уровне ворот почки. Обычно почки хорошо видны в положении пациента лежа на боку. Продольное сечение почки видно при размещении датчика на продолжении межреберной линии сбоку. На глубоком вдохе почки смещаются вниз из-под акустической тени ребер и видны в их продольном сечении.
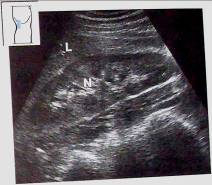
Рис. 1 Визуализация правой почки. Датчик расположен в области задней подмышечной линии справа. N - почка, L - печень.
Верхний полюс правой почки расположен на уровне или несколько ниже верхне-диафрагмального контура правой доли печени. Верхний полюс левой почки расположен на уровне ворот селезенки. Расстояния от верхнего полюса правой почки до контура диафрагмы и от верхнего полюса левой почки до ворот селезенки зависят от степени развития паранефральной клетчатки обследуемого.
Для получения продольной сононграммы правой почки в положении больного на спине пользуются серодикой показанной на рис 2.
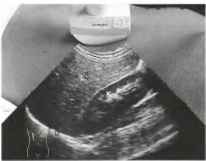
Рис. 2. Для получения изображения в боковой плоскости датчик смещается из парамедиального положения латерально. Данная плоскость используется при оценке плеврального угла, дистальнее диафрагмы (D) и для получения изображения продольного среза почки (К), расположенной кзади от печени (L).
Как и при полном исследовании любых других органов, необходимо обследовать почку во второй проекции чтобы изучить ее поперечное сечение. Датчик может быть установлен непосредственно под реберной дугой или в область последнего межреберья. Следует помнить, что нижние отделы почки располагаются ближе к датчику, верхние отделы удалены от него, т.е. продольная ось идет сверху вниз и от центральной оси тела в латеральном направлении.
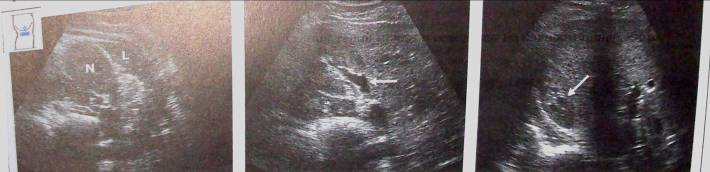
|
а — нижний полюс правой почки (N). L — печень; |
б — срез на уровне ворот почки (<), приведено наибольшее сечение почки; |
в — срез верхнего полюса почки (^). |
Рис. 3.а-в Визуализация правой почки на боковом поперечном сечении
Сонографию правой почки в поперечном сечении можно выполнить в положении больного на спине.
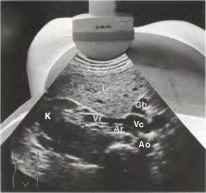
Рис. 4. При оценке продольного среза почки датчик ротируется в поперечное положение в средней части живота и перемещается к средней линии. Почка будет визуализироваться в поперечном срезе, кзади от печени (L). На уровне ворот почки в переднезаднем направлении будет визуализироваться сосудистая ножка почки, включающая почечную вену (Vr) и почечную артерию (Аr), также может определяться мочеточник. У пациентов со слабо выраженной подкожной жировой клетчаткой на одном снимке могут визуализироваться место впадения почечной вены в полую вену (Vc), место отхождения почечной артерии от аорты (Ао) и желчный пузырь (Gb) возле нижнего края печени.
Визуализация тела левой почки осуществляется аналогично визуализации правой почки.
Левая почка расположена также в неком треугольнике, сторонами которого служат позвоночник, мышцы и селезенка. Селезенка прикрывает почти половину почки. Нижняя половина почки сбоку граничит с нисходящей толстой кишкой и левым изгибом ободочной кишки. Ободочная кишка огибает почку спереди. Верхний ее полюс прикрыт спереди желудком. Таким образом, доступ к левой почке оптимален сзади и сбоку через межреберное пространство с использованием селезенки в качестве ультразвукового окна. И тем не менее, качество визуализации левой почки почти всегда гораздо хуже правой, в особенности если сопутствует тому еще и наложение газов кишечника.
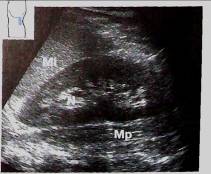
Рис.5 Визуализация левой почки. N — почка, Mi — селезенка, Мр — поясничная мышца.
Нормальные размеры почки:
Длина почки: 10—12 см Ширина почки: 4—6 см Дыхательная подвижность: 3—7 см Толщина паренхимы: 1,3—2,5 см
Форма среза нормальной почки во всех проекциях бобовидная или овальная. Контур почки обычно ровный, а при наличии сохранившейся фетальной дольчатости почки — волнистый (это вариант нормального строения почки). Эхографические характеристики почечной капсулы и паренхимы нормальной почки являются общепринятыми. По периферии ультразвукового среза почки определяется фиброзная капсула в виде гиперэхогенной ровной, непрерывной структуры толщиной 2-3 мм.далее определяется слой паренхимы.
Нормальная паренхима почки имеет немного сниженную или одинаковую эхогенность по сравнению с паренхимой селезенки или печени. Толщина паренхимы должна быть не менее 1.3 см. Отношение толщины паренхимы к ширине почечного синуса (= ПС индекс) уменьшается с возрастом:
ПС индекс (зависит от возраста):
< 30 лет: 1,6 : 1
< 60 лет: 1,2-1,6 : 1
> 60 лет: 1,1 : 1
Ворота почки определяются эхографически в виде 'разрыва» медиального контура паренхимы почки, при этом при сканировании со стороны передней брюшной стенки вверху развертки визуализируется расположенная кпереди анэхогенная трубчатая структура — почечная вена, ниже — расположенная кзади гипоэхогенная почечная артерия. Ворота почки вместе с почечной веной обычно хорошо видны на поперечном сечении. Из-за небольшого размера мочеточник и почечная артерия часто идентифицируются с большим трудом.
Паренхима неоднородна и состоит из двух слоев: коркового вещества и медуллярного вещества (или вещества пирамидок почки). Морфологическим субстратом коркового вещества почки (коры почки) является преимущественно клубочковый аппарат, извитые канальцы, интерстициальная ткань, содержащая кровеносные, лимфатические сосуды, нервы. Корковое вещество почки расположено по периферии ультразвукового среза почки толщиной 5-7 мм, а также образует инвагинации в виде колонок (columnae Bertini) между пирамидками. Эхогенность коркового вещества почки обычно чуть ниже либо сопоставима с эхогенностью паренхимы нормальной печени.
Медуллярное вещество содержит петли Генле, собирательные трубочки, протоки Беллини, интерстициальную ткань. На стандартном продольном сечении гипоэхогенные медуллярные пирамиды выглядят подобно нитям жемчуга между корой паренхимы и центрально расположенной эхогенной собирательной системой. Их не следует ошибочно принимать за опухоли или кисты. Нередко эта разница в эхогенности является причиной ложноположительной диагностики гидрокаликозов, когда очень темные, низкой эхогенности пирамидки принимаются начинающими врачами ультразвуковой диагностики за дипатированные чашечки. Современные гистоморфологические исследования паренхимы почки и сопоставление их с эхографической картиной позволяют предположить, что выраженная эхографическая кортикомедуллярная дифференциация обусловлена значительной разницей в количестве жировых вакуолей в эпителии тубулярных структур коры и пирамидок. Однако объяснить различную эхогенность коры и пирамидок только различным содержанием жировых вакуолей в эпителии канальцевых структур нельзя, т.к. известно, что эхогенность пирамидок почки при высоком уровне диуреза значительно ниже, чем эхогенность пирамидок той же почки в обычных условиях, количество же жировых вакуолей в зависимости от уровня диуреза не меняется. Также нельзя объяснить низкую эхогенность пирамидок наличием жидкости в канальцевых структурах, т.к. разрешающая способность ультразвукового аппарата при любых условиях не позволяет дифференцировать просвет канальца и жидкость в нем. Можно предположить, что низкая эхогенность медуллярного вещества связана с: 1) большим содержанием гликозаминогликанов в интерстициальной ткани, где происходит большинство функциональных процессов, обеспечивающих ионообмен, реабсорбцию воды и электролитов, транспорт мочи; гликозаминогликаны способны 'связывать’ жидкость, по словам авторов гипотезы, "очень быстро набухая и от бухая; 2) наличием гладкомышечных волокон в интерстициальной ткани, окружающей выводные протоки почечного сосочка.
|
Рис. 6. Схематическое изображение паренхимы почек и ее элементов. 1 — корковый слой паренхимы по периферии среза почки и инвагинации коры между пирамидками. 2 — пирамидки. |
|
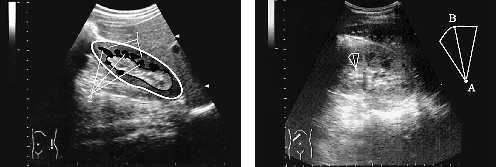
Рис. 7. Эхограмма почки. Толщина пирамидки (АБ) измеряется как высота треугольника с вершиной в проекции сосочка пирамидки. Основанием треугольника является граница между корой и пирамидкой по периферии среза пирамидки. |
Нередко колонка Бертина достаточно далеко выходит за внутренний контур паренхимы в центральную часть почки — в почечный синус, деля почку более или менее полно на две части. Образующаяся своеобразная паренхиматозная 'перемычка', т.н. гипертрофированная колонка Бертина, является нерассосавшийся паренхимой полюса одной из долек почек, которые в процессе онтогенеза сливаются, образуя почку взрослого человека. Пирамидки почки определяются в виде структур треугольной формы со сниженной по сравнению с корой эхогенности. При этом вершина пирамидки (сосочек пирамидки) обращена к почечному синусу — в центральную часть среза почки, а основание пирамидки прилегает к корковому веществу паренхимы, расположенному по периферии среза. Пирамидки почки имеют толщину 8-12 мм (толщина пирамидок определяется как высота треугольной структуры, вершина которой обращена к почечному синусу), хотя нормальные размеры пирамидок в значительной степени зависят от уровня диуреза. В норме выражена эхографическая дифференциация коры и пирамид: эхогенность коркового вещества значительно выше эхогенности пирамидок почки.
Нормальная форма почки может иметь некоторые признаки, отражающие ее эмбриональное развитие. Гиперплазированные колонны Бертини могут выступать из паренхимы в лоханку и не отличаться по эхогенности от остальной паренхимы почки.
Изоэхогенные паренхимальные мостики могут полностью разделять собирательную систему. Частичный или полный разрыв изображения собирательной системы в том же месте указывает на удвоение почки с раздельными мочеточниками и кровоснабжением для каждой половины. Действительно, сложности обычно возникают при диагностике удвоения чашечно-лоханочной системы, являющегося очень частой причиной ложных (ложноположительных и ложноотрицательных) заключений. Порой наличие паренхиматозной "перемычки” — т.н. гипертрофированной колонки Бертина, разделяющей почечный синус, является поводом для постановки эхографического диагноза неполного удвоения чашечно-лоханочной системы. Действительно, случаи с полным разделением почечного синуса паренхиматозной перемычкой более чем в 50% случаев сопровождаются удвоением лоханки и чашечек, однако наиболее часто встречающиеся неполные ("неглубокие") перемычки не являются ультразвуковым признаком удвоения чашечно-лоханочной системы, хотя могут давать выявляемое при экскреторной урографии смещение группы чашечек. Смещение группы чашечек воспринимается врачом рентгенологом как признак объемного процесса в почке. В данном случае ультразвуковое исследование поможет исключить наличие объемного процесса в почечном синусе.
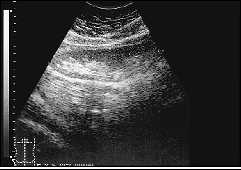
Рис.8. Эхограмма почки с удвоенной чашечно-лоханочной системой. Почка нормально сформирована. Только значительное увеличение длины почки (до 15,6 см) позволило заподозрить наличие удвоения чашечно-лоханочной системы по данным эхографии.
Превертебральная паренхиматозная перемычка подковообразной почки может быть ошибочно принята за пре-аортальную лимфаденопатию или тромбоз аневризмы аорты. Среди аномально сращенных почек наиболее часто встречается подковообразная почка. Чаще всего (примерно в 90% случаев) отмечается сращение нижними полюсами, гораздо реже — средними и верхними сегментами.
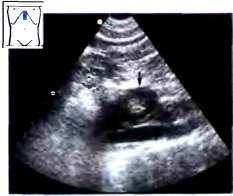
Рис. 9. Подковообразная почка (v). Расположенное перед аортой объемное образование, имеющее па продольном срезе овальную форму.
Дистопия почки — это аномалия развития почки, при которой почка в процессе эмбриогенеза не поднимается до обычного уровня. Различают гомолатеральную дистопию почки, при этом почка находится на "своей' стороне. Среди гомолатеральных дистопий выделяют дистопию поясничную, подвздошную и тазовую. Гетеролатеральная дистопия характеризуется более низким выявлением почки, но не на своей, а на противоположной стороне. При этом возможны варианты гетеролатеральной дистопии со сращением почек и без сращения.
Нефроптоз, или патологическая смещаемость почки, возникает при врожденной или приобретенной слабости связочно-поддерживающего аппарата почки, при этом основная роль в нормальной фиксации почки в почечном ложе отводится паранефральной клетчатке.
При эхографическом выявлении аномально расположенной почки обычно возникают трудности дифференциальной диагностики нефроптоза и дистопии. При этом необходимо помнить, что почка при нефроптозе имеет нормальной длины мочеточник и сосудистую ножку, расположенную на обычном уровне (уровень L1-L2 поясничных позвонков). Дистопированная почка имеет короткий мочеточник и сосуды, отходящие от крупных стволов на уровне почки.
Дольчатый контур почки может быть виден у детей и людей молодого возраста как проявление фетальной дольчатости, характеризующейся ровной поверхностью почки с наличием выемок между отдельными медуллярными пирамидами. Эти изменения следует отличать от почечных инфарктов, которые могут быть обнаружены у пожилых пациентов с атеросклеротическим стенозом почечной артерии.
Ограниченное утолщение паренхимы вдоль латерального края левой почки (либо в области края почечного синуса), обычно непосредственно под нижним полюсом селезенки, обнаруживается почти у 10% пациентов. Этот анатомический вариант, часто называемый «верблюжий горб» "горбатая” почка, иногда бывает очень трудно отличить от истинной опухоли почки. Эти состояния описываются как псевдоопухоли и также являются вариантами нормального строения почки. Одним из отличительных признаков псевдо-опухолевых 'выбухании’ паренхимы при сохранившейся фетальной дольчатости почки, в отличие от опухоли, является сохранение параллельности наружного и внутреннего контура паренхимы, сохранение нормальной эхоструктуры паренхимы.
Атрофические и воспалительные изменения в почках
Почки реагируют на различные воспалительные процессы разнородными сонографическими изменениями. При острых пиелонефрите или гломерулонефрите на ранних стадиях может быть нормальная картина.
Позднее отмечается увеличение почки, с преимущественным увеличением передне -заднего размера почки, в результате чего эхографический срез почки становится округлым, а не овальным, либо бобовидным, как в норме. Отмечается утолщение паренхимы и диффузное снижение эхогенности паренхимы. Отек вызывает увеличение, размеров, а интерстициальная инфильтрация вызывает повышение эхогенности паренхимы с усилением четкости ее границ относительно гипоэхогенных пирамид. Такая картина называется «выбитые медуллярные пирамиды». В сравнении с соседней паренхимой печени или селезенки, паренхима почки в таких ситуациях выглядит более эхогенной, чем паренхима нормальной почки.
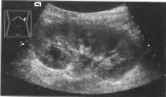
Рис.10. Острый пиелонефрит: увеличенная гипоэхогенная почка с облитерированным синусом и уровнем жидкости в почечной лоханке.
Этот тип эхографических изменений, как правило, сопровождается острой почечной недостаточностью. При этом в основе появления синдрома 'выделяющихся пирамидок лежит ишемия коркового вещества почки с шунтированием крови по венулам мозгового слоя. Ишемия коры почки развивается в результате межуточного отека, клеточной инфильтрации интерстиция и периферической вазоконстрикции. Уменьшается также эхогенность и площадь сечения почечного синуса в результате резорбции клетчатки почечного синуса, сдавливания почечного синуса утолщенной паренхимой.
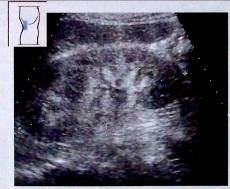
Рис.11. Увеличение почки при остром гломерулонефрите.
Интерстициальный нефрит может быть вызван хроническим гломерулонефритом, диабетической или уратной нефропатией (гиперурикемия как проявление подагры или повышенного обмена нуклеиновых кислот), амилоидозом или аутоиммунными заболеваниями, но установить истинную причину по повышению эхогенности паренхимы невозможно. Другой признак воспаления — нечеткая граница между паренхимой и собирательной системой.
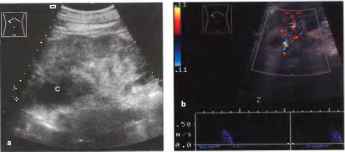
Рис. 12. а, b Тромбоз почечной вены, а Острый тромбоз почечной вены при септическом пиелонефрите: увеличенная почка (К, курсоры) с нечеткой гипоэхогенной структурой и пятнисто-полосатой гипоэхогенной трансформацией центрального эхо- комплекса. С - атипичная киста, b Спектральный анализ показывает крайне высокий ИР, составляющий 0,96.
Пара- и перинефрит чаще визуализируется в виде зон с нечеткими, неровными контурами сниженной эхогенности. При абсцедировании, при гнойном расплавлении паранефрия вокруг почки визуализируются анэхогенные полости, в которых может определяться взвесь. Определяется резкое снижение дыхательной подвижности почки. При наличии вязкого гнойного содержимого в случае "старого”, хронического паранефрита вокруг почки могут визуализироваться опухолевидные массы смешанной эхогенности. При этом границы почек будут нечеткими, однако сами гнойно-некротические массы крайне плохо дифференцируются в забрюшинном пространстве от жировой клетчатки. На рисунке представлена эхографическая картина гнойного апостематозного пиелонефрита. Видна увеличенная, деформированная почка, с резко утолщенной, неоднородной паренхимой, с отчетливыми очагами деструкции. Гнойный процесс распространился на паранефрий с развитием гнойного паранефрита (гипоэхогенная зона вокруг почки отмечена стрелкой).
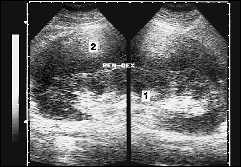
Рис. 13. Эхограмма почки (1) с острым гнойным паранефритом, который развился на фоне апостематозного пиелонефрита. Паранефрит (2) определяется в виде зоны сниженной эхогенности серповидной формы вокруг почки.
Стеноз почечной артерии является причиной периферических инфарктов, а также может приводить к общему уменьшению размеров почки, которое, однако, может быть проявлением возвратного или хронического воспаления.
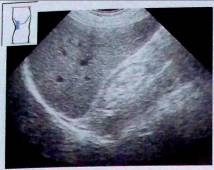
Рис. 14. Сморщенная почка. Значительное уменьшение почки. Нечеткая граница между корковым и мозговым слоями.
Выраженное истончение паренхимы, обнаруживаемое в терминальной стадии хронического нефрита, приводит к атрофии почки, которое часто сочетается с дегенеративной кальцификацией или конкрементами с соответствующей акустической тенью.
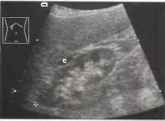
Рис.15. Уменьшение размеров почек при пиелонефрите (83,9 мм, курсоры): очаги истончения паренхимы вследствие ее рубцевания, приводящие к появлению волнистого контура поверхности. С - плоская киста. Тонкоигольная аспирация предполагаемого абсцесса ![]() эпителий надпочечника.
эпителий надпочечника.
Атрофированная почка может быть столь мала, что ее невозможно выявить сонографически. Связанное с этим снижение экскреторной функции может вызвать компенсаторную гипертрофию противоположной почки. При односторонней маленькой почке следует определить ее ПС-индекс. Если ПС-индекс имеет нормальное значение, можно говорить о врожденной гипоплазии почки.
Хотя сонография не позволяет проводить дифференциальный диагноз воспалительных заболеваний почек, ценность ее велика при наблюдении любого почечного воспаления во время лечения, для исключения осложнений (например, острой обструкции) и проведения чрескожной биопсии.
Кисты почек
Кисты почки являются анэхогенными образованиями и, дают дистальное усиление. Дополнительные критерии диагностики кист почки такие же, как и для кист печени. Кисты подразделяются на периферические кисты вдоль поверхности почки,
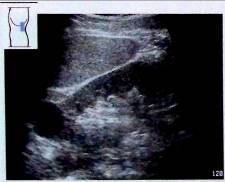
Рис. 16. Периферическая киста верхнего полюса почки.
Кисты паренхимы и кисты почечного синуса, который в дальнейшем необходимо дифференцировать с расширенной вследствие обструкции почечной лоханкой.
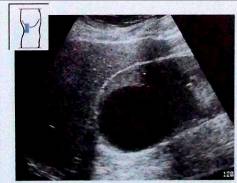
Рис.17. Крупная киста паренхимы.
Описание кисты должно включать ее размер, а также приблизительную локализацию (верхняя, средняя или нижней трети почки). Обнаружение нескольких кист почки не имеет существенного клинического значения, хотя рекомендуется проводить регулярные повторные исследования.
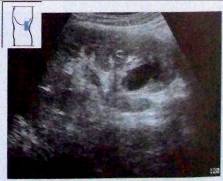
Рис.18. Киста почечного синуса.
В отличие от этого, при поликистозе почек у взрослых имеется не поддающееся подсчету количество кист, которые постоянно увеличиваются в размерах. Когда кисты достигают значительных размеров, больной может предъявлять жалобы на боли и чувство тяжести в верхней части живота.
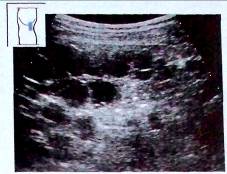
Рис.19. Поликистоз почек.
В дальнейшем поликистоз вызывает атрофию почки из-за смещения и истончения паренхимы органа, что приводит к развитию почечной недостаточности молодом возрасте и требует диализа или пересадки почки.
Признаки обструкци и мочевыводящих путей. Дифференциальная диагностика нарушений уродинамики
При обструкции мочевых путей нарушается нормальный пассаж мочи по мочевыводящим путям, жидкость более или менее полно выполняет полости чашечно-лоханочной системы почек, в результате чего становится возможной визуализация чашечно-лоханочной системы.
Собирательная система почек выглядит как центральный комплекс высокой эхогенности, который пересекается только маленькими тонкими сосудистыми структурами. При повышении диуреза после приема жидкости почечная лоханка может растягиваться и принимать вид анэхогенной структуры. Похожие проявления могут давать различные варианты развития внепочечной лоханки. В обоих случаях дилатация не затрагивает большие и малые чашечки. Существует целый ряд патологических состояний, при которых также визуализируется чашечно-лоханочная система, однако причиной этого не является обструкция. Это — острая и хроническая почечная недостаточность в стадии полиурии, хронический пиелонефрит, сопровождающийся склерозом и деформацией чашечковых и лоханочных структур, туберкулез почек с деформацией, ампутацией, склерозом чашечек, образованием каверн, диабетическая нефропатия с вторичным пиелонефритическим процессом и полиурией, папиллярный некроз, с последующим вовлечением чашечек в склеротический процесс. Пузырно-лоханочный рефлюкс является причиной визуализации чашечно-лоханочной системы при наполнении мочевого пузыря (пассивный рефлюкс), при активном сокращении детрузора (активный рефлюкс) с возможной последующей гидронефротической трансформацией почки. Если перед врачом ультразвуковой диагностики ставится задача выявления рефлюкса, желательно исследовать пациента в условиях обычной водной нагрузки, т.к. наличие жидкости в лоханке при увеличенном диурезе может привести к ложноположительной диагностике рефлюкса. Сложна ультразвуковая диагностика пассивного рефлюкса, так как дилатация лоханки имеет место практически у всех здоровых людей при перерастяжении мочевого пузыря. Можно поставить предположительный диагноз пассивного рефлюкса, если после мочеиспускания у пациента в течение получаса и более сохраняется дилатация полостей ЧЛС (при условии обычной гидратации пациента). Традиционно ультразвуковой диагноз рефлюкса подтверждается уретероцистографией.
Не всегда расширение чашечно-лоханочной системы свидетельствует об обструктивной уропатии. Варианты развития внепочечной лоханки уже упоминались на предыдущей странице. Кроме того, в воротах почки могут быть видны выделяющиеся сосуды, направляющиеся к гипоэхогенным медуллярным пирамидам. Они могут быть ошибочно приняты за элементы собирательной системы, но эти сосуды имеют более нежный вид и не столь растянуты, как это бывает при обструкции и расширении собирательной системы. Пиелоэктазия - ампулярное расширение почечной лоханки при усилении экскреции мочи. Для неё характерны следующие сонографические признаки:
· Треугольное или конусовидное гипоэхогенное образование в области почечной лоханки
· Отсутствие расширения чашечек.
· Отсутствие расширения мочеточника.
· ЦДИ: отсутствие сосудов.
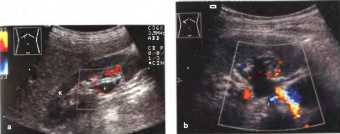
Рис. 20. Пиелоэктазия (Р), ЦДИ. Крупная почечная вена может быть исключена из списка заболеваний, с которыми следует дифференцировать это состояние.
Цветное доплеровское исследование позволит легко определить, являются ли эти структуры кровеносными сосудами с быстрым кровотоком или собирательной системой, заполненной неподвижной мочой. Кровеносные сосуды выглядят как цветокодированные структуры, цвет которых зависит от направления и скорости потока крови, тогда как медленно движущаяся моча в собирательной системе остается черной. Подобный принцип дифференциации по скорости потока может быть использован для отличия кист почечного синуса, не требующих какого-либо лечения, от обструктивного расширения почечной лоханки, которое следует наблюдать или лечить. Разумеется, эти два состояния могут существовать одновременно.
В литературе обсуждаются вазоренальные и вазоуретральные конфликты, обуславливающие наличие синдрома Frayly проявляющегося компрессией чашечек сосудами, аномалии сосудисто-мочеточниковых взаимоотношений (лоханочно-мочеточникового сегмента, ретрокавальное или ретроиликальное расположение мочеточника и пр.) с развитием гидрокаликозов, пиелокаликоэктазий, уретерокаликопиелоэктазий.
Отличить эти проявления от первой (легкой) степени обструкционной дилатации может оказаться очень трудным.
Различают обструкцию "изнутри” чашечно-лоханочной системы полостей почки. Наиболее часто наблюдается обструкция конкрементом, реже — солевым или воспалительным эмболом, опухолью. Встречается обструкция при различных аномалиях мочевыводящей системы — стриктурах мочеточника, стенозах лоханочно-мочеточникового сегмента, высоком отхождении мочеточника, уретероцеле и т.д. Ниже места обструкции мочевыводящие пути не визуализируются на фоне паранефральной клетчатки. Обструкция мочевыводящей системы «снаружи» наиболее часто обусловлена патологией забрюшинного пространства. Это — опухолевые поражения забрюшинных лимфоузлов, первичные и метастатические опухоли забрюшинного пространства, ретроперитонеальный фиброз, опухоли рядом расположенных органов.
При первой (легкой) степени обструкционной дилатации происходит расширение почечной лоханки, но без растяжения чашечек и видимого истончения паренхимы.
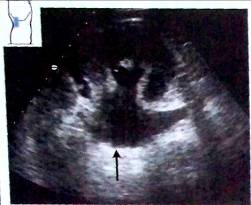
Рис. 21. Нарушение оттока мочи, первая стадия: а — лоханка заполнена жидкостью (^), шейки чашечек пока не растянуты;
Вторая (умеренная) степень обструкционной дилатации вызывает увеличение заполнения чашечек, а также уменьшение толщины паренхимы. Яркий центральный эхокомплекс становится разреженным и в итоге исчезает.
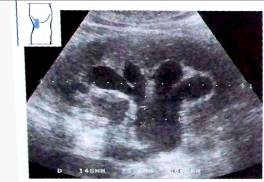
Рис. 22. Нарушение оттока мочи, вторая стадия. Расширение шеек чашечек.
Третья (выраженная) степень обструкционной дилатации характеризуется выраженной атрофией паренхимы вследствие сдавления и наличием кистозно-расширенной лоханки.
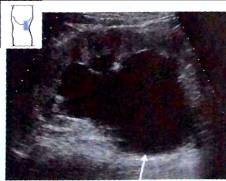
Рис. 23. Нарушение оттока мочи, третья стадия. Кистозно-расширенная лоханка (^), растянутые чашечки, значительное истончение паренхимы.
На четвертой (терминальной) стадии обструкционной дилатации паренхима практически не визуализируется.
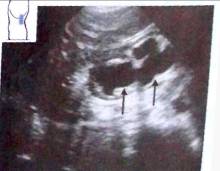
Рис. 24. Нарушение оттока мочи, терминальная стадия. Паренхима почти полностью отсутствует (^).
Сонография не в состоянии выявить все причины структивной уропатии. Поскольку в большинстве случаев средняя часть мочеточника закрыта находящимся над ни газом, камень мочеточника, если не застрял в лоханочном, мочеточниковом или околопузырном отделе (в верхней или нижней трети мочеточника), обычно не визуализируется. Менее частыми причинами обструкции мочеточника являются опухоль мочевого пузыря или матки, увеличении лимфатические узлы, а также ретроперитонеальный фиброз после облучения или идиопатический, как проявлена болезни Ормонда. Латентная обструкция может обнаружиться во время беременности, вследствие атонии мочеточников или при инфекции мочевых путей. Кроме того, причиной обструкции мочеточника может быть перерастяжение мочевого пузыря в результате нейрогенных нарушений и гипертрофии предстательной железы. В этих случаях ультразвуковое исследование должно включать осмотр мочевого пузыря и поиск увеличенной предстательной железы у муж чин.
Инфаркт почки
Эмболия или стеноз почечной артерии может вызвать очаговые инфаркты почки. Клинические проявления: боль в боку, гематурия и протеинурия; лихорадка, лейкоцитоз; тошнота, рвота Может развиваться почечная недостаточность с олигурией. Через несколько дней появляется артериальная гипертензия.
При инфаркте почки его форма, соответствует расположению сосудов в паренхиме селезёнки и характеризуется широким основанием у поверхности почки и сужением к воротам.
Ультразвуковые данные:
· Сегментарная окклюзия почечной артерии в течение 48 часов проявляется появлением зоны резко сниженной эхогенности, соответствующей зоне инфаркта. В острой стадии эмболии почечной артерии почка может иметь нормальную эхо-структуру, может определяться клиновидная гипоэхогенная область, вершина которой направлена к почечной лоханке.
· С 7 по 21 день после инфаркта наблюдается уменьшение зоны инфаркта, границы зоны инфаркта становятся более четкими. Образуется эхогенный треугольный рубец, вследствие которого на поверхности почки образуется углубление, а слой паренхимы уменьшается.
· При геморрагическом инфаркте в результате тромбоза почечной артерии кровоизлияние в паренхиму приводит к появлению неоднородного эхогенного образования неправильной формы.
· ЦДЭ показывает отсутствие кровотока в почечной артерии и иногда клиновидный дефект перфузии паренхимы.
· На поздних этапах при сканировании отмечается уменьшение размеров почки. К 35 дню после инфаркта определяемая зона резко уменьшается, эхогенность ее повышается. Остающиеся рубцы по эхогенноси сходны с камнями почек. Различить их можно по форме локализации.
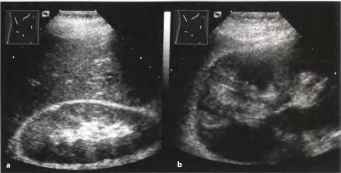
Рис. 25 а, b Инфаркт почки, а Клиновидная, четко отграниченная гипоэхогенная область.b Увеличение: присутствие треугольной бессосудистой зоны подтверждает диагноз инфаркта. Пациент поступил с жалобами на боль в боку.
Точность ультразвуковой диагностики: достоверный диагноз свежего инфаркта почки невозможен без использования ЦДЭ, точность которой достигает 85%. Диагноз может быть подтвержден при помощи ультразвукового исследования с использованием эхоконтрастных препаратов либо при помощи КТ-ангиографии.
Мочекаменная болезнь
В настоящее время эхография является наиболее точным методом неинвазивной диагностики нефролитиаза. Важным преимуществом эхографии является возможность визуализации конкрементов любого химического состава, в том числе — рентгенонегативных конкрементов мочевой кислоты. В то же время обнаружить камни в почках (нефролитиаз) гораздо труднее, чем желчном пузыре, поскольку эхогенные камни почек часто располагаются внутри равной по эхогенности собирательной системы и не дают каких-либо эхосигналов, позволяющих отличить их от окружающих структур. Сложности ультразвуковой диагностики конкрементов возникают при небольших размерах конкремента (3-4 мм). При отсутствии расширения наиболее важно обнаружить акустическую тень от конкрементов или кальцификатов, как, например, при гиперпаратиреозе.
Конкременты в расширенной собирательной системе являются замечательным исключением, поскольку они хорошо заметны в эхонегативной моче как эхогенные структуры. Камень, являющийся причиной обструкции, прекрасно визуализируется на фоне жидкости в чашечно-лоханочной системе
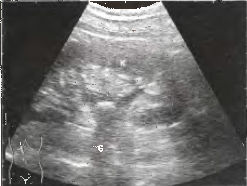
Рис. 26. Камень печеночной лоханки. Печеночная лоханка гипоэхогенна и расширена. В области лоханочно-мочеточникового сочленения обнаруживается камень с высокоамплитудным эхо-сигналом (стрелка) и дорсальной акустической тенью (S). К - почка.
В зависимости от состава, камни почек могут или полностью проводить ультразвук, или настолько его отражать, что видна только ближайшая поверхность в виде эхогенной чашки.
В ультразвуковой практике имеется значительная гипердиагностика конкрементов и песка в почке. Это связано с неправильной интерпретацией изображения почечного синуса при наличии в нем мелких эхопозитивных структур. Дифференциальный диагноз проводится с дугообразными артериями между корковым веществом почки и медуллярными пирамидами (яркое эхо без тени), сосудистыми кальцификатами у больных диабетом и кальцифицированными очагами фиброза после перенесенного туберкулеза почек. Для кальцинатов в сосудистой стенке характерно наличие двух линейных гиперэхогенных структур, расположенных по обе стороны от образования. Наконец, могут наблюдаться папиллярные кальцификаты после длительного приема фенацетина. Для кальцинации сосочка пирамидки характерно расположение в проекции сосочка пирамидки.
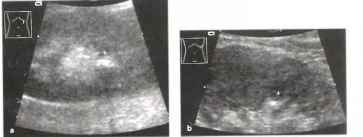
Рис.27. а, b. а Камень почечной лоханки (не вызывающий обструкцию): гиперэхогенный камень с дистальной акустической тенью (S; артефакт «мерцания» помогает подтвердить диагноз камней), b Кальцинация верхушки сосочка при сахарном диабете: яркий эхо-сигнал на верхушке пирамиды мозгового вещества (стрелка) с неполной акустической тенью (S).
Для конкремента характерна округлая форма и достаточно четкая акустическая тень. Однако все эти отличия очень часто не позволяют дифференцировать гиперэхогенные структуры на фоне клетчатки почечного синуса. Для уточнения характера имеющихся гиперэхогенных структур рекомендуется проведение фармакоэхографической пробы с лазиксом. Если данная гиперэхогенная структура является конкрементом, то она будет находиться в пределах дилатированной при полиурии чашечно-лоханочной системы. При этом акустическая "тень" от мелкого камня, окруженного жидкостью, может отсутствовать
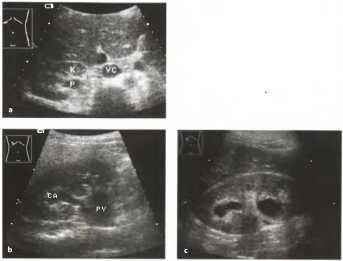
Рис.28. а-с. а Снимок правой почки в высокой поперечной плоскости (К). Кзади от артерии определяется расширенная почечная лоханка (Р) при отсутствии расширения проксимальной части мочеточника. VC - нижняя полая вена. Ь, с Расширение чашечно-лоханочной системы у пациента с болью в боку. Подозрение на желчную колику, b Расширенная чашечка (СА), сообщающаяся с расширенной и закупоренной почечной лоханкой (PY). с Камень проксимального отдела мочеточника, вызывающий обструктивное расширение чашечек. На снимке определяются анэхогенные образования в центральном эхо-комплексе. Верхнее образование представляет собой расширенную шейку чашечки. Расширение шейки чашечки более 5 мм (здесь - 11 мм) указывает на обструкцию. Нижнее образование представляет собой расширенную почечную лоханку.
Большие коралловидные камни трудно диагностировать, если они дают дистальную тень и из-за эхогенности их можно ошибочно принять за центральный эхогенный комплекс.
Если камни почек смещаются и переходят из внутрипочечной части собирательной системы в мочеточник, они могут, в зависимости от размеров, проходить в мочевой пузырь бессимптомно, или с коликой, или застрять и вызвать обструкцию мочеточника. Клинические признаки мочекаменной колики: острые сильные приступы абдоминальной боли, вызванные камнем почки или, в редких случаях, сгустком крови. Выход мочи в околопочечное пространство приводит к образованию уриномы.
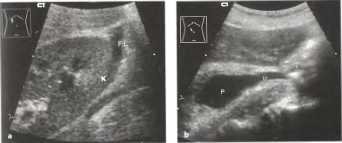
Рис. 29. а, b Почечная колика на фоне камня мочеточниково-лоханочного сочленения. а Гидронефротическая почка (К) с расширенной, заполненной жидкостью почечной лоханкой и транссудатом (уринома, FL). b Камень мочеточниково-лоханочного сочленения (стрелка, U) и расширенная почечная лоханка (Р). Снимок выполнен в верхней косой продольной плоскости брюшной полости по ходу правого мочеточника.
В среде врачей ультразвуковой диагностики широко распространено мнение о невозможности визуализации конкрементов в мочеточнике. Действительно, мочеточник при обычном уровне диуреза практически не дифференцируется от забрюшинной клетчатки. Однако при наличии уростаза, либо при искусственной полиурии визуализация мочеточника возможна. При выраженных дилатациях мочеточника (более 0.7-0.8 см), мочеточник визуализируется на всем протяжении до мочевого пузыря у больного любой комплекции.
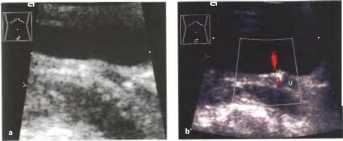
Рис.30. а, b Мочекаменная колика с камнем (стрелка), определяемым в предпузырной части мочеточника (U). а Снимок в В-режиме: высокоамплитудный эхо-сигнал с неполной акустической тенью. Снимок в нижней поперечно-косой плоскости брюшной полости, b ЦДЭ, выполненная 4 днями позднее: камень в устье мочеточника, не вызывающий его обструкции; струя мочи (красный цвет); слабый артефакт «мерцания» в акустической тени камня.
Мочеточник визуализируется лучше при исследовании во фронтальной плоскости в положении пациента на боку. При незначительных дилатациях (при этом мочеточник визуализируется в виде гипоэхогенной тонкой полоски 4-6 мм), как правило, очень трудна визуализация предпузырного отдела, так как после 'перекреста' с подвздошными сосудами мочеточник достаточно резко отклоняется кзади, к задней стенке мочевого пузыря. Поэтому при большом наполнении мочевого пузыря визуализация предпузырного отдела мочеточника резко затруднена, т.к. в таких условиях мочеточник еще больше отклоняется кзади. Можно рекомендовать при исследовании предпузырного отдела мочеточника максимально форсировать диурез (для более тугого заполнения мочеточника жидкостью) и не наполнять сильно мочевой пузырь — максимум до 100-150 мл. Мочевой пузырь при этом наполнен незначительно.
Кроме диагностики обструктной уропатии сонография помогает исключить другие причины абдоминальной боли, такие как панкреатит, колит скопление жидкости
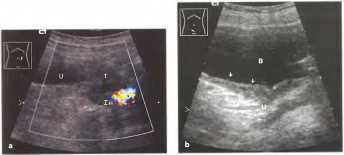
Рис.31 а, b Частые причины хронической обструкции мочевыводящих путей (ОМВП). а Метастазирующая опухоль в малом тазу (яичник, матка; на данном снимке: карцинома прямой кишки), b Карцинома мочевого пузыря (уротелиальная карцинома, стрелки), часто локализуется возле устья мочеточника. Дифференциальный диагноз включает метастазы карциномы простаты. U - мочеточник, IA - подвздошная артерия, В - мочевой пузырь.
Опухоли почек
В отличие от заполненных жидкостью кист, опухоли почек имеют внутренние эхосигналы, и за ними не определяется либо определяется слабое акустическое усиление.
К органоспецифическим доброкачественным опухолям почки относятся аденомы (или онкоцитомы). Ангиомиолипомы, уротелиальные папилломы. Доброкачественные опухоли почек (фибромы, аденомы, гемангиомы) достаточно редки и не имеют универсальной сонографической морфологии.
Только ангиомиолипома, доброкачественная смешанная опухоль, включающая в себя сосуды, мышечную и жировую ткани, имеет на ранней стадии специфические сонографические признаки, позволяющие отличить ее от злокачественного процесса. Мелкие ангиомиолипомы имеют такую же эхогенность, как и центральный эхокомплекс, и четко ограничены. Однако Derchi L. и соавт. (1992 г.) описали случай аденокарциномы почек, дающей практически идентичную ультразвуковую семиотику. С увеличением размера ангиомиолипома становится гетерогенной, что усложняет ее дифференциацию от злокачественных опухолей. Ангиомиолипома имеет медленный (несколько мм в год) не инвазирующий рост. Мелкие ангиомиолипомы паренхимы эхографически схожи с кальцинатами в паренхиме, однако при наличии ангиомиолипомы визуализируется одинаково хорошо и передний, и задний контур образования. При наличии кальцината ультразвуковые сигналы отражаются от передней поверхности образования, далее определяется акустическая тень. Более удаленный от сканирующей поверхности датчика контур образования не визуализируется. Ангиомиолипомы почечного синуса эхографически выявляются только при достаточно больших размерах опухоли, при наличии деформации центрального эхо-комплекса. Ангиомиолипомы могут иметь множественный характер. Наиболее часто множественные ангиомиолипомы в сочетании с множественными кистами определяются при туберозном склерозе — врожденном заболевании, характеризующемся развитием специфических гранулем в головном мозге, с клиникой олигофрении и эпилепсии, а также полиорганным опухолевым процессом.
Маленькая почечно-клеточная опухоль (гипернефрома) часто изоэхогенна по сравнению с остальной паренхимой почки. Только при дальнейшем росте гипернефрома становится гетерогенной и занимает пространство с выбуханием контура почки.
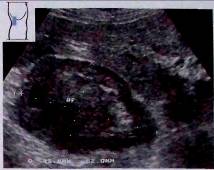
Рис.32. Гипернефрома. Крупная опухоль верхнего полюса почки с гипоэхогенными и ги- перэхогенными включениями.
Если обнаружена гипернефрома, необходимо тщательно обследовать почечные вены, соответствующие места расположения лимфатических узлов, контралатеральную почку для выявления неопластических изменений. Почечно-клеточный рак примерно в 5% случаев имеет билатеральный рост, запущенная опухоль может прорастать в сосуды и распространяться по ходу почечной и нижней полой вен. Если опухоль прорастает капсулу и распространяется на соседнюю поясничную мышцу, почка теряет способность смешаться придыхании.
Лейомиомы почки встречаются достаточно редко. Предполагается, что лейомиомы почки развиваются из мышечных элементов стенки сосудов почечного синуса. Эхографически лейомиомы представлены солидной объемной структурой с четкими ровными контурами более низкой эхогенности, чем паренхима почки.
Лимфомы почек вызывают диффузное увеличение органа с диффузным поражением паренхимы с множественными мелкими гипоэхогенными образованиями с нечетким контуром, либо визуализируются в виде гипо- и либо визуализируются в виде гипо- и анэхогенных крупных очагов округлой формы с тонкой капсулой и четким дистальным псевдоусилением. При этом необходимо проведение дифференциального диагноза с простыми кистами почек. Лимфома почки в большинстве случаев является органным проявлением общего заболевания и появляется обычно на поздних стадиях процесса. Часто в этой стадии заболевания визуализируются пакеты измененных лимфоузлов.
Светлоклеточная аденома эхографически не дифференцируется от рака почки. К сожалению, часто диагноз этой доброкачественной опухоли устанавливается только при аутопсии, после удаления органа. Кистозная форма аденомы при ультразвуковом исследовании имеет форму и структуру пчелиных сот. При этом приходится проводить дифференциальный диагноз с мультилокулярной кистой и кистозной формой гипернефроидного рака.
Левый надпочечник лежит кпереди и кнутри (не сверху) от верхнего полюса почки. Правый надпочечник размешается кзади от полюса, в направлении к нижней полой вене. У взрослых надпочечники не видны или иногда слабо различимы в околопочечной клетчатке. Гормонопродуцирующие опухоли надпочечников, такие как аденома при синдроме Кона или гиперплазия при синдроме Кушинга, обычно слишком малы, чтобы быть обнаруженными при сонографии. Только клинически выраженная феохромоцитома, обычно уже достигшая нескольких сантиметров в диаметре, может быть обнаружена сонографически в 90% случаев. Более существенное значение сонография имеет для выявления метастазов в надпочечники.
Метастазы обычно видны как гипоэхогенные очаги между верхним полюсом почки и селезенкой или нижней поверхностью печени, соответственно, и их следует дифференцировать с атипичными кистами почки. Гематогенное распространение метастазов обусловлено сильной васкуляризацией надпочечников и может происходить при бронхогенном раке, а также при раке молочных желез и почек. Является объемное образование в надпочечнике злокачественным или нет, решить на основании его эхогенности нельзя. Перед проведением тонкоигольной биопсии следует исключить феохромоцитому, чтобы избежать гипертонического криза.
Эхография пациентов перенесших трансплантацию почек
Почечные трансплантаты могут быть в любой из подвздошных ямок и соединены с подвздошными сосудами.
Обычно трансплантат помещается в подвздошную ямку контрлатеральной стороны реципиента. Почка развернута таким образом, что задняя поверхность почки обращена кпереди, передняя поверхность — кзади. Почечная вена анастомозирует с наружной подвздошной артерией, почечная вена — с внутренней подвздошной веной. Ориентация ворот трансплантата противоположна ориентации ворот нормальной почки. Мочеточник трансплантированной почки соединен с мочевым пузырем или, редко, с мочеточником реципиента. Почка располагается в косом направлении, забрюшинно, спереди от m. psoas и подвздошных вен.
Подобно дистопированным почкам, трансплантаты исследуют в двух проекциях но датчик помещают латерально в нижней части живота. Поскольку трансплантированная почка расположена непосредственно за брюшной стенкой, газ кишечника не мешает исследованию.
Крайне важной является ранняя диагностика отторжения трансплантата или других осложнений. Нормой для почечного трансплантата после операции является увеличение в размерах до 20%.
Очень важным показателем для выявления эхографических признаков патологии трансплантата является показатель соотношения передне -заднего размера почки к ее длине. В норме это соотношение составляет 0,3-0,54, при этом значение передне -заднего размера почки не превышает 5.5 см. соответственно поперечный срез трансплантированной почки сохраняет в норме бобовидную или овальную форму. Для точной оценки размеров почечный трансплантат сначала исследуют в продольном сечении и подбирают положение датчика таким образом, чтобы длина органа получилась максимальной. Затем датчик немного поворачивают. Такая двухэтапная методика дает уверенность, что данные измерения длины не занижены, а это может привести к ошибочному заключению об увеличении объема (упрощенная формула: vol = АxВ Сх0.5) при проведении последующих контрольных исследований.
По сравнению с нормальными почками, кора трансплантата выглядит более толстой, а эхогенность паренхимы снижается настолько, что медуллярные пирамиды становятся хорошо видимыми. Прогрессирующая воспалительная инфильтрация должна быть исключена проведением серии контрольных ультразвуковых исследований в течение короткого времени непосредственно в послеоперационном периоде. В дальнейшем в почечном трансплантате следует оценить отчетливость его наружного контура и границы между паренхимой и собирательной системой.
Раскрытая лоханка почки или слегка расширенная собирательная система (первая стадия) может наблюдаться вследствие функциональной недостаточности почечного трансплантата и не требует вмешательства. В норме, в послеоперационном периоде допустима умеренная дилатация ЧЛС трансплантата, по-видимому связанная с отеком уретеронеоцистоанастомоза. Однако эта дилатация не должна достигать значительных размеров. Растяжение мочой должно быть документировано.
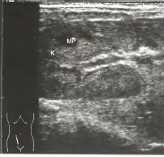
Рис.33 Почечный аллотрансплантат (К) в правой части нижнего этажа брюшной полости. Стрелки: расширенная, заполненная жидкостью чашечно-лоханочная система. С - почечные столбы, МР - гипоэхогенные пирамиды мозгового вещества
К осложнениям трансплантированной почки относятся острый тубулярный некроз, острое отторжение трансплантата, обструктивные процессы, сосудистые осложнения, образование различных затеков, гематом, абсцессов в результате несостоятельности анастомозов и кризов отторжения.
Нечеткая граница между паренхимой и собирательной системой и небольшое увеличение объема могут быть сигналами опасности начинающегося отторжения. Острое отторжение трансплантата развивается в течение нескольких первых недель после трансплантации (однако применение иммуносупрессии может в значительной степени изменить сроки появления острого отторжения). Описаны случаи развития острого отторжения в сроки до 5 лет после трансплантации. Гистологически при остром отторжении выявляется клеточная мононуклеарная инфильтрация и отек почечного интерстиция. Значительно изменяется сосудистое русло: резко утолщается стенка сосудов (артерий и артериоп) с развитием гемморагий. Инфарктов, тромбозов. Эхографически трансплантат увеличивается в размере, в основном за счет передне -заднего размера, при этом в поперечном сканировании форма среза становится округлой. Наблюдается быстрое увеличение объема почечного трансплантата (более чем на 25% за две недели). Соотношение передне -заднего размера к длине почки превышает 0,55. Передне -задний размер почки увеличивается более 5,5 см. Отмечается увеличение площади сечения пирамидок, что соответствует интерстициальному перитубулярному отеку. Эхогенность и площадь сечения центрального эхо-комплекса, соответствующего почечному синусу, уменьшаются за счет уменьшения количества жировых клеток в почечном синусе. В паренхиме появляются гипо- и анэхогенные участки, соответствующие зонам отека, гемморагий, некроза. В целом, кора трансплантата становится более эхогенной за счет клеточной инфильтрации. Чтобы сравнение был достоверным, следует выбирать воспроизводимые продольные и поперечные сечения для измерений и документирования. После трансплантации интенсивность иммуносупрессивной терапии постепенно снижается, промежутки времени между контрольными ультразвуковыми исследованиями можно увеличивать.
Острый тубулярный некроз развивается почти у 50% трансплантируемых почек. Патогенетическими факторами развития острого тубулярного некроза трансплантата являются синдром диссеминированного внутрисосудистого свертывания и гипотензия, имеющие место при хранении трансплантата до операции. Клинически острый тубулярный некроз проявляется появлением симптомов острой почечной недостаточности. Очень редко эхографически при остром тубулярном некрозе отмечается увеличение пирамидок и снижение их эхогенности. Наиболее часто острый тубулярный некроз эхографически не проявляется, однако отсутствие эхографических изменений при развитии острой почечной недостаточности трансплантата не "снимает" диагноза острого тубулярного некроза.
Обструкция мочевых путей является равным по частоте осложнением и, в зависимости от тяжести, может потребовать установки временного дренажа для предотвращения повреждения паренхимы почки. Следует провести измерения лоханки и взаимопоперечных сечениях, чтобы при после дующих исследованиях не пропустить какой-либо динамики, требующей терапевтического вмешательства. Явления дилатаций ЧЛС развиваются в результате обструкции мочеточника "изнутри» сгустком крови, камнем, в результате образования стриктуры, а также сдавливания мочеточника жидкостными затеками, образующимися возле трансплантата при несостоятельности анастомозов. Степени дилатаций ЧЛС, определяемые при УЗИ, в таких случаях весьма значительны
Лимфоцеле может развиваться как осложнение трансплантации почки. Обычно лимфоцеле обнаруживается между нижним полюсом почечного трансплантата и мочевым пузырем. Но может быть в любом месте рядом с трансплантатом. Жидкостные затеки чаще образуются в результате несостоятельности анастомозов, при остром отторжении трансплантата. Выявляют гематомы, лимфоидные затеки, серомы, уриномы. Жидкостные затеки могут нагнаиваться с образованием абсцессов. Чаще эхографическая картина затека не позволяет дифференцировать его состав.
Сосудистые реакции определяются в виде венозного тромбоза, полной или частичной артериальной окклюзии. При остром венозном тромбозе почка быстро и резко увеличивается в размере, кора паренхимы становится более толстой, эхогенность ее резко снижается, исчезает кортикомедуллярная дифференциация. В паренхиме почки появляются множественные гипоэхогенные участки, соответствующие зонам гемморагий. Изменения схожи с изменениями при остром отторжении, поэтому в заключение правильнее выносить два предположительных диагноза. Окклюзия основного ствола почечной артерии, как правило, никаких эхографических изменений не дает. Измерение индекса резистивности (RI) кровоснабжающих сосудов почки при проведении доплеровского ультразвукового исследования дает дополнительную информацию о состоянии почечного трансплантата. В последнее время весьма перспективным считается допплеровское исследование сосудов трансплантата для определения кризов отторжения, определения окклюзии почечных сосудов, а также специфики морфологических изменений, имеющих место при патологии трансплантата. Выраженное повышение резистентности сосудов наблюдается при кризе отторжения почечного трансплантата. При этом отмечается умеренное снижение максимальной систолической скорости кровотока и значительное снижение или исчезновение диастолического потока. Для выраженной реакции отторжения характерно значительное снижение систолического кровотока, практическое отсутствие кровотока в фазе диастолы, увеличение времени ускорения. Для реакции отторжения слабой или средней степени выраженности характерно умеренное снижение систолической скорости кровотока (преимущественно по междольковым артериям), снижение диастолического кровотока с пологим углом склона в период всей диастолы.




