Сонографическая диагностика заболеваний печени
Сонографическая диагностика заболеваний печени.
Эхограмма печени в норме
Подготовка пациента для ультразвукового исследования имеет большое значение, особенно при наличии каких-либо отклонений в строении, расположении, размерах органа или при наличии патологии. Основным фактором является соблюдение правил питания и режима исследования. Для успешного проведения эхографии необходимо соблюдение пациентом следующей диеты: исключение из рациона в течение полутора-двух дней овощей, фруктов, черного хлеба и молочных продуктов, вызывающих нежелательное для исследования вздутие кишечника, ограничение количества растительных соков в день перед исследованием. Само исследование должно проводиться натощак — при воздержании от приема пищи в течение 8- 12часов. В тех случаях, когда исследование проводится не и утренние часы или у больных с инсулинозависимым сахарным диабетом, возможно употребление в пищу несладкого чая и подсушенного белого хлеба. При наличии у пациента нарушения функции или какого-либо заболевания кишечника или органов пищеварительной системы целесообразно проведение медикаментозной коррекции перед исследованием. Независимо от наличия или отсутствия острых и хронических дисфункций или заболеваний всем пациентам показано назначение очистительных клизм в предшествующий исследованию день, если нет противопоказаний по характеру заболевания и состоянию больного.
Оптимизация условий проведения исследования
Попросите пациента поднять правую руку, в результате чего его грудная клетка тоже поднимется вверх. Положите его на спину, попросите глубоко вдохнуть и задержать дыхание. Не забывайте, что при частом использовании этого приема у пациентов, особенно у пожилых мужчин, возникает состояние гипервентиляции.
Современная ультразвуковая диагностическая аппаратура предоставляет широкий выбор разнообразных возможностей для лучшей визуализации органов. Наилучшими для исследования печени являются частоты датчиков 3,5-5 Мгц или мультичастотные и широкополосные датчики, позволяющие получать наиболее качественное изображение в широком спектре частот. Частоты порядка 3,5 МГц позволяют получить наилучшее изображение на большой глубине — от 12-15 до 22-24 см. Частоты порядка 5 МГц обеспечивают хорошее качество изображения на меньшей глубине от 4-5 до 10-12 см. Улучшению качества получаемой информации способствуют также функции, связанные с обработкой сигнала и изображения: изменение динамического диапазона, плотности линий и частоты кадров, фокусирование луча, увеличение в реальном времени и т.п.
Печень является самым большим органом, расположенным в правой верхней половине брюшной полости. В основном она скрыта за реберной дугой. О столь известных анатомических сведениях следует напомнить хотя бы потому, что они имеют огромное значение в выполнении ультразвуковых исследований:
- Размеры печени настолько велики, что ее невозможно обследовать, используя лишь какое-то одно положение датчика. Для полного ее осмотра необходимо использование большого числа положений и углов постановки датчика.
- Ультразвуковой луч для осмотра печени не может быть направлен по кратчайшему пути, его направляют либо между ребрами, либо из положения под реберной дугой. А это значит, что при проведении обследования многие ее области неоднократно попадают в поле зрения и при недостаточном знании анатомии печени осмотр других участков становится проблематичным.
Для получения удовлетворительного изображения печени в большинстве случаев помимо соответствующей подготовки пациента, достаточно проведения сканирования в трех плоскостях со стороны эпигастрия и правого подреберья — косого, продольного и поперечного. При косом сканировании датчик скользит вдоль реберной дуги. При таком расположении и придании датчику различных углов наклона — от 0° до 90° имеется возможность исследования всех отделов печени, за исключением передне-верхней поверхности. При поперечном сканировании датчик располагается под мечевидным отростком грудины. Соблюдение вышеописанной процедуры с дополнительным скольжением датчика в кранио-каудальном направлении позволяет качественно исследовать левую долю печени, включая ее переднюю поверхность. Продольное сканирование является третьим необходимым этапом исследования, который позволяет в поперечном срезе оценить конфигурацию отделов печени, состояние ее трех поверхностей (диафрагмальной, передней и висцеральной) и прочие характеристики. При продольном сканировании датчик скользит вдоль реберной дуги в направлении от левой доли печени к правой и наоборот, располагаясь вдоль длинной оси тела. Помимо указанных методик целесообразно также использовать доступ через межреберья по передней аксиллярной и средне-ключичной линиям. В этих случаях датчик располагается по ходу межреберья и с помощью изменения угла ею наклона имеется возможность хорошего акустического доступа к правой доли печени, воротам, ложу желчного пузыря. Особенно эффективен такой доступ у тучных пациентов и при выраженном метеоризме. Ограничением обычно является наличие у пациента эмфиземы легких. Еще один доступ позволяет провести исследование правой доли печени, у астеничных пациентов со стороны спины, по лопаточной и задней аксиллярной линиям. Однако распространенность этого доступа невелика. Проводить исследование печени целесообразно в большинстве случаев либо в положении пациента лежа на спине, либо на левом боку. Для успешного исследования полезно проводить исследование в различных фазах дыхания — как при максимальном вдохе, так и на выдохе и при нормальном дыхании. Это необходимо для правильной оценки размеров, формы и контуров печени, а также для оценки ее взаимоотношения с окружающими органами, тканями и выявляемыми объектами. Кроме того, необходимо учитывать, что различные режимы дыхания могут по-разному влиять на допплеровские методики исследования кровотока.
При проведении исследования печени целесообразно следовать приведенным ниже рекомендациям последовательного анализа состояния печени для уменьшения возможных диагностических ошибок.
1. Оценка расположения, формы, контуров и анатомического строения печени — сопоставление полученных результатов с имеющимися общими и региональными нормативами с учетом возможных индивидуальных особенностей каждого пациента.
2. Оценка размеров печени в целом и каждой из долей по отдельности — сопоставление полученных результатов с имеющимися общими и региональными нормативами с учетом возможных индивидуальных особенностей каждого пациента.
3. Оценка структуры и эхогенности печени — выявление прямых и косвенных признаков диффузного, очагового или смешанного поражения паренхимы.
4. Оценка сосудистого рисунка печени в целом и конкретных сосудов, протоковой системы в В-режиме — выявление признаков обеднения, обогащения сосудистого рисунка, признаков деформации, ампутации и других нарушений и изменений строения и отображения сосудистой сети, расширения протоковой системы.
5. Оценка влияния окружающих органов и структур на состояние изображения печени — определение возможного искажения эхографической картины печени (артефакты).
6. Проведение дифференциальной диагностики выявленных изменений с учетом данных анамнеза, клинических, лабораторных, инструментальных и других методов исследования.
7. Использование данных современных методик исследования для получения дополнительной диагностической информации. При наличии соответствующего технического оснащения — проведение импульсного допплеровского исследования, цветового допплеровского исследования в различных режимах и т.п.
8. При недостаточной определенности выявленных изменений — проведение динамического наблюдения за пациентом в сроки, адекватные конкретной ситуации, или применение прицельной биопсии для верификации характера поражения.
В подавляющем большинстве случаев при ультразвуковом исследовании печень визуализируется в правом подреберье, за исключением варианта инверсии внутренних органов.
Поперечный срез правой доли печени в положении продольного сканирования чаще напоминает "состарившийся" полумесяц, а форма левой доли при тех же условиях имеет вид Г - образной структуры.
Изображение печени, получаемое при ультразвуковом исследовании, состоит из множества томографических срезов, имеющих небольшую толщину, что не позволяет получить визуальное отображение формы всего органа, а целом. Поэтому исследователю приходится проводить мысленную реконструкцию формы органа. Очевидно, в данном случае специалист основывается на глубоких знаниях о топографии печени.
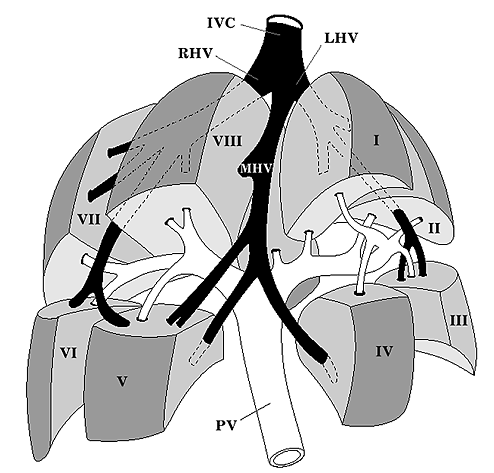
Рис. 1. Сегментарное строение печени с разведением сегментов (схема по С. Couinsud).
В то же время, необходимо отметить, что четко размежевать сегменты печени при ультразвуковом исследовании не удается ввиду отсутствия явных анатомических и эхографических маркеров границ сегментов в пределах долей. Во время исследования возможно лишь выделять центральные зоны ceгментов, ориентируясь на ветви воротной вены.
При ультразвуковом исследовании печени в большинстве, четко различаются все четыре доли (правая, левая, квадратная и хвостатая). Анатомическими ориентирами границ между долями, выявляемыми при эхографии, служат: между правой и квадратной долями ложе желчного пузыря; между квадратной и левой долями — круглая связка и борозда крутой связки; между квадратной и хвостатой долями — ворота печени; выемка венозной Связки в виде гиперэхогенной перегородки (удвоенный листок капсулы и жировая клетчатка) — между левой и хвостатой долями. Хвостатая доля имеет в той или иной степени ярко выраженный хвостатый отросток, располагающийся на эхограммах кзади от ворот печени, кпереди от нижней полой вены и в латеральном направлении от основной массы хвостатой доли.
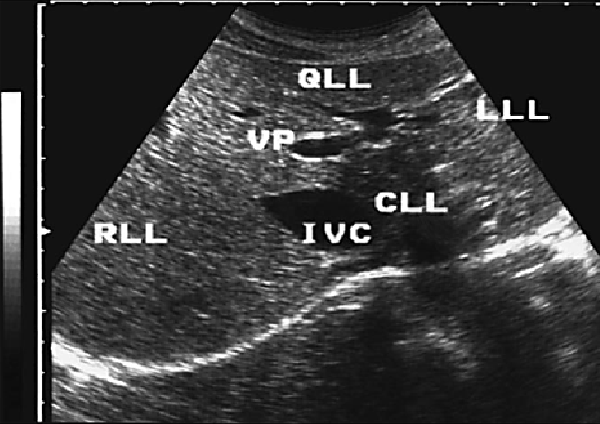
Pис. 2. Эхограмма печени ( датчик расположен параллельно реберной дуге). RLL – правая доля, LLL- левая доля, QLL- квадратная доля, CLL- хвостатая доля, сканирования VP и IVC обозначены левая долевая ветвь, воротной вены и нижняя полая вена соответственно.
При исследовании печени в продольном сечении датчик должен быть расположен перпендикулярно к поверхности тела в эпигастральной области вдоль белой линии живота, и звуковой луч должен веерообразно проходить через верхнюю часть живота (рис. 3.). Время сканирования должно быть достаточным для изучения нормальной анатомии. Схематическое изображение синтопии и скелетотопии органов при продольном сканировании в эпигастрии представлено на рис 4. При наклоне датчика к правой стороне живота пациента паравертебрально слева и кзади от печени (9) обнаруживаются аорта (15). чревный ствол (32) и верхняя брыжеечная артерия (ВБА) (17). В норме все крупные сосуды гипоэхогенные (темные) или анэхогенные (черные).
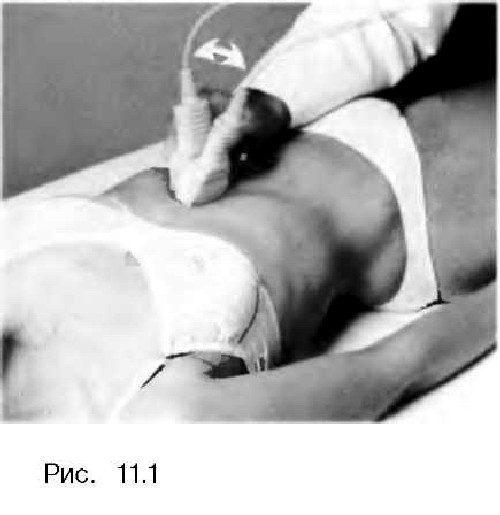
Рис. 3.
Расположенная сверху диафрагма (13) размешается на левой стороне, а расположенные ниже поджелудочная железа (33) и место образования (12) воротной вены (11) — на правой стороне изображения.
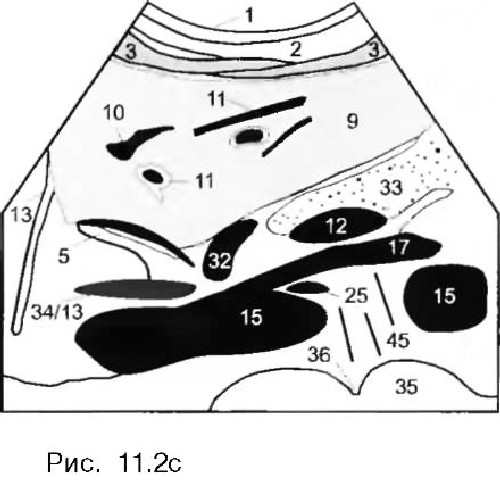
Рис. 4.
Гипоэхогенные тяжи диафрагмы (ножки диафрагмы) (13) и гастроэзофагеальное соединение (34) видны кпереди от аорты и непосредственно ниже диафрагмы. Важно отметить место, где левая почечная вена (25) пересекает аорту, достигая расположенной справа, нижней полой вены. Она идет через узкое пространство между аортой и ВБА, непосредственно кзади от места отхождения ВБА от аорты. Если она видна плохо, неподготовленный исследователь может спутать этот сосуд с гипоэхогенными лимфатическими узлами. Сравнение с поперечным сечением на этом же уровне прояснит в дальнейшем, что изображено на сонограмме.
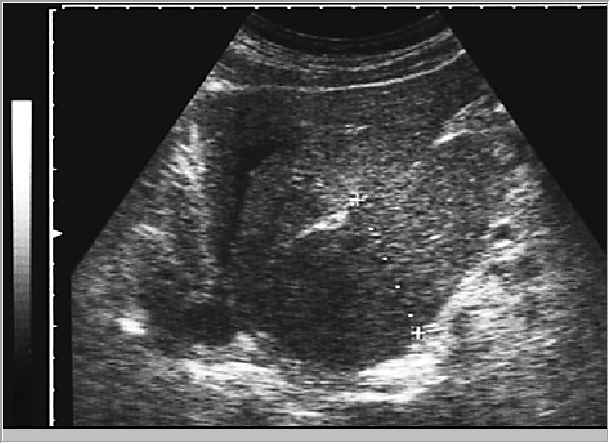
Рис. 5. Сонограмма печени в положении при исследовании в сагиттальной плоскости (отмечена выраженная хвостатая доля, выступающая под висцеральной поверхностью левой доли)
Для получения продольных срезов связки датчик устанавливается почти перпендикулярно правой реберной дуге в направлении от ее средней трети к области пупка с различными углами наклона и ротации. Для получения поперечных срезов связки датчик устанавливается почти параллельно правой реберной дуге на линии от ее средней трети к области пупка с различными углами наклона и ротации и скользит вдоль этой линии. Целесообразно проведение измерения этих трубчатых структур в нескольких местах и нескольких проекциях во избежание ошибок. При наличии формы поперечного среза, отличающегося от округлого, целесообразно получение размера короткой и длинной оси сосуда или протока. Так, воротная вена измеряется в области средней трети ее длинника и непосредственно в воротах печени. Печеночные вены обычно измеряются на удалении не более двух сантиметров от места их впадения в нижнюю полую вену. Нижняя полая вена измеряется в месте ее расположения около хвостатой доли. При достаточно больших размерах хвостатый отросток может значительно выступать со стороны висцеральной поверхности печени (рис. 5).
Как уже было сказано ранее, теоретически в печени при ультразвуковом исследовании можно идентифицировать 8 анатомических сегментов Приводимое ниже описание локализации сегментов относится к изображению, получаемому в положении косого и поперечного сканирования. I сегмент соответствует хвостатой доле. Он имеет четкие, эхографически определяемые границы со II. Ill и IV ceгментами — от II и III сегментов I сегмент отграничивается венозной связкой, a oт IV ceгмента — воротами печени. От VIII сегмента правой доли I сегмент частично отграничивается нижней полой веной и устьем правой печеночной вены. II и III сегменты располагаются в левой доле - II сегмент виден в нижне-каудальной части изображения левой доли с центральным расположением сегментарной ветви левой долевой ветви воротной вены. Ill сегмент занимает верхне-краниальную часть изображения левой доли с аналогичным расположением соответствующей ветви воротной вены. Отграничение этих сегментов от остальных соответствует границам левой доли, определяемым при эхографии. IV сегмент печени соответствует квадратной доле. Его условными границами являются — от III сегмента круглая связка печени и борозда крутой связки, oi I сегмента - ворота печени. Четко видимый ориентир, отграничивающий IV сегмент от сегментов правой доли, отсутствует. Косвенными ориентирами служат: во-первых, ямка желчного пузыря (ложе), видимая при ультразвуковом исследовании как гиперэхогенный тяж различной толщины (в зависимости от выраженности жировой ткани), идущий о косом направлении от ворот печени к нижнему краю правой доли: во-вторых, средняя печеночная вена, проходящая частично позади IV сегмента. Ложе желчного пузыря указывает на приблизительную границу между IV и V сегментами, а средняя печеночная вена — на приблизительную границу между IV и VIII сегментами. V, VI, VII, VIII сегменты относятся к правой доле. Определение их границ в толще правой доли затруднительно в связи с отсутствием четких ориентиров — возможно лишь примерное определение сегмента при учете центрального расположения в нем соответствующей сегментарной ветви воротной вены. V сегмент располагается за областью ложа желчного пузыря и несколько латеральнее. VI сегмент занимает область 1/3 части правой доли латеральнее и ниже V сегмента. Еще ниже располагается VII сегмент, который доходит своей границей до контура диафрагмы. Оставшуюся часть правой доли занимает VIII сегмент, который еще иногда называют “язычковым”. Особенностью VIII сегмента является его переход на диафрагмальную поверхность позади квадратной доли, где он практически неотличим от последней.
Ведя разговор об ультразвуковой анатомии печени, нельзя не отметить возможные анатомические варианты развития, которые в некоторых случаях могут имитировать те или иные патологические состоянии. К таковым анатомическим вариантам развития печени относятся: инверсия печени, ротация печени, вариации контуров и размеров долей, доля Риделя, истончение левой доли, врожденное отсутствие левой доли, локальная гипертрофия долей и сегментов печени, дополнительные борозды, интерпозиция толстого кишечника и т.п. Инверсия печени — расположение органа в ином месте брюшной полости — чаще всего в левом подреберье, сочетающееся с инверсией прочих органов пище верительной системы. Ротация печени — изменение ее расположения вдоль одной из осей — длинной или короткой. Чаще наблюдается вариант ротации по длинной оси, при котором к передней брюшной стенке обращен не нижний край печени, а либо ее висцеральная, либо диафрагмальная поверхности. Вариации контуров и размеров долей являются достаточно частой находкой, однако, дни их идентификации необходимо сопоставление данных, полученных при эхографии, касающихся не только строения органа, но и его частей, с данными анамнеза и клинико-лабораторно-инструментальных исследований. То же самое относится и к остальным вариантам анатомических особенностей печени. Доля Риделя представляет собой врожденную изолированную гипертрофию правой доли печени, при которой может сложиться впечатление о гепатомегалии вследствие патологического процесса, хотя данные эхонографии указывают на нормальный характер строения печеночной паренхимы. Дополнительные борозды на поверхностях печени могут привнести лишние сложности, особенно в тех случаях, когда идет речь о травме органа. В этом случае решающее значение имеет оценка контура, капсулы и субкапсулярной паренхимы печени в области предполагаемых изменений. Интерпозиция толстого кишечника связана с таким вариантом расположения поперечно-ободочной кишки и восходящей ободочной кишки, при котором акустический доступ к печени или ее отделам осложнен настолько, что проведение исследования через традиционные доступы является проблематичным.
Капсула печени отчетливо визуализируется в виде гиперэхогенной структуры, окружающей паренхиму печени, за исключением участков, прилежащих к диафрагме, где капсула не дифференцируется от последней (рис. 6).
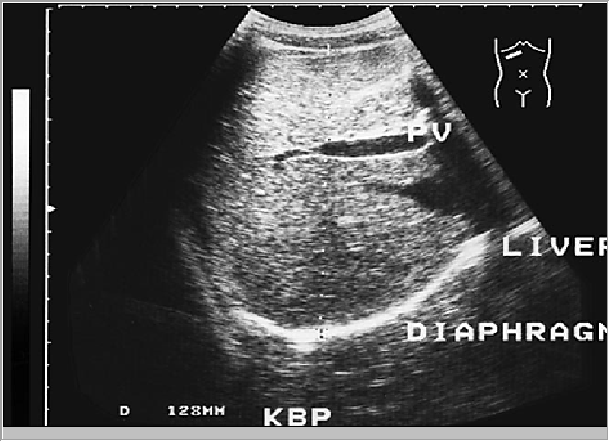
Рис. 6. Косое сканирование в правом подреберье (В области нижнего края правой доли – отчетливо видна капсула печени. Ее самостоятельное изображение в области диафрагмальной поверхностей и отсутствие.)
Контуры печени имеют достаточно ровные и четкие очертания. Поверхности печени имеют различную кривизну на разных участках. На висцеральной поверхности печени, обращенной к брюшной полости, часто имеется несколько вдавлений, образованных тесным прилеганием ряда органов правой почки, печеночного изгиба толстой кишки, двенадцатиперстной кишки, желудка, правого надпочечника. Достаточно часто хорошо визуализируется круглая связка и венечная борозда, изредка — серповидная связка. Круглая связка обычно имеет вид гиперэхогенной округлой (при косом сканировании) структуры, часто дающей акустическую тень или эффект дистального ослабления эхосигнала. При продольном сканировании связки видна в виде гиперэхогенного тяжа, идущего косо в кранио-каудальном направлении снизу вверх. Венечная борозда чаще всего выявляется в виде участка втяжения на передней поверхности печени при косом сканировании. У тучных пациентов в области борозды выявляется утолщенный слой жировой клетчатки, который, находясь в углублении борозды, может симулировать поверхностно расположенное объемное образование смешанной эхогенности и неоднородной структуры. Прочие структуры связочного аппарата печени в обычных условиях не дифференцируются и становятся доступными для идентификации только при наличии асцита или локальных скоплений жидкости. При продольном сканировании четко визуализируется нижний край печени. Угол нижнего края левой доли, не превышает 45 градусов, правой — 75 градусов. Левая оконечность печени также имеет острый угол — до 45 градусов. В норме нижний край печени практически не выступает из-под реберной дуги и при установке датчика перпендикулярно последней акустическая тень от нее падает на нижний край печени.
Исключение составляют случаи, когда имеется опущение печени без увеличения ее размеров и без особенности конституционального строения. Так у гиперстеников нижний край печени чаще выступает на 1-2 см из-под реберной дуги, а у астеников, наоборот, печень скрыта в глубине подреберья. При определении размеров печени можно пользоваться различными методиками. Наиболее информативными и общепринятыми являются косой вертикальный размер правой доли (КВР) — до 150 мм, кранио-каудальный размер левой доли (ККР) до 100 мм, толщина правой доли — до 110-125 мм, толщина левой доли — до 60 мм.
Эхография позволяет дифференцировать разнообразные трубчатые структуры, находящиеся внутри паренхимы печени. К ним в первую очередь относятся печеночные вены и их мелкие ветви, ветви воротной вены, печеночной артерии и желчевыводящие протоки. В паренхиме неизмененной печени четко прослеживаются ветви воротной вены и печеночные вены, причем отчетливая визуализация мелких (до 1 -2 мм в диаметре) ветвей печеночных вен в ряде случаен является важным диагностическим признаком. Воротная вена делится на два крупных ствола в воротах печени — правую и левую долевые ветви, образующие характерный рисунок при косом сканировании (рис. 7).
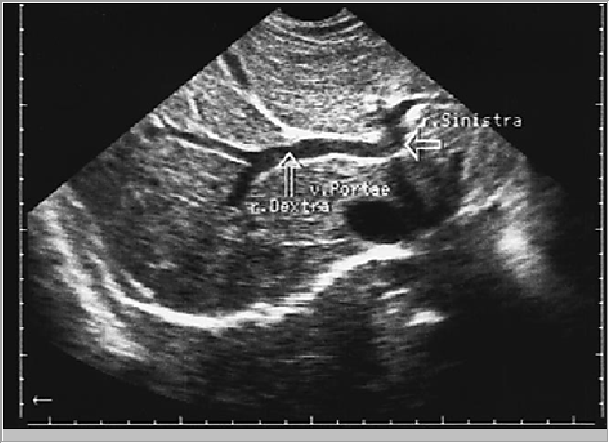
Рис. 7. Сонограмма бифуркации воротной вены на правую левую долевые ветви с фрагментами сегментарных отделов (датчик установлен вдоль правой реберной дуги).
Сегментарные ветви воротной вены располагаются в центральных отделах сегментов печени и далее разделяются на субсегментарные ветви, характерными признаками которых является горизонтальное расположение на томограммах и наличие четко выраженных эхопозитивных стенок. Внутренний диаметр воротной вены уменьшается в направлении более мелких ветвей. Печеночные вены обычно представлены время крупными магистральными стволами — правым, средним и левым, и мелкими ветвями (рис 8).
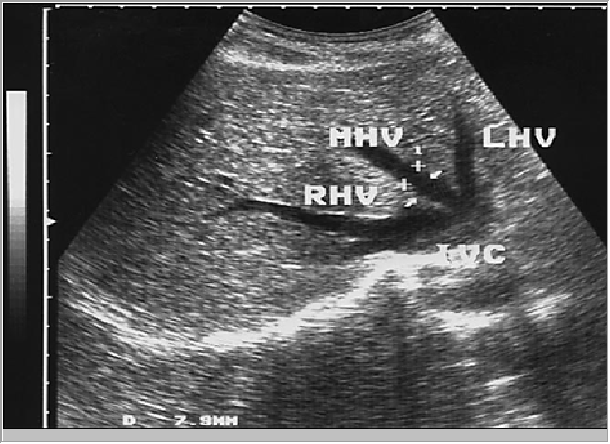
Рис. 8. Сонограмма печеночных вен впадающих в нижнюю полую вену (IVC): RHV – правая. MHV-средняя и LHV-левая почечные вены.
Правая печеночная вена располагается в толще правой доли печени, средняя проходит в главной междолевой борозде, а левая — в толще левой доли печени. В глубине, за хвостатой долей, они впадают в нижнюю полую вену. В некоторых случаях может встретиться иной вариант “рассыпной" тип, когда вместо трех магистральных стволов визуализируются несколько менее крупных вен. Отличительными признаками печеночных вен являются их радиальное расположение — направление от периферии в центр '‘отсутствие" стенок (за исключением случаев, когда сканирующий луч проходит по направлению к стенке под углом, близким к 900), четкая прослеживаемость мелких ветвей (до 1 мм в диаметре) до периферии органа. Нормальный диаметр воротной вены составляет 10·14 мм. печеночных вен — 6-10 мм на расстоянии до 2 см от устьев. Диаметр нерасширенного основного ствола воротной вены в области печеночно-двенадцатиперстной связки, в зависимости от конституции исследуемую, составляет 10-14 мм. В комплекс исследования печени входит также осмотр нижней полой вены на участке ее прилегания к печени. Нижняя полая вена располагается в борозде между правой явной и хвостатой долями. Ее поперечное сечение может иметь диаметр до 20 25 мм. четко видимые стенки и близкую к овальной форму. Печеночная артерия визуализируется в области ворот печени как трубчатая структура небольшого диаметра, обычно до 4-6 мм, с высокоэхогенными стенками. Ветви печеночной артерии могут быть выявлены в В-режиме в области бифуркации и долевых ветвей. Более мелкие градации обычно не дифференцируются. Возможность выявить и идентифицировать мелкие сегментарные и субсегментарные ветви печеночной артерии имеется при использовании диагностических приборов высокого класса, имеющих высокую разрешающую способность и функции цветового и спектрального допплеровского исследования.
В некоторых случаях могут наблюдаться те или иные особенности строения и расположения печеночных сосудов, например, добавочные сосуды — дополнительная ветвь печеночной артерии к квадратной доле, хвостатой доле или V сегменту, своевременное выявление которых может предотвратить некоторые осложнения при проведении операций на печени и желчевыводящей системе. Дифференциация трубчатых структур обычно не представляет существенных сложностей, если учитываются все признаки, включая исследование “на протяжении" — т.е. прослеживание дальнейшего хода трубчатой структуры в обоих направлениях. Современные методики цветового и импульсного допплеровского исследования позволяют в подавляющем числе случаев легко дифференцировать эти структуры по наличию цветового сигнала и разности скоростей и направления кровотока в них.
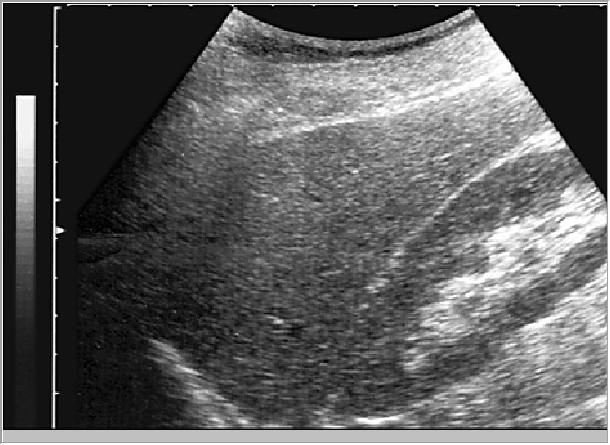
Рис. 9. Вариант нормальной сонографический картины паренхимы печени (продольное сканирование несколько латеральнее серединно-ключичной линии).
По мнению большинства исследователей, структура паренхимы неизмененной печени представлена мелкозернистым изображением, состоящим из множества мелких точечных и линейных структур, равномерно расположенных по всей площади полученного среза Рис. 9. Иногда вариантом неизмененной паренхимы печени может быть более крупнозернистое изображение, при условии сохранения однородности ткани. По эхогенности ткань нормальной печени сопоставима или несколько превышает эхогенность коркового вещества почки (являющегося эталоном при отсутствии патологии этого органа). В ряде случаев в области ворот печени может наблюдаться некоторое повышение эхогенности паренхимы печени. Эхогенность хвостатой доли из-за особенностей ее расположения часто может быть несколько ниже эхогенности левой доли. Причиной, приводящей к некоторому снижению эхогенности хвостатой доли, чаще всего является повышенное поглощение и отражение ультразвука круглой связкой и воротами печени. Еще одним важным признаком считается звукопроводимость органа, которая в норме является хорошей и при исследовании возможна отчетливая визуализация глубоких отделов печени и диафрагмы. Звукопроводимость характеризует отражающую, поглощающую и рассеивающую способности ткани. Чем больше изменений присутствует в ткани (жировых, фиброзных и т.д.), тем хуже ее звукопроводимость и, соответственно, хуже визуализация глубоко расположенных отделов и структур.
Осмотр квадратной доли на поперечном сечении
Подберите такую позицию датчика, чтобы экранное изображение круглой связки находилось в середине паренхимы печени Левее связки, т.е. справа на мониторе, просматривается левая доля печени. Правее связки располагается квадратная доля, которая по анатомическим канонам относится к правой доле, а по функциональному делению — к левой доле печени.
Повторите осмотр круглой связки еще раз и в то же время осматривайте квадратную долю. По ходу связки вверх и вниз внимательно оценивайте увиденную картину. Не пропустите момент появления на экране квадратной доли и желчного пузыря, расположенного у нижнего края печени, т.е. слева на экране. Желчным пузырь является правой границей квадратной доли.
Напрямую с доступами и фазами дыхания связаны и вопросы измерения размеров печени. Косой вертикальный размер правой доли (КВР) отражает величину правой доли печени в направлении от нижнего края до наибольшей выпуклости купола диафрагмы, получаемую при выведении максимальной площади среза изображения правой доли. Соответствующее изображение дня измерения КВР правой доли печени, получается в положении косого сканирования с расположением датчика по среднеключичной линии вдоль реберной дуги с некоторым, часто индивидуально подбираемым, углом наклона — в интервале от 75° до 30°. Измерять этот размер можно практически в любой фазе дыхательного цикла, однако, в фазу максимального задержанного вдоха может быть допущена ошибка измерения, связанная с движением нижнего края печени вниз, что приведет к ложному уменьшению размера. При отсутствии патологии КВР правой доли печени не превышает 150 мм. Кранио-каудальный размер левой доли (ККР) соответствует величине левой доли от ее нижнего края до диафрагмальной поверхности и в клинической практике в какой-то степени соответствует одному из размеров печени по Курлову, определяемому методом перкуссии. Его нормальные показатели не превышают 100 мм.
Толщина левой доли соответствует величине левой доли от ее передней до задней, обращенной к позвоночному столбу, поверхности. ККР и толщина левой доли измеряются в положении продольного сканирования с расположением датчика в сагиттальной плоскости по средней линии тела практически в вертикальном положении. Получаемый при этом поперечный срез левой доли позволяет провести оба измерения одновременно. Толщина левой доли является одним из важнейших параметров, позволяющих своевременно определять увеличение печени. Нормальные значения данного размера не должны превышать 50-60 мм. Толщина правой доли отображает ее величину от передней поверхности, до места перехода диафрагмальной поверхности в висцеральную (Рис. 10.).
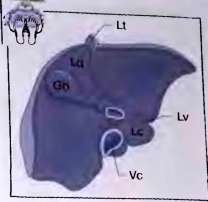
Рис. 10. Печень, вид спереди. Видимая снаружи серповидная связка (Lf) анатомически делит печень на правую и левую доли. Lt — круглая связка, Lc — хвостатая доля, Lq — квадратная доля, IL — левая доля печени, rL — правая доля печени.
Этот размер измеряется также в положении продольного сканирования с расположением датчика в сагиттальной плоскости по средне-ключичной линии или ближе к передне-аксиллярной линии с частичным выведением в срез правой почки по ее длиннику. При отсутствии патологии печени значения толщины правой доли не превышают 120-125 мм . Последние три размера могут быть определены в большинстве случаев без существенных ошибок в любой фазе дыхания. Толщина хвостатой доли, измеряемая как при продольном, так и при косом или поперечном сканировании, позволяет получать дополнительную диагностическую информацию при ряде заболеваний. Ее толщина в норме не превышает 30- 35 мм. Дополнительной возможностью для контроля размеров печени является осуществляемое в режиме нормального дыхания измерение расстояния от нижнего края печени, до нижнего края реберной дуги с ориентацией на акустическую тень от последней. Этот подход особенно целесообразен при значительном увеличении размеров, когда полное изображение максимального среза печени не помещается на экране даже при минимальном увеличении на максимальной глубине сканирования — до 24-30 см. Необходимо учитывать также, что при глубоком вдохе печень, смещаясь каудальнее, ложно сокращает свои вертикальные размеры. Необходимым условием правильного и полноценною исследования печени в В-режиме является измерение диаметров печеночных сосудов и протоков. Обязательному измерению подлежат: магистральный ствол воротной вены, печеночные вены, общий желчный проток, печеночная артерия, нижняя полая вена. Оценка состояния и диаметра воротной вены, общего желчного протока, печеночной артерии производится на протяжении печеночно-двенадцатиперстной связки в положении косого сканирования.
При проведении исследования необходимо учитывать также особенности, возникающие при наложении эхографической картины окружающих органов и структур на изображение печени в томографических срезах, получаемых в процессе сканирования. Наиболее часто такие особенности встречаются в местах тесного контакта висцеральной поверхности печени с правой почкой, печеночным изгибом толстой кишки, двенадцатиперстной кишкой, желудком, правым надпочечником. Некоторые патологические процессы в этих органах, располагающиеся по их внешнему контуру, могут проецироваться на паренхиму печени, создавая трудности с определением их характера и органопринадлежности. Кроме того, помехи от содержимого органов желудочно-кишечного тракта (печеночного изгиба толстой кишки, двенадцатиперстной кишки, желудка, поперечно-ободочной кишки) могут экранировать и маскировать возможные изменения в соответствующих областях паренхимы печени. Таким образом, для проведения успешного ультразвукового исследования печени необходимо применять весь спектр методик и доступов.
Ультразвуковые признаки портальной гипертензия. Роль венозных анастомозов.
Наиболее частая причина повышения давления в воротной вене — это нарушение венозного оттока вследствие цирроза. Непосредственное сдавление воротной вены прилегающей опухолью обнаруживается реже. Опухоль поджелудочной железы прорастает селезеночную или верхнюю брыжеечную вену без поражения воротной. Расширение воротной вены более 13 мм следует считать подозрительным в отношении портальной гипертензии. Внутренний диаметр воротной вены измеряется перпендикулярно продольной оси сосуда, которая обычно направлена косо по отношению к сонографическому изображению. Стенка сосуда не включается в измерение. Следует помнить, что спленомегалия, вызванная другими причинами, может приводить к увеличению внутреннего диаметра селезеночной или воротной вены без портальной гипертензии.
Необходимо отметить, что увеличение диаметра воротной вены не является обязательным признаком, существующим постоянно, т.к. после образования портокавальных анастомозов диаметр воротной вены может уменьшиться до нормальных величин. В ряде случаев встречается реканализация пупочной вены, проходящей в круглой связке печени. При развитии портальной гипертензии могут визуализироваться портокавальные коллатерали — множественные мелкие (до 1-3-5 мм в диаметре) извитые венозные сосуды в области ворот печени и селезенки, под нижним краем левой доли печени. Их может быть сложно, дифференцировать на приборах, не имеющих допплеровского блока, поэтому главным техническим приемом для дифференциации их от мелких образований (лимфатических узлов, метастазов и т.п.) является многоплоскостное сканирование, позволяющее выявить их трубчатый характер. При наличии допплеровского блока в приборе эта задача упрощается, благодаря наличию спектрального или цветового сигнала от коллатералей. Иногда выявление портокавальных коллатералей является одним из решающих признаков, говорящих в пользу цирроза печени при исключении других причин портальной гипертензии. При наличии в клинической картине заболевания желтухи важным дифференциально-диагностическим признаком печеночного генеза гипербилирубинемии является отсутствие расширения внутрипеченочных и внепеченочных желчевыводящих протоков. В качестве дополнительных признаков учитывается наличие асцита и спленомегалии. Однако следует всегда помнить о возможности развития синдрома портальной гипертензии вследствие ряда других заболеваний. В дифференциальной диагностике цирроза печени, так же, как и острого и хронического гепатита, особое внимание уделяется не только выявлению признаков диффузных изменений паренхимы печени и степени их выраженности, но и получению убедительных данных в пользу того, что неоднородность паренхимы не связана с множественным мелкоочаговым солидным поражением печени, а также дифференциации причин гипербилирубинемии и портальной гипертензии. Значимым дифференциально-диагностическим критерием также является сопоставление эхографической картины с клинико-лабораторными показателями.
При портальной гипертензии, независимо от ее генеза, выявляется ряд нижеперечисленных общих эхографических признаков, присутствующих в том или ином виде в зависимости от степени выраженности нарушения гемодинамики.
• Обнаружение портокавальных коллатералей в воротах печени.
• Диметр воротной вены в воротах печени > 15 мм.
• Расширение селезеночной вены >1.2 см.
• Спленомегалия.
• Обнаружение асцита.
• Реканализация пупочной вены (синдром Cruveilhier-Baumgarten).
• Варикозно расширенные вены пищевода (при эндоскопии).
Рассмотрим нарушения портального кровотока. Одним из важных вопросов, связанных с диагностикой патологии печени с помощью ультразвукового метода исследования, является оценка портальной гемодинамики. Портальный кровоток может нарушаться как при диффузных поражениях паренхимы печени, так и при ряде других патологических состояний — тромбозе воротной вены, первичном врожденном портальном фиброзе, кавернозной трансформации воротной вены, увеличении кровотока по воротной вене, синдроме Бадда-Киари, поражении печеночно-двенадцатиперстной связки различными опухолями и сдавлении ее измененными лимфатическими узлами, а также при ряде заболеваний поджелудочной железы. В связи со столь широким спектром факторов, приводящих к портальной гипертензии, возникает необходимость дифференцировать причину нарушения портальной гемодинамики и, соответственно, более корректно устанавливать диагноз.
Правое подреберное косое сечение (рис. 11) наиболее подходит для получения продольного изображения печеночных вен и места их слияния с косо рассеченной нижней полой веной.
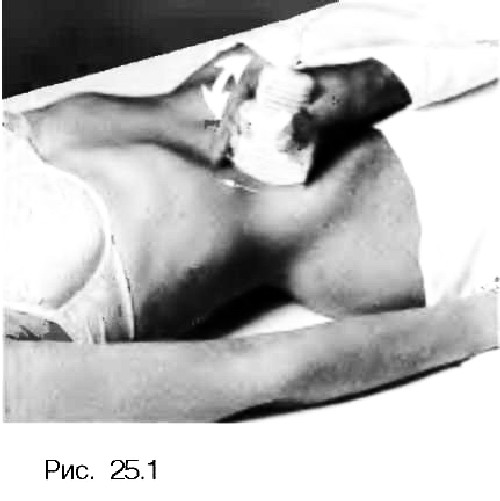
Рис. 11
Если диаметр воротной вены имеет пограничное значение, а проба на спадание вены при форсированном дыхании отрицательная или неубедительная, внутренний диаметр печеночных вен лучше измерять на этом уровне. Максимальный диаметр периферических печеночных вен не должен превышать 6 мм . Нецелесообразно измерение печеночных вен в месте слияния с нижней полой веной из-за широких анатомических вариаций и ложных результатов. Например, печеночные вены пациента без патологии сердца на измеренные непосредственно вблизи полой вены, имеют диаметр 10 мм, в то время как периферические ветви печеночных вен — только 3—5 мм. При правожелудочковой недостаточности печеночные вены расширены, и дыхательные изменения их просвета отсутствуют.
На этом сечении можно также исключить правосторонний плевральный выпот, проявляющийся как эхонегативная жидкость между диафрагмой и акустической тенью от легких. Обеднение сосудистого рисунка по периферии печени может быть признаком далеко зашедшего цирроза печени. Тромбоз печеночных вен (синдром Бадд-Киари) может быть диагностирован на косых межреберных сечениях с использованием цветного доплеровского исследования, определяющего скорость, характер и направление внутрисосудистого кровотока.
Увеличение размера воротной вены обычно более выражено в период до развития портосистемных коллатералей. При появлении последних из-за сброса крови в систему нижней полой вены размер воротной вены может возвращаться к нормальному.
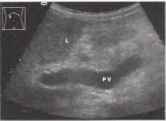
Рис. 12. Ранняя стадия портальной гипертензии. Имеется пограничное расширение воротной вены (PV): 12,9 мм внутри печени, 13,7 мм в печеночно-двенадцатиперстной связке (курсоры). L - печень.
Применение цветового допплеровского исследования позволяет установить направление и характер кровотока в вене и ее ветвях, а импульсное допплеровское исследование дает информацию о скоростях кровотока в этих сосудах. Из большого количества предложенных для оценки состояния портальной гемодинамики показателей наиболее общепризнанным и имеющим практическое значение, подтвержденное многочисленными исследованиями, является показатель линейной скорости кровотока. Его значение у здоровых лиц составляет интервал от 18 до 23 см/с. причем его значение резко возрастает при исследовании после приема пищи (на 100-200%) или при задержке дыхания в фазе глубокого вдоха (на 50-70%). Этот показатель также является весьма чувствительным к точности соблюдения методики исследования и к участку, с которого снимаются показатели. Ряд других показателей, таких, как вычисление объемной скорости кровотока, по мнению ряда специалистов, показали недостаточную точность и клиническую эффективность. Ряд исследователей отмечает более низкие линейные скорости кровотока в воротной вене в норме — до 15 ± 0.2 см/с, и достаточно высокую эффективность определения объемной скорости кровотока (до 845 ± 20 мл/мин в норме).
Замедление скорости кровотока по воротной вене ниже 15-20 см/с. Показатели скоростей кровотока в воротной вене также могут иметь неодинаковое значение в различных участках сосуда. Так, скорости кровотока в магистральном стволе — на участке от места слияния верхней брыжеечной и селезеночной вен до бифуркации в воротах печени — несколько выше, чем в долевых ветвях, а при появлении коллатералей из-за сброса крови в систему нижней полой вены скорость в магистральном стволе может значительно превышать нормальные показатели. Поэтому для корректной оценки гемодинамики необходимо проводить оценку скоростей кровотока не только во внепеченочной части воротной вены, но и в области ворот печени и в долевых ветвях воротной вены.
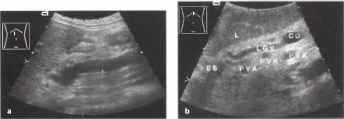
Рис. 13. Портальная гипертензия, портально-системные коллатерали. Верхняя мезентериальная вена расширена до 14 мм (курсоры). Стрелка: расширение левой желудочной вены, которая спускается до воротной вены (PV) по левой стороне, b На снимке, выполненном выше и левее, определяется левая желудочная вена (LGV), идущая от венозного слияния (СО) до пищевода (варикозно - расширенные вены). ES - пищевод, PVA - перигастральные варикозно-расширенные вены.
Таким образом, замедление портального кровотока во внутрипеченочных ветвях будет свидетельствовать и о наличии повышенного сопротивления в связи с поражением паренхимы печени, и о наличии портосистемных анастомозов при ускорении кровотока по магистральному стволу. В. Увеличение диаметра сосудов, образующих воротную вену и их ветвей: селезеночной, верхней и нижней брыжеечных вен. В большинстве случаев селезеночная и верхняя брыжеечная вена легко выявляются при ультразвуковом исследовании. Селезеночная вена легко идентифицируется кзади от тела поджелудочной железы и имеет средний диаметр около 4-6 мм. Верхняя брыжеечная вена на поперечных срезах выявляется несколько кпереди и левее одноименной артерии. Ее диаметр в норме тоже не превышает 4-6 мм. но форма поперечного сечения имеет вид овала с короткой передне-задней осью. Появление портокавальных коллатералей, которые при эхографии имеют вид извитых гипоэхогенных трубчатых структур небольшого диаметра с крайне неотчетливо видимыми стенками, что создает определенные трудности для их выявления и дифференциации. Располагаются эти сосуды в типичных местах локализации портокавальных коллатералей.
Для правильной диагностики портальной гипертензии имеют особое значение несколько групп — с венами пищевода и желудка, спленоренальные, гастроренальные и панкреатодуоденальные. Особенность этих сплетений заключается в наличии удовлетворительного акустического доступа для их исследования через левую долю печени, селезенку и левую почку. Для их дифференциации с успехом используются методики импульсного и цветового допплеровского исследования. В первом случае регистрируется спектр кровотока, получаемый от этих структур, во втором случае четко визуализируется цветовой сигнал. При отсутствии допплеровского блока в приборе коллатерали иногда сложно дифференцировать от мелких забрюшинных лимфатических узлов. Портокавальные анастомозы необходимо дифференцировать от порто-портальных анастомозов при некоторых патологических состояниях. У ряда пациентов происходит реканализация пупочной вены с восстановлением кровотока по ней, что хорошо выявляется при эхографии.
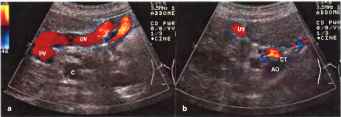
Рис. 14. Реканализованная пупочная вена и околопупочная вена (UV), идущая от пупочной ветви левой воротной вены (VP). ЦДЭ: портально-системные коллатерали с извитыми околопупочными сосудами («голова медузы»), которые обычно впадают в правую или левую подвздошную вены, а Продольный снимок в крайней верхней плоскости брюшной полости, b Снимок в правой косой подреберной плоскости. АО - аорта, СТ - чревный ствол, С - венозное слияние.
Реканализация пупочной вены видна как появление эхонегативного просвета в толще круглой связки печени и, соответственно, возможность получить спектральные и цветовые сигналы при исследовании в допплеровском режиме.
При прогрессировании нарушения портального кровотока регистрируется нарастающее количество свободной жидкости в брюшной полости. При небольших количествах свободной жидкости ее удобнее выявлять в малом тазу, латеральных карманах брюшной полости, слева от печени и под ее висцеральной поверхностью, где визуализируется тонкая анэхогенная полоска, повторяющая контур органа.
Дифференциальный диагноз строится на основании учета состояния паренхимы печени, ворот печени, печеночно-двенадцатиперстной связки, селезенки, иногда поджелудочной железы. Анализ выполняется при исследовании в В-режиме и. по возможности, с использованием допплеровских методик. Тромбоз воротной вены может быть вызван такими различными причинами, как воспалительные заболевания органов брюшной полости, состояния после оперативных вмешательств, опухоли печени, толстого кишечника, поджелудочной железы и др.
Кавернозная трансформация воротной вены может иметь разную степень выраженности морфологических изменений наподобие кавернозной ангиомы с вариабельной локализацией — начиная с отдельных фрагментов воротной вены, или селезеночной, или брыжеечных вен, и заканчивая вовлечением в единый процесс всех этих сосудов. Эхографически может быть выявлено образование, располагающееся в проекции указанных сосудов или их фрагментов, имеющее смешанную эхогенность и выражено неоднородную структуру, в которой могут
дифференцироваться множественные мелкие извитые трубчатые структуры. При использовании допплеровских методик в них удается получить спектр, соответствующий только венозному сосуду, в отличие от истинных образований, где присутствует и артериальное кровоснабжение.
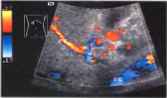
Рис.15. Кавернозная трансформация воротной вены. Извитые сосуды образовались вследствие опухолевой инфильтрации воротной вены (пятнистые синие и красные сосуды представляют собой извитые коллатерали) и ее окклюзии. PV - неизмененный внутрипеченочный сегмент воротной вены, VC - нижняя полая вена.
Гистоморфологически это образование представляет собой конгломерат из тромбированной воротной вены, фрагмента сальника и множества постоянно тромбирующихся, реканализирующихся и вновь открывающихся коллатералей.
При неонкологических заболеваниях тромбоз чаще развивается из-за локального нарушения системы свертывания крови и образования сгустка в просвете воротной вены. Эхографическая картина обусловлена наличием в просвете воротной вены неоднородного образования, смешанной эхогенности с неровными и нечеткими контурами, препятствующего кровотоку. Размеры сгустка могут быть различными — от 0.5 см до полной окклюзии воротной вены и даже ее ветвей и частично образующих ее сосудов (селезеночной, верхней и нижней брыжеечных вен).
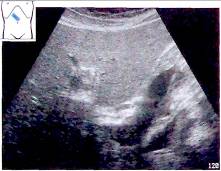
Рис.16. Расширение воротной вены при ее тромбозе.
Относительно редко встречается тромбофлебит внутрипеченочных ветвей воротной вены с последующим ее тромбозом. При опухолевых поражениях в просвете воротной вены образуется опухолевый тромб, также препятствующий кровотоку.
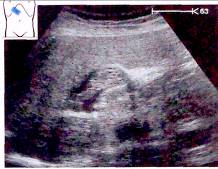
Рис. 17. Визуализация эхогенной ткани в просвете воротной вены.
Его изображение в большинстве случаев имеет неровные, бугристые контуры, умеренно неоднородную солидную структуру повышенной или смешанной эхогенности. Размеры обычно небольшие — в пределах 3-5 см. Указанные изменения могут быть выявлены с высокой степенью достоверности при эхографии в В-режиме и с использованием допплеровских методик.
Первичный портальный фиброз является врожденным заболеванием с прогрессирующим течением. Нарушение портальной гемодинамики происходит из-за прогрессирующего фиброза в перипортальных отделах, воротах печени. При эхографии выявляются признаки диффузных изменений паренхимы печени в виде небольшого увеличения размеров печени, неоднородности ее структуры и смешанной эхогенности, изменения сосудистого рисунка. В области ворот печени могут выявляться порто-портальные коллатерали — анастомозы между магистральным стволом воротной вены и ее мелкими ветвями в воротах и паренхиме печени, минуя фиброзированные участки, которые могут иметь вид гиперэхогенных "пятен" в проекции ворот. Эти изменения также могут быть обнаружены с высокой степенью достоверности при эхографии в В-режиме и с использованием допплеровских методик.
При синдроме Бадда-Киари первичным является нарушение оттока по печеночным венам в результате облитерирующего эндофлебита либо в результате их сдавливания или окклюзии в связи с другими причинами —
опухоли, тромбозы, цирроз, перикардит и т.п. Затем, после развития нарушений оттока крови из печени по печеночным венам и повреждения паренхимы с появлением в эхографической картине увеличения
печени и признаков диффузного поражения паренхимы (повышения эхогенности, мелко- и крупноочаговой неоднородности структуры, обеднения сосудистого рисунка), может развиваться портальная гипертензия.
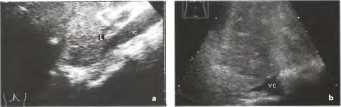
Рис. 18. Синдром Бадда-Киари. а Острый синдром Бадда-Киари: метастазы карциномы яичника в лимфатические узлы (L), полностью инфильтрирующие полую вену (VC) в месте впадения печеночных вен. b Хронический вторичный синдром Бадда-Киари: диффузные печеночные метастазы из карциномы бронха. Печеночные вены облитерированы до уровня полой вены (VC). проходимость которой еще сохранена.
При эхографии важно выявить причину, приведшую к нарушению оттока крови по печеночным венам.
Для этого тщательно исследуется область устьев печеночных вен и нижней полой вены, особенно область I, II, VII и VIII сегментов печени. Частой внепеченочной причиной портальной гипертензии является сдавливание воротной вены в области печеночно-двенадцатиперстной связки различными опухолями, измененными лимфатическими узлами или инфильтративными воспалительными образованиями. Своеобразие эхографической картины зависит от причины, вызвавшей сдавление.
Исследование важнейших путей оттока лимфы от печени.
Нормальный размер абдоминальных лимфатических узлов составляет 7—10 мм. Увеличенные нормальные лимфатические узлы, достигающие 20 мм в длину, могут быть обнаружены в паховой области и вдоль дистальной части наружной подвздошной артерии (рис. 19). Во всех случаях увеличения лимфоузлов следует проводить контрольные исследования для определения динамики изменения их размеров — например, для оценки эффективности химиотерапии. Кроме того, любая гепато или спленомегалия должна быть документирована и выражена в цифрах.
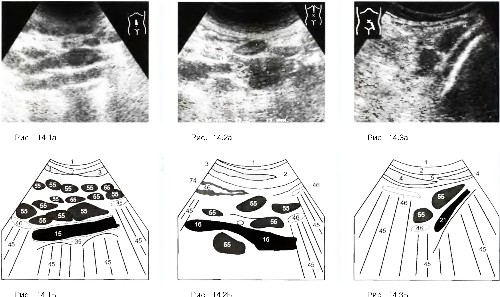
Рис. 19
Лимфатические узлы, обычно гипоэхогенные, следует дифференцировать от заполненных жидкостью петель кишечника по отсутствию перистальтики и от вен по малой подверженности компрессии. Компьютерная томография является лучшим методом диагностики тромбоза вен (не сдавливаемых при пальпации) или у чрезвычайно тучных пациентов, однако сонография более предпочтительна у худощавых или кахектичных пациентов. Увеличенные лимфатические узлы могут быть обнаружены при воспалительном процессе, злокачественной лимфоме (болезнь Ходжкина или неходжкинская лимфома) и метастатическом поражении.
В настоящее время отсутствуют надежные критерии для проведения дифференциального диагноза доброкачественных и злокачественных поражений лимфатических узлов.
В то же время принято считать , что лимфатические узлы, увеличенные на фоне воспаления, всегда имеют относительно небольшой размер (<2 см), продолговатую овальную форму и гипоэхогенную структуру. Они имеют четкий контур, два слоя с расположенным в центре участком повышенной эхогенности в области ворот (признак жировой ткани в воротах) и периферическую эхогенность как у печени. Нередко причиной воспалительных изменений лимфатических узлов в области ворот печени становится острый гепатит, воспалительные изменения наблюдаются также при хронических заболеваниях печени и желчных путей. При хронических воспалительных заболеваниях печени размер лимфатических узлов, как правило, не изменяется.
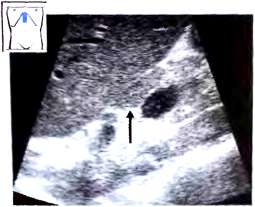
Рис.20. Лимфатический узел (^) в воротах печени при хроническом гепатите С.
Лимфатические узлы, пораженные метастазами опухолей, напротив, скорее округлые, чем овальные, часто неоднородной структуры и имеют нечеткий контур. Они также склонны образовывать конгломераты. Зная пути лимфооттока, можно определить место первичной опухоли. Например, парааортальная лимфаденопатия у пациентов молодого возраста может говорить об опухоли яичек или поражение лимфатических узлов в месте разветвления чревного ствола при раке желудка.
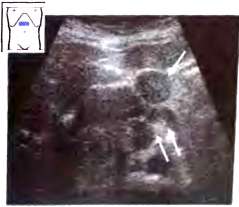
Рис. 21. Лимфатический узел (v) в месте разветвления чревного ствола (^^) при раке желудка.
Увеличенные лимфатические узлы при злокачественной лимфоме, в основном, овоидной формы, со смазанными краями и более гипоэхогенные, чем при воспалительном процессе или метастазировании опухоли. В одной трети случаев в селезенке обнаруживаются сопутствующие очаговые или диффузные изменения. Преимущественное вовлечение брыжеечных лимфатических узлов свидетельствует о неходжкинской лимфоме и исключает болезнь Ходжкина, при которой вовлекаются грудные и забрюшинные лимфатические узлы.
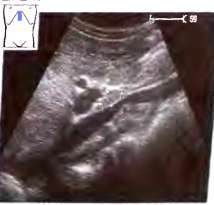
Рис. 22. Лимфатический узел (маркер) кпереди от полой вены при неходжкинской лимфоме.
Увеличенные лимфатические узлы, расположенные по ходу крупных сосудов, часто визуализируются при последовательных осмотрах па поперечном сечении. Они видны как округлые гипоэхогенные объемные образования, появляющиеся и исчезающие на коротком протяжении. Злокачественная лимфома искривляет или смещает соседние сосуды, но не поражает стенку сосудов и соседние органы.
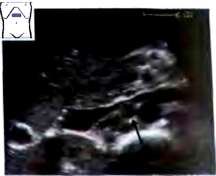
Рис.23. Лимфатический узел (^) между полой веной аортой.
Жировая инфильтрация печени и другие очаговые изменения её паренхимы
Одной из наиболее частых находок при проведении исследования является повышение эхогенности паренхимы печени при жировой инфильтрации.
Этиология жировой инфильтрации печени (жирового гепатоза, стеатоза печени, жировой дистрофии печени) может быть весьма разнообразна и вызывается токсическими агентами, несбалансированным питанием, врожденными и приобретенными эндогенными метаболическими нарушениями. Однако эхографическая картина жировой инфильтрации зависит не столько от причины, сколько от тяжести и распространенности поражения.
Жировая инфильтрация или стеатоз печени вызывает диффузное увеличение эхогенности печени. Это повышение эхогенности лучше всего оценивать при сравнении с эхогенностью почки. У здоровых пациентов эхогенность печени и почек почти одинакова. Отражение звука, вызванное выраженной жировой инфильтрацией, приводит к акустическому ослаблению, которое нарастает в печени пропорционально расстоянию от датчика. В результате сниженная эхогенность задних отделов печени может быть недостаточной для исследования
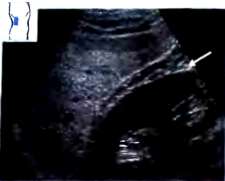
Рис. 24. Жировая инфильтрация печени. Эхогенность паренхимы печени значительно выше эхогенности ткани почки. Большие скопления жира вокруг почки (<). Ожирение.
Диффузная форма жировой инфильтрации печени характеризуется тем, что дистрофические изменения захватывают практически всю паренхиму печени с различной степенью интенсивности или практически одинаково. Могут встречаться отдельные участки неизмененной паренхимы. Они, прежде всего, обнаруживаются в непосредственной близости от воротной вены или желчного пузыря (14) (рис. 26) Следует еще раз подчеркнуть, что эти изменения не имеют признаков объемного образования. Расположенные рядом сосуды не смещены (рис. 25); периферически рас положенные области повышенной или относительно сниженной эхогенности жировой инфильтрации не дают выпячивания контура печени и не вдавливают желчный пузырь, как это иногда бывает в случаях опухолей или метастазов.
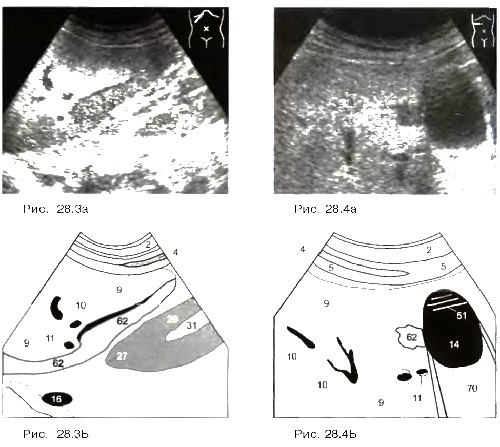
Рис. 25 Рис. 26.
При диффузной и отчасти локальной форме жировой инфильтрации размеры печени обычно увеличиваются — преимущественно за счет измененных отделов. Форма органа не нарушается. Контуры остаются ровными, однако, при выраженных изменениях появляется их закругленность, особенно нижнего края, более выраженная в поздних стадиях.
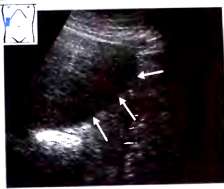
Рис. 27. Жировая инфильтрация печени. Закругление нижнего края печени (^^^).
Звукопроводимость органа чаще понижена за счет того, что ткань, содержащая жировые включения, обладает способностью рассеивать, отражать и поглощать ультразвуковое излучение в большей степени, нежели неизмененная. Вследствие этого глубокие отделы печени и диафрагма, как правило, визуализируются неотчетливо. Достоверно отмечается повышение эхогенности измененной паренхимы, коррелирующее по выраженности со степенью тяжести процесса и сопровождающееся, в большинстве случаев, акустическим эффектом ослабления ультразвука в глубоких слоях паренхимы. Характер повышения эхогенности паренхимы при диффузной и локальной формах также может быть разнообразным — как равномерным, так и фокусовидным — в виде практически равномерного повышения эхогенности всех измененных участков паренхимы или фокусовидного изменения эхогенности, когда в некоторых местах интенсивность отражения выше, чем по соседству, и имеет вид нечетко очерченного круга с расплывчатым контуром. В некоторых случаях при этих формах жировой инфильтрации в паренхиме печени могут выявляться участки, пониженной эхогенности. которые имеют вид гипоэхогенного образования, хотя на самом деле являются фрагментами менее измененной паренхимы. Структура паренхимы печени при жировой инфильтрации обычно остается однородной. При нарастании морфологических изменений в органе структура паренхимы приобретает зернистый вид. Исключение составляют случаи, когда эти изменения сочетаются с другими дистрофическими процессами в органе. Сосудистый рисунок печени претерпевает значительные изменения, пропорциональные распространенности и степени выраженности дистрофических процессов.
При очаговой форме выявляются единичные участки жировой инфильтрации, которые напоминают гиперэхогенные объемные образования.
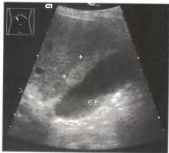
Рис.28. Очаговая жировая инфильтрация (стрелки), типичная локализация вблизи ложа желчного пузыря: овальная эхогенная структура. GB - желчный пузырь.
Отмечается "сглаженность” (меньшая отчетливость) сосудистого рисунка, обусловленная в первую очередь ухудшением визуализации мелких ветвей печеночных вен, которые не выделяются на фоне высокоэхогенной паренхимы из-за отсутствия четко видимых стенок. Ветви воротной вены, как правило, визуализируются лучше (рис 29.), благодаря своим высокоэхогенным стенкам, однако, и они могут быть выявлены с трудом при резко выраженных изменениях паренхимы. Нарушения печеночной гемодинамики при данной патологии длительное время не происходит
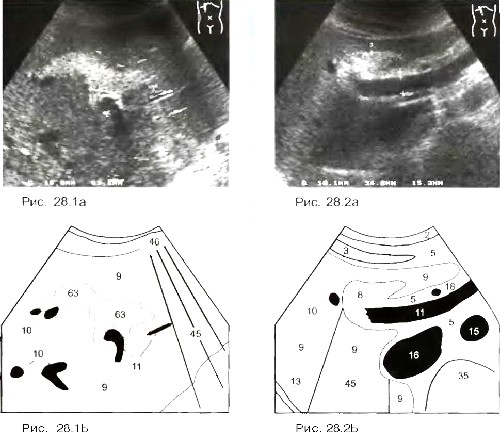
Рис. 29.
Применение методики цветового допплеровского исследования помогает обнаружить практически невидимые в В-режиме мелкие и, иногда, средние ветви печеночных вен и воротной вены и, соответственно, более четко оценить характер изменений в паренхиме печени.
При очаговой форме жировой инфильтрации патологические изменения обычно захватывают лишь небольшой участок паренхимы, поэтому существенных изменений размеров, контуров, эхогенности, структуры и сосудистого рисунка печени в целом не происходит. В зоне такого ограниченного участка отмечается повышение эхогенности паренхимы с однородной структурой паренхимы или иногда с зернистым текстурным рисунком, весьма напоминающее собой гиперэхогенное объемное образование. Сосудистый рисунок печени в зоне измененного участка паренхимы не претерпевает каких-либо существенных изменений. Различия очаговой жировой инфильтрации и очагового фиброза печени незначительны. Очаговый фиброз печени имеет более неоднородную гиперэхогенную текстуру очагов, часто с неправильными очертаниями . Сосудистый рисунок в зоне очагов фиброза может быть несколько деформирован.
Нередко достаточно сложную проблему для исследователя создают очаговые изменения и паренхиме печени. Некоторые из них без особых затруднений верифицируются по ультразвуковым особенностям, диагностика других требует проведения детального анализа с привлечением иных методов обследования. При первичном обнаружении очаговых изменений в паренхиме печени необходимо оценить следующие параметры:
- Эхогенность: анэхогенное, гипоэхогенное, эхогенность образования равна эхогенности паренхимы печени, эхогенное, гиперэхогенное, дистальное акустическое усиление, ослабление проведения ультразвукового сигнала;
- форма: круглая, овальная, неравномерная, треугольная, многоугольная;
- границы: четкие, нечеткие;
- размеры: измерение дастся, как минимум, в двух плоскостях;
- структура: гомогенная/негомогенная, гипоэхогенный/гиперэхогенный ободок, гипоэхогенный/гиперэхогенный центр;
- число: солитарный узел, множественные узлы, многочисленные;
- положение: положение внутри печени (правая доля, левая доля, сегмент), близость кровеносных сосудов;
- окружающая ткань: смещена, инфильтрирована
В группе доброкачественных солидных образований печени при ультразвуковом исследовании имеется возможность выявить и в большинстве случаев дифференцировать такие образования, как гемангиома, очаговая узловая гиперплазия и аденома печени.
Гемангиомы являются одним из наиболее часто встречающихся доброкачественных образований печени. Самовыявление гемангиом в подавляющем большинстве случаев не представляет существенных затруднений в отличие от их дифференциальной диагностики от ряда доброкачественных и злокачественных очаговых поражений печени.
Гемангиомы печени имеют равномерно повышенную эхогенность (яркие) в сравнении с остальной тканью печени, ровные контуры без эхогенного ободка. В непосредственной близости от них может быть обнаружена дренирующая печеночная вена обычного диаметра (не расширенная). Большинство гемангиом маленькие, но достигнув значительных размеров, могут становиться преимущественно гетороэхогенными, что затрудняет окончательный диагноз (рис 30).
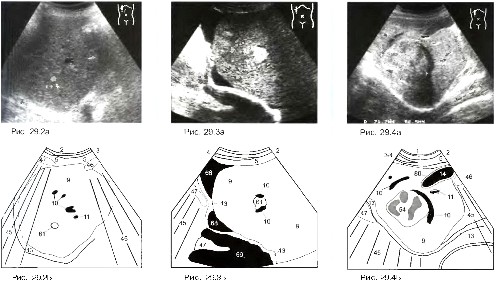
Рис. 30.
Эхографически гемангиомы подразделяются на две группы — капиллярные и кавернозные, имеющие некоторые отличия по ряду эхографических признаков, обусловленных особенностями их гистологического строения. Так, капиллярные гемангиомы представлены множеством крайне мелких полостных структур, которые находятся за пределами разрешающей способности ультразвуковых сканеров, что создает впечатление практически однородной структуры
В противоположность этому кавернозные гемангиомы имеют в своей структуре наряду с мелкими достаточно крупные полости, которые дифференцируются при ультразвуковом исследовании как эхонегативные или гипоэхогенные участки (Рис.31).
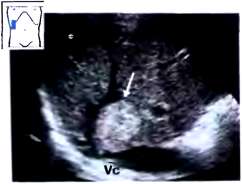
Рис.31. Гиперэхогенная большая гемангиома, сдавливающая печеночную вену (v). Vc — полая вена.
Капиллярные гемангиомы обычно располагаются в непосредственной близости от ветвей печеночных вен и ветвей воротной вены. Форма капиллярных гемангиом приближается к округлой или эллипсоидной. Контуры гемангиом достаточно четкие, хорошо дифференцируются от окружающей паренхимы печени, за исключением случаев выраженных диффузных изменений печени, таких, как жировая инфильтрация, хронический гепатит с выраженными морфологическими изменениями, цирроз и ряд других поражений печени. Несмотря на четкость, во многих случаях контуры гемангиом бывают неровным. Изменений со стороны окружающей паренхимы печени обычно не наблюдается.
Размеры капиллярных гемангиом обычно не превышают 30-40 мм в диаметре. Эхогенность капиллярных гемангиом обычно значительно превышает эхогенность паренхимы печени, хотя имеются сообщения о возможной пониженной эхогенности ткани гемангиомы.
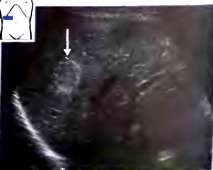
Рис. 32. Относительно гипоэхогенная гемангиома(v).
Структура капиллярных гемангиом в большинстве случаев выглядит однородной с мелкосетчатым текстурным рисунком. При относительно больших размерах в структуре капиллярных гемангиом могут дифференцироваться участки неоднородности, имеющие некоторые отличия в текстуре и эхогенности от основной массы образования. За гемангиомой может определяться неотчетливо выраженный эффект дистального псевдоусиления эхосигнала, главным образом, за крупными капиллярными или кавернозными гемангиомами. Во многих случаях может выявляться несколько образований.
Особенностью капиллярных гемангиом печени является медленный рост при динамическом наблюдении, которое
осуществляется в зависимости от конкретных условий через 3-6 месяцев. Применение допплеровских методик исследования в большинстве случаев не дает дополнительной информации — при цветовом исследовании даже в режиме энергетического цветового допплеровского исследования редко удается выявить сигнал из структуры гемангиомы. Аналогичная ситуация складывается и с методикой импульсного допплеровского исследования. Эхографическая картина кавернозных гемангиом печени имеет ряд отличий от капиллярных. Эти отличия заключаются, прежде всего, в размерах и структуре образований. Так, располагаясь в паренхиме печени так же, как и капиллярные гемангиомы, кавернозные гемангиомы имеют обычно большие размеры, достигая 80-150 мм в диаметре, и, соответственно, бывает сложно определить первично питающий сосуд. Форма кавернозных гемангиом может быть достаточно разнообразной. Контуры обычно неровные. Структура также отличается разнообразием ввиду наличия кавернозных полостей, которые создают эффект неоднородности структуры в виде гипо- и анэхогенных участков различного размера и конфигурации, что приводит к определенным трудностям в дифференциальной диагностике данных образований. Ввиду наличия кавернозных полостей достаточно большого размера часто выявляется эффект дистального псевдоусиления эхосигнала от кавернозных участков. Рост данных образований тоже имеет медленный характер. Признаков инвазии печеночной паренхимы, характерных для злокачественных образований не выявляется. Применение допплеровских методик обычно дает результаты, аналогичные указанным для капиллярных гемангиом, хотя визуализация кровотока в ткани гемангиомы и получение ряда его параметров возможна в большем проценте случаев. Необходимо, однако, учитывать, что в этих случаях обычно выявляются нормальные печеночные сосуды, оказавшиеся в проекции
гемангиомы из-за ее больших размеров. Дифференциальная диагностика капиллярных и кавернозных гемангиом
печени основывается на выявлении характерных эхографических признаков при первичном исследовании и учете клинико-анамнестических данных, а также при динамическом наблюдении. К важным параметрам, учитываемым при проведении дифференциальной диагностики гемангиом, относятся: локализация, форма и характер контуров, структура и эхогенность, количество и медленный рост .
В ряде случаев данных, получаемых при ультразвуковом исследовании, недостаточно для установления определенного диагноза. Особенно часто такая ситуация наблюдается либо при множественных мелких и крупных гемангиомах.
либо при крупных кавернозных гемангиомах. При отсутствии возможности провести дополнительно компьютерное томографическое исследование с контрастированием, магнитно-резонансную томографию или селективную
ангиографию бывает необходимо верифицировать диагноз с помощью пункции под визуальным контролем. При такой постановке вопроса необходимо помнить о возможности осложнений, в первую очередь связанных с обильными кровотечениями и возможным обсеменением при злокачественных новообразованиях и эхинококкозе. Поэтому пунктировать кавернозные гемангиомы и образования, подозрительные на эхинококковое поражение (без результатов серологического исследования), не рекомендуется.
Очаговая узловая гиперплазия печени является относительно редко встречающейся врожденной патологией печени. Она, как правило, гипоэхогенна. Однако в некоторых случаях она может иметь эхогенность, равную эхогенности паренхимы печени. Следует отметить, что часто не удается на основании данных, полученных в результате ультразвукового исследования, провести дифференциальный диагноз с аденомой или атипичной гемангиомой Большей частью этот вид доброкачественного поражения печени встречается у женщин, и его частота имеет тенденцию к увеличению. В последнее время отмечен рост количества наблюдений очаговой узловой гиперплазии печени. Данное образование морфологически представлено нормальными компонентами печеночной паренхимы. Единственным отличием от нормальной паренхимы печени является нарушение долькового строения паренхимы в зоне образования. Эхографическая картина данного доброкачественного поражения печени может быть достаточно разнообразной. Разнообразие обусловлено, как правило, размерами и эхографическим типом узловой гиперплазии. При небольших размерах узловой гиперплазии изменения размеров, контуров и формы печени обычно не наблюдаются. При крупных размерах образования, сопоставимых с размерами доли печени, в которой оно располагается, наступают соответствующие изменения со стороны этого отдела печени. Очаговая узловая гиперплазия может располагаться в любом отделе печени, однако, наиболее частой локализацией является правая доля (чаще V, VI, VII сегменты). Размеры образования также весьма вариабельны — от 0,5 до 20,0 см в диаметре. Рост образования весьма медленный, многолетний.

Рис.33. Очаговая узловая гиперплазия (v).
Форма образования обычно приближается к округлой. Контуры обычно ровные и. в зависимости от типа эхогенности, могут быть либо достаточно отчетливыми, либо расплывчатыми. Капсула не визуализируется, поскольку отсутствует. Структура образования имеет диффузную мелкоочаговую неоднородность, иногда с неотчетливым радиальным строением. Эхогенность очаговой узловой гиперплазии печени может быть трех вариантов: ниже или выше эхогенности окружающей паренхимы и изоэхогенной — сопоставимой по эхогенности с окружающей паренхимой, что серьезно затрудняет проведение дифференциальной диагностики между данным образованием и другими очаговыми и диффузными изменениями. Чаще всего встречаются гиперэхогенные узлы.
При проведении дифференциальной диагностики следует учитывать, что поражения печени, эхогенность которых равна эхогенности паренхимы это: очаговая узловая гиперплазия, гепатоцеллюлярная карцинома, метастазы, гемангиома.
Очаговая узловая гиперплазия часто выглядит как ограниченный цирротически измененный участок на фоне
нормальной паренхимы печени. Сосудистый рисунок печени может изменяться в зоне расположения очага при достижении последним размеров, приводящих к деформации или сдавлению крупных ветвей внутрипеченочных сосудов.
Применение методик допплеровского исследования, особенно цветового и энергетического вариантов, позволяет наглядно выявлять эти изменения. При использовании импульсного допплеровского исследования важным, хотя и не абсолютно однозначным, параметром является отсутствие сосудов с атипичным спектром кровотока, в той или иной мере характерным для злокачественных новообразований. В зависимости от степени изменения состояния сосудов могут развиваться те или иные вторичные изменения гемодинамики печени — портальная гипертензия. Нарушения кровотока по печеночным венам и т.д. с характерными эхографическими признаками. Протоковая система печени может претерпевать такие же изменения, как и сосудистый рисунок при больших размерах образования.
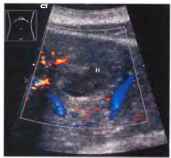
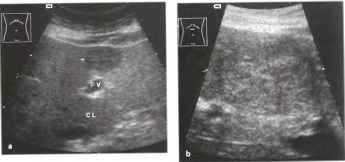
Рис. 34. Очаговая узловая гиперплазия. а Гипоэхогенное образование (стрелки) в сегменте III. PV - центральная воротная вена, CL - хвостатая доля, b Увеличенное изображение: смутно различимый звездчатый рубец (эхогенная структура в форме звезды), с ЦДЭ: сосудистый рисунок по типу «спиц колеса». Наличие звездчатого рубца и картины «спиц колеса» позволяет установить диагноз, дополнительное контрастирование помогает в постановке диагноза.
В дифференциальной диагностике очаговой узловой гиперплазии печени особое внимание уделяется не только выявлению признаков локального изменения структуры и эхогенности паренхимы печени и степени их выраженности, но и получению убедительных данных в пользу того, что неоднородность паренхимы не связана с солидным злокачественным поражением печени, а также дифференциации выявленных изменений от эхографической картины при некоторых диффузных поражениях печени. При наличии гипербилирубинемии и портальной гипертензии требуется более пристальное внимание к мельчайшим эхографическим признакам. Необходимо отметить, что во многих случаях установить окончательный диагноз возможно только при использовании пункционной биопсии под визуальным контролем (эхография, компьютерная томография). Выбор методики визуального контроля обусловлен особенностями пациента и материально-технической базой конкретной клиники.
Аденомы печени встречаются достаточно редко. Еще реже эти доброкачественные образования могут быть дифференцированы от ряда других очаговых поражений печени только по данным эхографии. В отличие от очаговой узловой гиперплазии и гемангиом печени аденомы могут исходить как из гепатоцитов, так и эпителия желчных ходов, или иметь смешанное происхождение. В связи со значительной вариабельностью эхографической картины, аденому печени бывает достаточно сложно, а в ряде случаев и невозможно, дифференцировать от других очаговых поражений печеночной паренхимы.
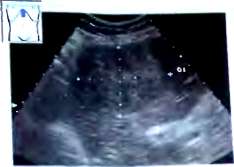
Рис.35. Аденома печени.
В эхографической картине аденомы печени могут присутствовать различные варианты, связанные с изменчивой эхогенностью и структурой.
Локализоваться аденома может в любом отделе печени. При небольших размерах аденомы не происходит
существенных отклонений в общей эхографической картине печени — в форме, размерах, строении. При локализации вблизи капсулы печени могут выявляться признаки деформации поверхности печени и при достаточно крупных размерах опухоли возможно нарушение не только формы, контуров и размеров печени, но и ее внутренней структуры, включая сосудистый рисунок. Эхографическая картина аденомы печени представляет собой образование неправильной округлой формы различного размера. Контуры аденомы достаточно четкие, хотя могут быть неровные. Четкость контуров,
отличающая аденому от ряда других очаговых поражений печени, обусловлена наличием тонкой соединительнотканной капсулы. Сама капсула может отчетливо не визуализироваться, особенно на фоне каких-либо диффузных изменений паренхимы печени, однако, четкость отграничения сохраняется (рис. 35). Эхогенность аденомы может быть разнообразной — и гипоэхогенной, и изоэхогенной, и гиперэхогенной, и, наконец, иметь смешанный вариант.
Структура образования большей частью представлена достаточно однородной текстурой, но иногда, особенно при больших размерах аденомы, могут выявляться участки неоднородности с нечеткими контурами, имеющие иную, нежели основная масса, эхогенность (рис. 36). При достаточно больших размерах, а также при расположении вблизи от внутрипеченочных сосудов, можно наблюдать деформацию сосудистого рисунка печени, что наглядно проявляется при использовании методик цветового допплеровского исследования. Импульсная допплерография обычно не выявляет каких-либо характерных для этого заболевания данных по параметрам кровотока. Случаи малигнизации редки и рост аденомы печени достаточно медленный, что позволяет проводить дифференциальную диагностику, в том числе и при динамическом наблюдении.
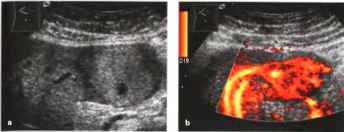
Рис.36. Аденома печени, а Изоэхогенная опухоль с анэхогенным очагом некроза/кровоизлияния. b Энергетическая допплерометрия: четко визуализируется васкуляризация с артериальным характером кровоснабжения. Гистологическое исследование: гепатоцеллюлярная аденома.
Несмотря на наличие некоторых, казалось бы, характерных эхографических признаков, дифференциальная диагностика этого доброкачественного поражения, базирующаяся только на данных эхографии, крайне затруднена.
Достаточно часто встречаются аденомы, имеющие весьма неоднозначную эхографическую картину. Все это приводит к необходимости получения более точных данных с помощью пункционной биопсии под контролем ультразвука либо других методов верификации.
В группе доброкачественных кистозных образований печени при ультразвуковом исследовании имеется возможность выявить и в большинстве случаев дифференцировать такие образования, как врожденные множественные и солитарные кисты, приобретенные посттравматические, паразитарные и воспалительные кисты печени.
В связи с особенностями распространения ультразвука в мягких тканях и жидкостях, у кистозных образований выявляется ряд специфических артефактов:
— эффект усиления дальней стенки — большая яркость этого участка стенки, чем боковых отделов;
— эффект дистального псевдоусиления эхосигнала — линейное или конусовидное повышение эхогенности подлежащих тканей по сравнению с тканями, находящимися по соседству на той же глубине;
— эффект боковых теней — появление акустической тени или ослабления эхосигнала от боковых стенок кисты;
— эффект реверберации — появление повторяющихся искаженных отражений стенки кисты, проецирующихся на изображение полости кисты в области передней стенки.
Диагностика подобных образований размерами около 5 мм не вызывает особых затруднений. Солитарные, как правило, врожденные кисты обнаруживаются приблизительно у 4% взрослых людей. Для подобных кист характерны округлая или овальная форма, гладкая граница, тонкая стенка, анэхогенность без внутренних включений, а также дистальное акустическое усиление и краевая тень. Диагноз ставится на основании данных ультразвукового исследования. Множественные кисты встречаются значительно реже.
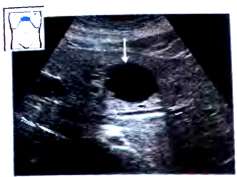
Рис. 37. Киста печени. Образование имеет округлую форму, гладкие контуры, отсутствует отражение от стенки кисты, видны дистальное акустическое усиление, краевая тень.
Врожденные кисты печени в большинстве случаев являются результатом нарушения развития внутрипеченочных желчных протоков или их окклюзии. Значительно реже встречаются дермоидные кисты печени. Практически важным является разделение врожденных кист печени на простые солитарные кисты и поликистоз печени. Последний может часто сочетаться с поликистозом почек и поджелудочной железы. Простые солитарные кисты печени обычно имеют характерную эхографическую картину. При ультразвуковом исследовании выявляются одиночные жидкость содержащие образования различной локализации. Чаще
всего простые солитарные кисты имеют форму, близкую к округлой или неправильной округлой. Размеры могут колебаться в интервале от нескольких миллиметров до десятков сантиметров. При эхографии достаточно хорошо дифференцируются стенки кисты в виде тонкой гиперэхогенной линии вокруг эхонегативной полости. Особенно хорошо выявляется задняя стенка (по отношению к направлению распространения луча). Толщина стенки кисты обычно невелика — до 1-1,5 мм. Ввиду этого на некоторых типах ультразвуковых приборов с недостаточно высокой разрешающей способностью стенки могут четко не дифференцироваться. Самообразование эхографически представляет собой эхонегативную зону в паренхиме печени без каких-либо внутренних структур. Однородное жидкое содержимое кисты (в большинстве случаев желчь или межтканевая жидкость) обеспечивает беспрепятственное проведение ультразвука.
При больших размерах простые солитарные кисты могут приводить к увеличению размеров печени, изменению ее формы, нарушению внутренней структуры с возможным в редких случаях нарушением печеночной гемодинамики и оттока желчи.
Рис. 38. Солитарная киста печени, сдавливающая правую печеночную вену (^).
Применение методики цветового и импульсного допплеровского исследования демонстрирует полное отсутствие кровотока в толще стенки кисты, что иногда является важным дифференциально-диагностическим признаком. Иногда при цветовом допплерографическом исследовании можно заметить слабо выраженные цветовые сигналы, как в области стенок, так и в полости кисты. При истинных кистах печени эти сигналы являются артефактами и быстро исчезают при изменении параметров исследования. Важно помнить также и о возможных осложнениях солитарных кист — нагноении, разрыве и кровоизлияниях в стенки или полость кист. Эти процессы могут существенно изменить эхографическую картину кист, особенно структуру их полости — привести к появлению взвешенных элементов и нитей, сгустков и перегородок. Аналогичная картина, хотя и редко, может наблюдаться при малигнизации кисты, когда выявляются либо утолщение капсулы кисты, либо появление пристеночного солидного компонента или перегородок с вегетациями и т.п., особенно с наличием цветового допплеровского сигнала от этих структур. В такой ситуации требуется тщательная оценка анамнеза и клинико-лабораторной картины заболевания.
Множественные кисты наблюдаются при поликистозе печени. Во многих случаях при поликистозе поражаются все доли печени. При этом может отмечаться увеличение размеров и деформация печени. Поверхности могут иметь множественные выбухания при субкапсулярном расположении кист. При поликистозе отмечается большое разнообразие размеров кист, часто выявляется неровность их контуров. Стенки кист могут дифференцироваться не вполне отчетливо при массивном поражении. Остальные эхографические признаки, относящиеся к эхографической картине кист, не отличаются от таковых у простых солитарных кист. При массивных поражениях структура паренхимы печени выглядит неоднородной не только из-за множественных разноразмерных эхонегативных образований с эффектом дистального псевдоусиления, но и из-за множественных мелких линейно-точечных гиперэхогенных участков. Сосудистый рисунок печени может быть, как деформирован, так и нечетко дифференцироваться из-за множества мелких эхонегативных участков в структуре паренхимы печени (кист). В этом случае при наличии конкретных задач оказывает помощь методика цветового допплеровского исследования, четко дифференцирующая эхонегативные структуры в паренхиме печени на кровеносные сосуды и кисты, а также желчные протоки при их расширении.
Рис.39. Множественные крупные (8 см) кисты печени (^^).
Дермоидные кисты печени являются достаточно редким явлением. По своей эхографической картине они больше напоминают солидные образования, нежели кисты. Главным отличием от простых кист печени является наличие достаточно густого и неоднородного внутреннего содержимого, вплоть до кальцинированных структур. В то же время во многих случаях сохраняется большинство побочных эффектов (кроме реверберации), присущих практически любому жидкостному образованию, что в свою очередь отличает эти образования от солидных. Капсула дермоидных кист обычно хорошо дифференцируется при ультразвуковом исследовании в виде гиперэхогенной пинии, огибающей образование.
Дифференциальная диагностика кист печени основывается на выявлении характерных эхографических признаков, свойственных жидкостным структурам, и учете клинико-анамнестических данных. Динамическое наблюдение в затруднительных случаях позволяет решать ряд дифференциально-диагностических вопросов.
Приобретенные (ложные) кисты печени могут иметь воспалительное, травматическое и паразитарное происхождение. Различный генез этих трех вариантов кист обуславливает и различие в их эхографической картине, анамнезе и клинической картине, что позволяет сделать наиболее правильный вывод.
Посттравматические кисты печени. К травматическим кистам печени наиболее часто относят гематомы, биломы и серомы. Выявление при эхографии подобного образования довольно часто позволяет установить анамнестическую связь с травмой. Во многих случаях знание характера травматического воздействия и его направления помогает трактовать выявляемые при эхографии изменения. Принципиально важной является дифференциация повреждения на два вида — с разрывом капсулы печени и без такового. Первый вариант сопровождается кровотечением в брюшную полость и может привести к летальному исходу. Второй — в большинстве случаев ограничивается образованием внутрипеченочной гематомы или биломы.
Эхографическая картина гематомы имеет определенную динамику, связанную с характером травмы (острая или тупая), со временем существования гематомы и возможным повторяющимся поступлением свежей крови. После
тупой травмы в паренхиме печени может выявляться либо участок пониженной эхогенности с неровными и иногда нечеткими контурами либо небольшой участок нарушения структуры паренхимы с гипоэхогенным ореолом.
Локализация может быть разнообразной, но, как правило, гематомы располагаются вдоль условной линии удара ближе к поверхностным участкам паренхимы, часто вплотную к капсуле печени, приводя в дальнейшем к локальному выбуханию на поверхности.
Рис.40. Внутрипеченочная гематома (v).
Затем формируется эхонегативная жидкость содержащая полость. Позднее начинаются процессы организации гематомы, эхографически отображающиеся как неравномерное повышение эхогенности полости гематомы с появлением в ней сгустков и нитей фибрина в виде образований смешанной и повышенной эхогенности и перегородок.
Рис. 41. Гематома (Н) в верхней части левой доли печени (L) Обнаружена случайно через несколько недель после выздоровления
После этого этапа дальнейшее развитие эхографической картины гематомы может идти несколькими путями. Во-первых, может продолжаться процесс организации, когда размеры гематомы уменьшаются, становится более, отчетливо видна ложная капсула в виде гиперэхогенного ободка, внутренняя структура приобретает вид солидного образования вплоть до появления участков кальцификации. Во-вторых, могут преобладать процессы лизиса с расщеплением внутренних компонентов гематомы и превращением содержимого гематомы в однородную жидкость с хорошими проводящими свойствами. В этом случае гематома превращается в вариант серомы и мало отличается по своему эхографическому изображению от простой солитарной кисты печени. В-третьих, возможно поступление небольших порций свежей крови из поврежденного, но не тромбированного сосуда. В этом варианте эхографическая картина гематомы как бы "замораживается' на этапе начала организации — в полости сохраняется и жидкое содержимое, и сгустки и нити фибрина. При динамическом исследовании даже в короткие промежутки времени может отмечаться изменение внутреннего рисунка гематомы и иногда увеличение ее размера. В-четвертых, у ряда пациентов может произойти нагноение гематомы с формированием достаточно типичной эхографической картины абсцесса печени.
Дифференциальная диагностика гематом в ряде случаев сложна ввиду возможных особенностей их внутреннего строения, особенно в фазе организации. Обязательным действием при подозрении на гематому печени, вне зависимости от наличия или отсутствия указаний на возможность внутрибрюшного кровотечения, является динамическое наблюдение за состоянием эхографической картины, по возможности через короткие промежутки времени, с параллельным учетом клинико-лабораторных показателей.
Серомы также являются одним из возможных вариантов травматического повреждения печени различного генеза — внешняя механическая тупая травма, интраоперационная травма или результат удаления инкапсулированного объемного образования из паренхимы печени, результат превращения гематомы и т.п. Эхографическая картина сером имеет постоянные и вариабельные признаки. К первым относятся характеристики полости — эхонегативное пространство, содержащее однородную жидкость (межтканевая жидкость). Ко вторым относятся параметры, связанные с характером травмы — размер, форма, четкость выраженности капсулы. В целом серомы в эхографическом изображении весьма напоминают солитарные кисты печени. Процесс формирования сером обычно занимает большее время, чем. скажем, гематомы или абсцесса.
В дифференциальной диагностике, сером от других кистозных образований учитываются как эхографические признаки, выявляемые при повторных исследованиях, так и данные клинической картины и анамнеза.
Биломы по своей эхографической картине также мало отличаются от простых солитарных кист печени и сером. Локализация билом может быть такой же, как и гематом. Учитывая тот факт, что содержимым биломы является желчь, поступающая из травмированного протока и имеющая характерные эхографические признаки, необходимо проводить периодические контрольные исследования с целью предупреждения возможного значительного увеличения биломы в размерах и ее разрыва с истечением содержимого в брюшную полость, что может привести к тяжелым последствиям.
Инфекционные и паразитарные поражения печени
Гепатит – это воспалительное заболевание печени. На сегодняшний день наукой идентифицировано несколько вирусов гепатита: A, B, C, D (дельта), Е, G, TTV. Вирусы гепатита A и E (в России вирус гепатита E встречается крайне редко) передаются как кишечные инфекции - с загрязненными продуктами и водой, через грязные руки. Острые гепатиты A и E не ведут к развитию хронического гепатита. Некоторые другие вирусы, не относящиеся к группе вирусов гепатита, например, вирус простого герпеса, цитомегаловирус, вирус Эпштейна–Барра, также способны вызывать острый гепатит, который не ведет к развитию хронического гепатита и цирроза печени. Лечением острых вирусных гепатитов, которые могут протекать очень тяжело, занимаются врачи-инфекционисты.
В зависимости от тяжести и стадии заболевании при остром гепатите могут происходить различные изменения эхографический картины. Некоторую роль в быстроте и выраженности динамики эхографической картины печени при остром гепатите могут играть этиопатогенетические факторы — варианты вирусных, токсических и метаболических поражений. Помимо однократного ультразвукового исследования, целесообразно проведение повторного, или повторных исследований в динамике — для контроля дальнейшего направления развития патологического процесса. Необходимым является сопоставление данных эхографии с результатами клинических, лабораторных и прочих инструментальных методов исследования. Несмотря на это, в подавляющем большинстве случаев сделать однозначные выводы об этиологии и патогенезе выявляемых при эхографии изменений на основании динамических изменений эхографической картины не представляется возможным.
Наиболее яркая эхографическая картина имеет место при тяжелой форме протекания заболевания. Размеры печени в фазе выраженной манифестации клинической картины могут начать уменьшаться — в этом случае клиницисты отмечают симптом "тающей льдинки". Эхогенность печени при прогрессирующем воспалительном процессе может продолжать снижаться ввиду более распространенного выраженного отека паренхимы. Причем структура паренхимы может казаться более однородной. При усугублении течения заболевания в паренхиме печени могут развиваться очаговые некрозы, которые эхографически могут выглядеть в острой фазе как гипо - и анэхогенные участки с нечеткими и неправильными контурами и неоднородной внутренней структурой. Отмечается обогащение сосудистого рисунка печени за счет еще более выраженной дифференциации сосудистых стенок мелких ветвей венозной и артериальной системы печени, которое само по себе создает дополнительное впечатление мелкоочаговой неоднородности паренхимы. Со стороны магистральных стволов печеночных вен изредка можно наблюдать преходящее уменьшение их диаметра. В некоторых случаях наступает также преходящее нарушение портального кровотока, выражающееся в незначительном увеличении размера основного ствола воротной вены, снижении показателей скоростного и объемного кровотока по воротной вене, иногда увеличении селезенки.
При средней тяжести течения в фазе манифестации заболевания форма органа обычно существенно не изменяется, контуры печени остаются ровными, четко очерченными. Капсула печени обычно дифференцируется лучше, чем в норме. Это обусловлено увеличением разницы акустических сопротивлений между паренхимой и капсулой. Часто отмечается увеличение размеров печени в большей степени за счет правой доли. Увеличивается как косой вертикальный размер, так и толщина правой доли. Контуры печени остаются ровными, края — острыми, хотя в некоторых случаях можно отметить их закругление. Контур диафрагмы обычно визуализируется отчетливо в виде непрерывной гиперэхогенной линии. Структура паренхимы печени в большинстве случаев неоднородная. Неоднородность паренхимы складывается из участков несколько сниженной, средней и относительно повышенной эхогенности, что соотносится с участками более или менее выраженной отечности паренхимы и неизмененных участков. У большинства пациентов наблюдается изменение сосудистого рисунка печени, выражающееся в более четкой визуализации стенок мелких ветвей воротной вены и печеночных вен — симптом выделяющихся сосудов — за счет повышения звукопроводимости паренхимы, на фоне которой лучше выделяются мелкие сосудистые структуры. Со стороны крупных стволов печеночных вен. воротной вены и печеночной артерии обычно диагностически существенных изменений не происходит.
В эхографической картине острого гепатита с менее выраженной клинико-морфологической симптоматикой отмечаются практически аналогичные изменения, однако степень их выраженности, а также продолжительность существования значительно меньше.
При регрессии воспалительного процесса эхографическая картина приближается к норме. При нетяжелом течении заболевания возможно практически полное восстановление нормального эхографического изображения печени. В случае тяжелого течения заболевания, наоборот, со стороны паренхимы печени отмечается постепенное повышение общей эхогенности с присутствием достаточно выраженной мелкоочаговой и даже крупноочаговой неоднородности паренхимы. Сосудистый рисунок при этом становится несколько обедненным — за счет нечеткой визуализации мелких ветвей.
При регрессии воспалительного процесса эхографическая картина приближается к норме, хотя достаточно часто остается или появляется несколько повышенная эхогенность паренхимы, часто сохраняется увеличение размеров печени — большей частью также за счет правой доли. В ряде случаев может сохраняться умеренно выраженная мелкоочаговая неоднородность паренхимы. Нередко острый гепатит становится причиной воспалительных изменений лимфатических узлов в области ворот печени.
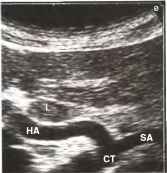
Рис. 42. Солитарный гипоэхогенный лимфатический узел (L) в области ворот печени при инфекционном гепатите НА - печеночная артерия, SA - селезеночная артерия, СТ - чревный ствол.
Помимо изменения качественного отображения сосудистого рисунка, важным дифференциально-диагностическим признаком является отсутствие деформации, дислокации и прочих вариантов изменения структурности и строения сосудистого рисунка. При значительной выраженности воспалительного процесса и. соответственно, значительном отеке паренхимы печени эхогенность последней снижается в большей степени (“темная печень”). Звукопроводимость печени при этом повышается. При наличии в клинической картине заболевания желтухи важным дифференциально-диагностическим признаком печеночного генеза гипербилирубинемии является отсутствие расширения внутрипеченочных и внепеченочных желчевыводящих протоков. При этом следует помнить о том, что расширение протоковой системы печени при подпеченочном блоке наступает не мгновенно, а спустя некоторый период времени. Этот период зависит от степени и выраженности обструкции. Кроме того, на разных типах ультразвуковых приборов сроки выявления расширенных внутрипеченочных протоков весьма различаются. Так, на портативных приборах, обладающих не очень высокой разрешающей способностью, возможность идентифицировать такие мелкие трубчатые структуры, как расширенные желчевыводящие протоки, появляется к концу третьих — началу четвертых суток после появления признаков желтухи. На приборах высшего класса, обладающих к тому же возможностью проведения исследования в режимах импульсной и цветовой допплеровских методик, такая возможность имеется уже к концу первых — началу вторых суток после появления клинико-лабораторных признаков желтухи. Помимо визуализации протоков в В-режиме, благодаря высокой разрешающей способности имеется возможность подтвердить отсутствие кровотока, как методом спектрального анализа, так и методом цветового исследования (что несколько проще и экономнее по времени). В дифференциальной диагностике данной патологии важным моментом является не только выявление признаков диффузных изменений паренхимы печени и степени их выраженности, но и уверенность исследователя в том, что неоднородность паренхимы не связана с множественным мелкоочаговым солидным или солидно-кистозным поражением печени. Важным дифференциально-диагностическим критерием является сопоставление эхографической картины с клинико-лабораторными показателями и их соответствие острому воспалительному процессу.
При заражении вирусами B, C и D высока вероятность развития хронической инфекции, при которой вирус продолжает размножаться в течение многих лет и вызывает прогрессирующее поражение печени. Важно знать, что после заражения вирусами гепатита B или C явные симптомы острого гепатита могут не наблюдаться. Острый гепатит в большинстве случаев протекает без желтухи. При так называемых желтушных формах острого гепатита желтуха может быть очень незначительной (небольшая желтизна белков глаз, потемнение мочи) и пройти незамеченной.
При хроническом гепатите изменения ультразвуковой картины печени во многом зависят от стадии, продолжительности и тяжести заболевания. При легкой степени и в начальной стадии заболевания эхографически существенные изменений могут не фиксироваться. При этом во многих случаях бывает трудно предполагать даже наличие каких-либо изменений со стороны эхографической картины, особенно на приборах портативного класса, а зачастую и на аппаратах среднего класса. Максимальные отклонения, которые могут быть выявлены при ультразвуковом исследовании в это время, обычно заключаются в несколько увеличенных размерах печени, незначительном повышении ее эхогенности, более, чем обычно, выраженной зернистости или иногда незначительно выраженной мелкоочаговой неоднородности паренхимы. Существенных изменений со стороны печеночных вен и воротной вены не наблюдается. Из изложенного видно, что ранняя диагностика хронического гепатита и его форм с неярко выраженными морфологическими изменениями по данным ультразвукового метода исследования представляет весьма сложную и в настоящее время трудно решаемую проблему, требующую высокоразрешающего диагностического оборудования. Однако в дальнейшем, при прогрессировании заболевания, либо при исследовании пациента с умеренной или тяжелой формой этой патологии может быть отмечена разнообразная эхографическая картина.
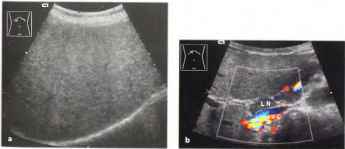
Рис. 43. а, b Хронический гепатит С, легкая форма, а крайне незначительное огрубление эхо-структуры печени и повышение ее ультразвуковой плотности, легкая акустическая тень. Снимок в правой межреберной плоскости, b ЦДЭ: воспалительная лимфаденопатия ворот печени (LN). Снимок в правой межреберной плоскости в проекции ворот печени. VC - полая вена.
Достаточно часто при хроническом гепатите встречается увеличение размеров печени не только за счет правых, но и левых отделов. При этом часто отмечается увеличение всех измеряемых размеров — косого вертикального размера и толщины правой доли, кранио-каудального размера и толщины левой доли, причем в разных случаях может превалировать как увеличение вертикальных, так и передне-задних показателей. Толщина хвостатой доли изменяется редко. Изменения формы печени обычно находятся в пределах ее анатомической конфигурации. Контуры печени остаются ровными и четко видимыми, хотя капсула может дифференцироваться менее отчетливо, чем в норме. Выявляется закругление нижнего края, угол его при этом увеличивается. Контуры печени длительное время остаются ровными. Их неровность начинает проявляться только в фазе перехода в цирроз печени. Контур диафрагмы в большинстве случаев визуализируется отчетливо, однако, иногда может отмечаться “истончение" — худшая визуализация контура диафрагмы за счет повышения затухания ультразвука в ткани печени. В зависимости от длительности заболевания и тяжести морфологических повреждений эхогенность паренхимы печени может колебаться в диапазоне от умеренно до значительно повышенной.
Повышение эхогенности паренхимы печени может быть достаточно равномерным (при небольшой степени выраженности изменений) или неравномерным — отдельными участками, “полями" — с чередованием с изоэхогенными участками неизмененной паренхимы. С нарастанием морфологических изменений в ткани печени усиливается и изменение ее эхографической картины. В структуре паренхимы печени отмечается появление участков неоднородности небольшого размера, обычно до 0,5-1 см, как правило, высокой эхогенности, занимающих в сумме большие площади среза паренхимы. При обострении процесса часто можно отметить усиление неоднородности структуры и изменение характера эхогенности из-за появляющегося отека паренхимы в виде гипоэхогенных участков, рассеянных по площади среза.
Рис.44. Тяжелый хронический лекарственный токсический гепатит с фиброзом: плотная, зернистая гипоэхогенная структура с отсутствием видимых сосудов и выраженной акустической тенью (та же картина, что и при хроническом токсическом алкогольном гепатите со структурной трансформацией).
Достаточно важным признаком неоднородности структуры печени при хроническом гепатите, в отличие от цирроза печени, является неотчетливость контуров участков неоднородности. Изменения сосудистого рисунка печени сводятся, главным образом, к постепенно прогрессирующему его обеднению, то есть последовательному ухудшению визуализации в первую очередь мелких периферических ветвей печеночных вен и во вторую очередь — мелких ветвей воротной вены, хотя в то же время часто может наблюдаться усиление отражения от перипортальных структур. Данные изменения обусловлены повышением эхогенности и появлением неоднородности паренхимы, на фоне которых мелкие сосуды теряются и не дифференцируются в В-режиме.
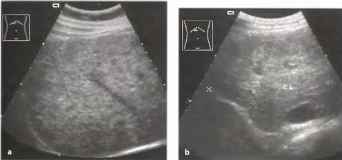
Рис. 45.а, b Выраженный хронический вирусный гепатит, цирроз печени, а Тяжелый хронический гепатит В: пятнистая структурная трансформация, размытые очертания печеночных вен. b Стадия В (по Чайлду) цирроза печени при гепатите С: грубоэхогенные участки фиброза с массивным увеличением хвостатой доли (CL). CL:RL (правая доля печени) - 74:43 мм (курсоры; в норме соотношение составляет <0,55).
Определенную помощь в выявлении этих сосудов дает применение цветовых допплеровских методик. Тем не менее, в некоторых случаях может наблюдаться улучшение визуализации ветвей воротной вены — тогда, когда процесс приводит к изменениям в портальных и перипортальных зонах. В этом случае стенки ветвей воротной вены могут выглядеть несколько более эхогенными и утолщенными. Магистральные печеночные вены визуализируются несколько менее отчетливо, но без серьезных изменений параметров. Основной ствол воротной вены не расширен, существенных нарушений по скоростям и объемному кровотоку в воротной вене не отмечается. При наличии в клинической картине заболевания желтухи важным дифференциально-диагностическим признаком печеночного генеза гипербилирубинемии является отсутствие расширения внутрипеченочных и внепеченочных желчевыводящих протоков. Из других параметров отмечается снижение звукопроводимости органа, обусловленное повышенным поглощением и рассеиванием энергии ультразвукового луча в измененной ткани печени, в отличие от острого гепатита, где улучшение звукопроводимости печени связано с наличием отека паренхимы.
Важными вопросами дифференциальной диагностики хронического гепатита, так же, как и острого гепатита, является не только выявление признаков диффузных изменений паренхимы печени и степени их выраженности, но и уверенность исследователя в том, что неоднородность паренхимы не связана с множественным мелкоочаговым солидным или солидно-кистозным поражением печени. Значимым дифференциально-диагностическим критерием является сопоставление эхографической картины с клинико-лабораторными показателями.
Таким образом хронический вирусный гепатит характеризуется различными изменениями зхогенности и контуров, от минимальных, когда печень имеет нормальный вид (легкий или «персистентный» гепатит с низкой активностью), до изменений, характерных для ранней формы цирроза печени (тяжелый или «агрессивный» гепатит с высокой активностью).
При хроническом гепатите часто выявляются следующие ультразвуковые данные:
· Некоторая грубость эхоструктуры печени.
· При хроническом токсическом гепатите имеется акустическая тень.
· Часто спленомегалия.
· Неравномерность диаметра печеночных вен.
· Появление дольчатости и зернистости контуров печени.
· Прогрессирующее увеличение диаметра воротной вены:
·
· Считается, что эхо-структура и характер контуров печени зависят от протяженности изменений, степени фиброзной трансформации и этиологии цирроза. Вид сосудов ворот печени, присутствие асцита и размеры селезенки определяются тяжестью портальной гипертензии и активностью воспалительного процесса.
Как было сказано выше, степень выраженности изменений эхографической картины зависит от степени повреждения печеночной ткани, однако в настоящее время еще не найдено четкой корреляционной связи между этиологией и морфологической формой хронического гепатита с одной стороны и изменениями эхографической картины с другой стороны.
Воспалительные кисты (абсцессы) печени.
Среди анэхогенных поражений печени принято выделять: непаразитарные и паразитарные кисты печени, концентрическое расширение желчных протоков (синдром Кароли), распад метастатического поражения и абсцесс печени.
Инфекционные абсцессы могут возникать после травм печени, хирургических вмешательств, при холангите, сепсисе, флебите портальной вены. При допплеровском ультразвуковом исследовании видна повышенная васкуляризация капсулы, отсутствие сигнала от кровотока внутри полости абсцесса. При УЗИ абсцесс печени проявляется как округлая структура с плотной, неровной капсулой, имеющая толстые стенки и неровную внутреннюю поверхность. Внутри лоцируется плотное жидкое содержимое, возможно наличие газа. Для амебных абсцессов характерна толстая капсула с множественным внутренними перегородками, отсутствие скоплений газа в абсцессе, нередки множественные поражения.
В эхографической картине абсцесса печени имеется ряд особенностей, связанных со временем его существования. Так, в фазе формирования, при наличии соответствующих клинико-лабораторных данных, в паренхиме печени можно выявить зону пониженной эхогенности с неоднородной структурой и нечеткими, переходящими в нормальную ткань, контурами. В центральной части этой зоны пониженной эхогенности обычно выявляется анэхогенный, практически бесструктурный участок. Впоследствии, при параллельном нарастании клинических проявлений, формируется жидкостьсодержащая эхонегативная полость с внутренним эхогенным содержимым, обусловленным наличием гноя и тканевого детрита.
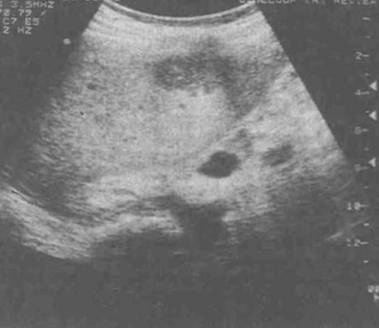
Рис. 46. Сонографическая картина абсцесса печени: на границе правой и левой долей определяется патологическое образование неоднородной структуры с нечёткими контурами размером 5х2,5 см.
При абсцессах печени выявляются характерные для жидкостной структуры эхографические признаки :эффект усиления задней стенки, эффект боковых акустических теней, эффект дистального псевдоусиления эхосигнала. Кроме того отмечается формирование четкого отграничения полости абсцесса от окружающей паренхимы печени в виде несколько неоднородного ободка повышенной эхогенности различной толщины — от 0,5-1 мм до 10-15 мм. являющегося пиогенной оболочкой.
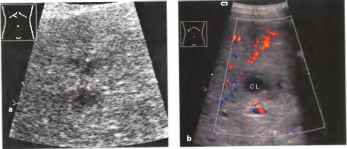
Рис. 47. а. Абсцесс печени, возникший в результате септического холангита: образование с нечеткими границами (стрелки), b Абсцесс печени, возникший в результате инфицирования через желчные пути: неоднородное образование с нечеткими границами, слегка эхогенным контуром и разжижением в центре (CL). При ЦДЭ сосуды в области образования не обнаруживаются.
Часто выявляется сепарация содержимого полости абсцесса с образованием границы "жидкость-жидкость" с горизонтальным уровнем, где более густая эхогенная часть находится внизу, а более жидкая эхонегативная — вверх. При этом отмечается перемещение всего внутреннего содержимого при изменении положения тела пациента .В случае появления пузырьков газа в полости абсцесса (вследствие анаэробного воспалительного процесса) при сонографии выявляются гиперэхогенные объемные структуры, занимающие положение у верхней стенки и дающие конусообразный эффект реверберации с образным названием 'хвост кометы";
Рис. 48 Артефакт хвост кометы
Некоторые отличия может иметь эхографическая картина паразитарного абсцесса при амебиазе, который преимущественно распространен в Азии. Южной Америке и Африке. Ввиду несколько иного варианта развития абсцесса в печени обычно при попадании амеб развивается воспалительная инфильтрация с последующим формированием очагов некроза. В дальнейшем возможно слияние некротических очагов в один или несколько абсцессов. В эхографической картине соответственно может наблюдаться появление вначале умеренной, а затем и выраженной диффузно-очаговой неоднородности паренхимы со смешанной и преимущественно пониженной эхогенностью. Затем на этом фоне формируются эхонегативные участки неправильной формы и различных размеров с неровными и нечеткими контурами. В дальнейшем, они образуют одну или несколько полостей, практически аналогичных по акустическим признакам бактериальным абсцессам, но, тем не менее, с рядом отличий: контуры обычно неровные с "карманами", эхогенная оболочка вокруг абсцесса выражена неотчетливо, в полости абсцесса может присутствовать более неоднородное содержимое, вплоть до наличия секвестров печеночной ткани и большого количества газа.
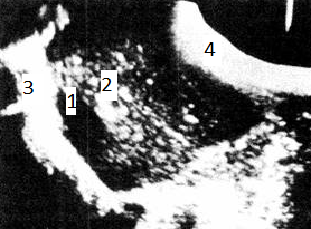
Рис. 49. При УЗИ виден амёбный абсцесс (1) печени (2), лежащий позади диафрагмы (3). Видна передняя брюшная стенка (4)
Существенной вспомогательной диагностической подсказкой служит выявление признаков относительно быстрого изменения эхографической картины в корреляции с проводимым лечением при динамическом исследовании.
В дифференциальной диагностике абсцессов печени особое внимание уделяется не только выявлению признаков локального изменения структуры и эхогенности паренхимы печени и степени их выраженности, но и получению убедительных данных в пользу того, что неоднородность паренхимы обусловлена наличием именно жидкостного (или жидкостных) образований имеющих четкую связь с клинико-лабораторными показателями и анамнезом, а также имеющих определенную динамику эхографической картины, коррелирующую с состоянием больного и проводимым лечением.
Наиболее распространённым паразитарным заболеванием печени является эхинококкоз.
Существуют два вида эхинококкоза, которые отличаются друг от друга по эпидемиологии, патогенезу и клиническим проявлениям. Гидатидный эхинококкоз вызывается внедрением в организм человека и последующим развитием в нем личиночной стадии червя Echinococcus granulosus. Возбудителем альвеолярного эхинококкоза является личинка ленточного червя Echinococcus multilocularis.
Согласно классификации изображений эхинококковых кист по ВОЗ (2003) принято выделять следующие типы поражения печени:
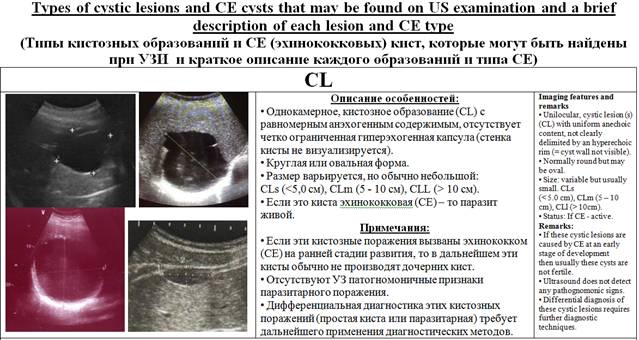
Критерии диагностики кисты являются:
• Сферическая форма.
• Эхонегативное содержимое.
• Ровные края.
• Дистальное акустическое усиление.
• Яркая задняя стенка.
• Краевое затенение вследствие критического угла отражения.
Таким образом, в общей картине эхинококкового поражения наблюдается объемное жидкость содержащее образование с хорошо очерченной капсулой в одной из долей печени — преимущественно правой. Образование существует длительный период времени и имеет тенденцию к постепенному, часто значительному, увеличению размеров и изменению своей эхографической структуры согласно переходу из одного приведенного в классификации типа в другой.
Дифференциальная диагностика эхинококкоза может быть затруднена, так как отличия от эхокартины других однокамерных жидкостьсодержащих образований, да и от ряда осложненных, травматических, малигнизированных кист и некоторых специфических поражений печени могут быть крайне незначительны. В этих случаях при подозрении на возможность паразитарного происхождения кисты рекомендуется проводить серологические тесты, обладающие весьма высокой специфичностью.
Альвеококковое поражение печени эхографически неотличимо от изо-, гипоэхогенных метастазов, особенно при небольших размерах. При больших размерах альвеококкового очага в нем может образовываться жидкостьсодержащая полость, дающая дистальное псевдоусиление эха.
Дифференциальная диагностика альвеококкоза сложна и требует проведения серологических тестов.
Цирроз и гепатоцеллюлярный рак
Кроме хронического алкоголизма возможными причинами цирроза печени могут быть вирусный гепатит, метаболические расстройства и токсические вещества окружающей среды. Латентные циррозы с печеночной декомпенсацией могут протекать без сонографически определяемых изменений, и в этом случае сонография не подходит для исключения заболевания. На более поздних стадиях возникают сонографические изменения, которые могут быть использованы как критерии цирроза печени.
Сложность диагностики и дифференциальной диагностики диффузных поражений печени заключается в практически полном отсутствии специфичных признаков, главным образом на ранних стадиях заболеваний — еще до появления таких, например, симптомов, как портальная гипертензия и т.п.
В то время как вдоль края нормальной печени имеется тонкая эхогенная капсула, цирротическая печень имеет неровную поверхность (мелкая волнистость и выпуклость), что вызывает повышенное рассеяние звука с утратой нормального отражения от капсулы. Это ведет к тому, что капсула не визуализируется или визуализируется частично. Отсутствие капсулярной линии лучше всего заметно, когда печень окружена асцитической жидкостью. В этом случае контур диафрагмы хорошо очерчен, в то время как при отсутствии асцита контур диафрагмы либо не визуализируется, либо имеет истонченный и фрагментированный вид. Форма печени претерпевает соответствующую изменению размеров трансформацию. Контуры печени постепенно становятся неровными, бугристыми — за счет рубцовых втяжений и участков регенерации в субкапсулярных зонах Нижний край обеих долей становится тупым (более 75° для правой и более 45° для левой доли).
Рис. 50. Алкогольный цирроз печени. Бугристая нижняя поверхность печени (^^^).
Структура паренхимы с нарастанием выраженности морфологических изменений становится диффузно неоднородной с множественными участками повышенной (паренхиматозные очаги фиброза, утолщенные стенки внутрипеченочных ветвей воротной вены, участки фиброза в перипортальных зонах и вокруг желчевыводящих протоков) и средней или пониженной эхогенности (очаги регенерации и островки нормальной ткани).
Кроме того, периферическая сосудистая сеть при циррозе становится разреженной, оставшиеся сосуды имеют различный диаметр и увеличенный угол слияния (> 45°). Нормальные печеночные вены (10) имеют прямой ход, соединяются друг с другом под острым углом и видны на периферии печени. При циррозе ветви воротной вены вблизи ворот имеют утолщенную яркую стенку и резкие изменения диаметра («обрезанное портальное дерево»). Возможна также некоторая деформация средних по размеру стволов печеночных вен. В области ворот печени могут наблюдаться зоны значительно повышенной эхогенности, обусловленные развитием массивных фиброзных изменений.
Рис.51. Сужение и колебания просвета (>) печеночных вен при циррозе печени.
Регенераторные узлы имеют нормальную эхогенность и распознаются только косвенно по смешению расположенных рядом сосудов. Размеры участков неоднородности вариабельны — от 0,2 до 2 см и более, причем размер этих участков неоднородности (мелкие или крупные) не всегда коррелирует с морфологической формой цирроза (мелконодулярный, крупнонодулярный и т.п.). Наконец, деформированная и двояковыпуклая конфигурация печени, сниженная способность к деформации (выявляется при надавливании датчиком на печень) и увеличенная, закругленная левая и хвостатая доли свидетельствуют о циррозе печени. Размеры органа на ранних стадиях могут быть значительно увеличены — вначале правая доля, затем левая и хвостатая. Толщина последней может значительно превышать 3,5-4 см, что является признаком компенсаторной гипертрофии. Затем, при прогрессировании заболевания, в результате гибели печеночных клеток и развития на их месте соединительной ткани размеры долей, в первую очередь правой, уменьшаются.
Диагностическими критериями цирроза печени являются:
• Отсутствие тонкой гиперэхогенной линии капсулы.
• Малое количество периферических печеночных сосудов.
• Тупой угол соединения печеночных вен (> 45°).
• Гиперхогенная стенка воротной вены.
• Резкие изменения диаметра ветвей воротной вены.
• Регенераторные узлы со смещением рядом расположенных сосудов.
• Бугристый контур печени (только в поздних стадиях).
• Сморщенная печень (только в поздних стадиях).
• Признаки/симптомы портальной гипертензии.
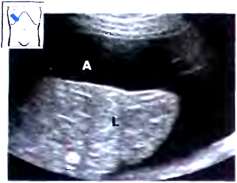
Рис. 52. Алкогольный цирроз печени. Эхогенность паренхимы повышена. Печень (L) уменьшена в размере и окружена асцитической жидкостью (А).
Осложнения цирроза печени включают портальную гипертензию и ее последствия, асцит (68) и гепато-целлюлярный рак, возникающий на поздних стадиях цирроза. Поэтому цирротическая печень должна быть самым тщательным образом обследована для выявления дополнительных патологических изменений. Только поздние стадии цирроза дают сморщивание печени. Гепатоцеллюлярный рак может быть изоэхогенным по отношению к оставшейся паренхиме печени и обнаруживаться только за счет изгиба и смещения прилегающих печеночных вен.
Возможность действенной количественной оценки степени изменения паренхимы печени, для разных пациентов в настоящее время отсутствует, что весьма осложняет дифференциальную диагностику и уточнение степени повреждения паренхимы по данным ультразвукового исследования. Данные, получаемые при эхографии, не позволяют также делать выводы о типе цирроза (портальный, билиарный. постнекротический или метаболический). При высокой чувствительности эхографии к выявлению тех или иных отклонений в структуре паренхимы печени специфичность метода остается недостаточной для уверенного установления инструментального диагноза в начальных фазах заболевания и при недостаточно ярко выраженных морфологических изменениях, особенно при отсутствии вторичных проявлений.
ЭХОГРАФИЧЕСКАЯ КАРТИНА ПЕЧЕНИ ПРИ ЗЛОКАЧЕСТВЕННЫХ ОЧАГОВЫХ ПОРАЖЕНИЯХ
Ультразвуковая диагностика первичных злокачественных опухолей печени
К первичным злокачественным новообразованиям печени, диагностируемым при ультразвуковом исследовании, относят холангиоцеллюлярный и гепатоцеллюлярный печени рак.
Холангиоцепллюлярный рак печени (холангиокарцинома) развивается из эпителия желчных протоков. В отличие от гепатоцеллюлярного рака, эхографическая картина при холангиоцеллюлярном раке печени не отличается разнообразием, да и сама по себе холангиокарцинома довольно редко. Особенности развития этого злокачественного поражения печени обуславливают и его ультразвуковое изображение.
Рис. 53.Первичная холангиоцеллюлярная карцинома (ХЦК) печени: образование с нечеткими границами.
Варианты эхографической картины включают в себя единичное узловое образование в одной из долей печени (I вариант) и множественное узловое поражение с локализацией в разных отделах печени (II вариант). Обобщенная эхографическая картина холангиокарциномы имеет ряд характерных признаков. Опухоль имеет вид объемного образования неправильной округлой формы с несколько неровными и нечеткими контурами. Структура образования может быть либо достаточно однородной, особенно на ранних этапах развития, либо умеренно диффузно неоднородной. Эхогенность чаще всего повышенная, иногда смешанная — с гипер- и изоэхогенными участками. Ввиду расположения опухоли в проекции желчевыводящего протока, клинические проявления в виде желтухи появляются очень рано, когда опухоль имеет еще небольшие геометрические размеры — до 1,5-2,5 см в диаметре. Раннее появление клинических проявлений при I варианте вызывается быстрой окклюзией желчевыводящего протока и, соответственно, его изолированным расширением, что четко дифференцируется как в В-режиме, так и при использовании допплеровских методик.
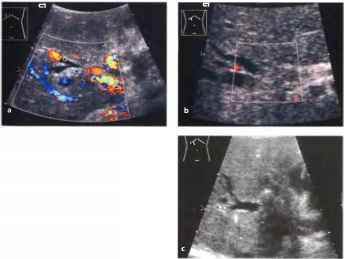
Рис. 54. Внутрипеченочный холестаз вследствие холангиоцеллюлярной карциномы,
При II варианте происходит такое же нарушение оттока желчи, но в нескольких протоках. Эхографическая картина I и II вариантов практически одинакова и различается лишь числом опухолевых узлов и их локализацией. В запущенных случаях при длительном существовании опухоли и больших ее размерах структура образования может иметь более выраженную неоднородность и смешанную эхогенность. Со стороны эхографической картины печени на ранних стадиях может отмечаться только наличие самого образования или нескольких образований, и расширение отдельных внутрипеченочных желчевыводящих протоков. Внепеченочные участки желчевыводящей системы обычно не изменяются. В поздних стадиях при несколько больших размерах образований может отмечаться увеличение размеров печени, иногда выбухание или неровность контуров и деформация сосудистого рисунка.
В дифференциальной диагностике первичного холангиоцеллюлярного рака печени особое внимание уделяется не только выявлению признаков наличия одного или нескольких объемных образований, но и получению убедительных данных в пользу того, что расширение внутрипеченочных желчевыводящих протоков связано с их окклюзией этим солидным образованием, а также дифференциации выявленных изменений от эхографической картины билиарной гипертензии иного генеза.
Ультразвуковая диагностика гепатоцеллюлярного рака печени
Гепатоцеллюлярный рак печени (гепатокарцинома. гепатома) развивается из гепатоцитов. Эхографическая картина гепатоцеллюлярного рака печени отличается разнообразием, которое обусловлено не только видом изображения, но и стадией развития заболевания. Так, на ранней стадии заболевания, когда опухоль имеет небольшие размеры — до 3-4 см в диаметре, ее может быть сложно, дифференцировать от ряда доброкачественных очаговых и псевдоочаговых поражений, а также от вторичных злокачественных поражений Ультразвуковая картина варьирует; имеет место типичная картина метастаза, когда опухоль обнаруживается в неизмененной ткани печени. Гипоэхогенное, изоэхогенное, гиперэхогенное или неоднородное образование с неровными контурами, располагающееся в толще паренхимы одной из долей печени. При циррозе печени солитарная или изолированная карцинома часто не имеет периферического ореола. На ранних стадиях, за исключением расположения опухоли в субкапсулярных областях и около крупных печеночных сосудов, изменения размеров, формы, контура и внутренней структуры печени могут не выявляться. При увеличении размеров опухоли более отчетливо дифференцируется как ее внутренняя структура, так нарушения со стороны строения печени. Часто выявляются дегенеративные изменения (кровоизлияние внутрь опухоли, отложения солей кальция). ЦДЭ: выраженная васкуляризация артериальными сосудами при отсутствии типичного хаотического сосудистого рисунка.
Рис.55.Первичная гепатоцеллюлярная карцинома: несколько слегка гипоэхогенных опухолевых образований (Т) в печени с алкогольным токсическим циррозом; асцит.
Для узловой формы первичного рака печени характерен достаточно выраженный полиморфизм, который заключается в разнообразии структуры, эхогенности и контуров образования, причем при дальнейшем росте образование может менять свою эхогенность.
Поверхностное (субкапсулярное) расположение встречается значительно реже, чем глубокое — в толще паренхимы. При небольших размерах образования существенного нарушения внутреннего строения печени обычно не наступает. При выявлении достаточно крупных образований (более 4-5 см в диаметре) можно отметить ряд признаков со стороны печени в целом. Ввиду наличия достаточно крупного образования форма доли печени и ее размеры могут изменяться. Контуры печени могут приобретать несвойственные им выбухания в местах расположения опухолевых узлов.
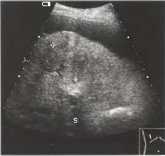
Рис. 56. Микрокальцинаты (стрелка) с акустической тенью (S) в первичной печеночно-клеточной карциноме, также определяется другая опухоль (курсоры).
В дифференциальной диагностике первичного гепатоцеллюлярного рака печени особое внимание уделяется не только выявлению признаков локального изменения структуры и эхогенности паренхимы печени и степени их выраженности, но и получению убедительных данных в пользу того, что нарушение структуры паренхимы связано с солидным злокачественным поражением печени, а также дифференциации выявленных изменений от эхографической картины при некоторых доброкачественных очаговых и диффузных поражениях печени. При наличии гипербилирубинемии и портальной гипертензии требуется более пристальное внимание к мельчайшим эхографическим признакам. Дифференциальную диагностику первичного рака печени осложняет также относительно частое его возникновение на фоне цирроза печени или других диффузных поражений. Необходимо отметить, что во многих случаях установить окончательный диагноз возможно только при использовании пункционной биопсии под визуальным, в частности, эхографическим контролем
Метастазы в печень
Нередко достаточно сложную проблему для исследователя создают очаговые изменения и паренхиме печени. Некоторые из них без особых затруднений верифицируются по ультразвуковым особенностям, диагностика других требует проведения детального анализа с привлечением иных методов обследования.
В группе злокачественных поражений печени по частоте встречаемости метастатическое поражение стоит на первом месте. Наиболее частыми источниками метастазов в печень являются злокачественные опухоли толстой кишки, прямой кишки, поджелудочной и молочных желез, реже — желудка, легких, мягких тканей и системы кроветворения. Метастатическое поражение печени отличается ярко выраженным разнообразием эхографической картины, что связано с полиморфностью изображения метастазов и значительным динамическим изменением эхокартины.
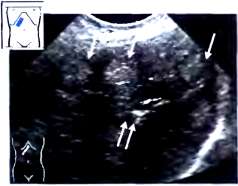
Рис.57. Диффузное поражение печени метастазами. Крайне неоднородная картина. В неоднородной паренхиме видны гипоэхогенные зоны (v) и кальцификаты (^^).
Метастазы опухолей в ткань печени могут быть как гипоэхогенными, так и гиперэхогенными, или иметь эхогенность, равную эхогенности ее паренхимы. Метастазы, особенно небольших размеров, могут обладать относительно однородной структурой, однако типичной является форма кокарды с гипоэхогенным ободком.
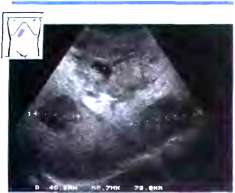
Рис.58. Метастазы в печень. Округлые гипоэхогенные неоднородные метастазы.
Метастазы в печени могут возникать от первичной опухоли не только желудочно-кишечного тракта, но также легких и молочной железы. Сонографические проявления метастазов полиморфны. Метастазы в печень колоректального рака обычно эхогенные, вероятно связанные с васкуляризацией опухоли вследствие относительно медленного ее роста. Более быстро растущие метастазы бронхогенного рака или рака молочной железы состоят почти исключительно из опухолевых клеток и чаще гипоэхогенные. Из-за разнообразных проявлений метастазы нельзя достоверно отнести к какой-либо определенной первичной опухоли
Рис. 59. Meтастазы рака толстой кишки в печень. Округлые гипоэхогенные метастазы, некоторые окружены ободком.
Выявление метастазов зависит от размеров, эхогенности и локализации первичной опухоли. УЗИ позволяет с точностью более 80% выявлять метастазы, размеры которых составляют немногим менее 1 см.
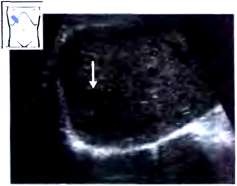
Рис. 60. Метастазы злокачественной опухоли толстой кишки в печень (v). Кокардоформный метастаз с широким гипоэхогенным ободком.
В дифференциальной диагностике метастатического рака печени особое внимание уделяется не только выявлению признаков локального изменения структуры и эхогенности паренхимы печени и степени их выраженности, но и получению убедительных данных в пользу того, что нарушение структуры паренхимы связано с солидным или кистозно-солидным злокачественным поражением печени, а также дифференциации выявленных изменений от эхографической картины при некоторых доброкачественных очаговых и диффузных поражениях печени.
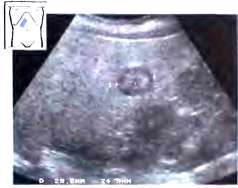
Рис. 61. Метастазы почечно-клеточного рака в печень. Кокардоформные метастазы с узким гипоэхогенным ободком.
Дифференциально-диагностический ряд включает в себя — диффузные поражения печени (цирроз и фиброз печени, хронический гепатит, реже жировая инфильтрация печени), доброкачественные очаговые поражения (кавернозные гемангиомы, очаговая узловая гиперплазия печени, аденома, организованные гематомы), первичные злокачественные поражения (гепатома), специфические поражения печени (туберкуломы, саркоидоз), вторичные диффузные поражения печени, нагноившиеся и малигнизированные солитарные кисты, множественные кисты печени, некротизированные первичные опухоли печени, абсцессы печени, гематомы, бипомы и серомы, кавернозные гемангиомы, эхинококкоз.
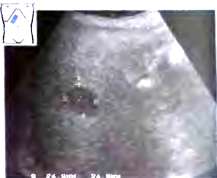
Рис. 62. Метастазы почечно-клеточного рака в печень.
Изоэхогенные метастазы часто становятся сложной дифференциально-диагностической проблемой. Они могут обнаруживаться лишь по наличию гипоэхогенного контура, по смещению соседних структур или инфильтрации. Использование ТГВ, ЦДЭ или эхоконтрастных препаратов позволяет добиться лучшей визуализации. Изоэхогенные образования, обнаруживаемые только по гипоэхогенному контуру. Возможно смещение соседних структур или инфильтрация.

Рис. 63. Изоэхогенные метастазы в печень (М) из карциномы поджелудочной железы. Образования отграничиваются от нормальной ткани печени лишь гипоэхогенной полоской (это является причиной того, что в определенной доле случаев подобные метастазы не видны при УЗИ, однако обнаруживаются при использовании других методов диагностики). При ЦДЭ сосуды в метастазах не обнаруживаются.
При наличии гипербилирубинемии и портальной гипертензии также требуется пристальное внимание к различным эхографическим признакам. Дифференциальную диагностику метастатического рака печени осложняет не только выраженная полиморфность поражения и возможность комбинации различных эхографических типов метастазов у одного пациента, но и относительно частое его возникновение на фоне других диффузных или очаговых поражений печени.
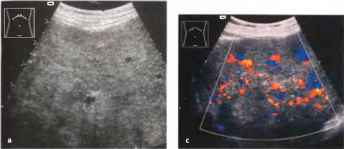
Рис.64 а, b Метастазы в печень у пациента с колоректальном карциномой. В-режим: гетерогенная эхо-структура паренхимы печени с отсутствием четких метастазов. b ЦДЭ: нормальный сосудистый рисунок не определяется. Отдельные беспорядочно
Необходимо отметить, что в подавляющем большинстве случаев невозможно эхографически дифференцировать первичность или вторичность поражения при единичных узлах. Во многих случаях установить окончательный диагноз возможно только при использовании пункционной биопсии под визуальным, в частности, эхографическим контролем.




