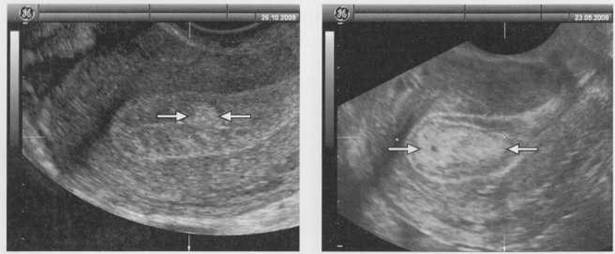
Ультразвуковые исследования в гинекологии и акушерстве
Ультразвуковые исследования в гинекологии и акушерстве
Нормальная эхограмма органов женской половой сферы
Необходимым условием успешного сонографического исследования является знание синтопии органов малого таза. Матка располагается кзади и кверху от мочевого пузыря. На сагиттальном срезе в переднезаднем направлении определяются следующие структуры: лонное сочленение (звуковая волна не проходит через кость, поэтому датчик следует располагать над симфизом), мочевой пузырь, матка и прямая кишка.
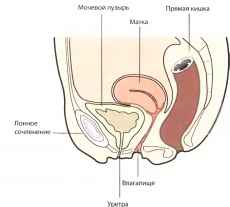
Рис. 1 Взаиморасположение органов нижнего этажа брюшной полости у женщин.
Матка представляет собой полый гладкомышечный орган уплощенной грушевидной формы.
Матка состоит из шейки и тела. Границей между шейкой и телом матки является область внутреннего зева. Различают переднюю, заднюю стенки и дно тела матки. Толщина передней и задней стенок примерно одинакова. Выделяют правый и левый маточные углы, завершающие дно матки и переходящие в маточные трубы. Миометрий состоит из трех слоев гладкомышечных и эластических волокон, между которым располагается рыхлая соединительная ткань, кровеносные и лимфатические сосуды и нервы. Расположение мышечных слоев идет в различных плоскостях, что позволяет многократно увеличивать размеры матки при вынашивании беременности. Наибольшую массу занимает средний слой, волокна которого расположены преимущественно в круговом направлении, а в тонких наружном и внутреннем слоях волокна идут в продольном направлении Снаружи матка покрыта плотной серозной оболочной, внутри имеет полость во фронтальной плоскости в форме треугольника, выстланную слизистой оболочкой (эндометрий), претерпевающей циклические изменения у женщин репродуктивного возраста. Передняя и задняя стенки матки примыкают друг к другу, в связи с чем в сагиттальном сечении полость имеет щелевидную форму. Область перехода полости матки в цервикальный канал называется внутренним зевом и является наиболее узким местом, а вся эта зона обозначается как перешеек.
Матка - наиболее легко определяемый орган малого таза. На сагиттальных эхограммах она выявляется как образование характерной грушевидной формы, расположенное в непосредственной близости позади мочевого пузыря. Неизмененный миометрий имеет в целом однородную мелкоячеистую структуру средней эхогенности. На при борах с высокой разрешающей способностью можно различить 3 слоя миометрия: внутренний (субэндометриальный) в виде тонкой гипоэхогенной полоски вокруг М-эхо; средний - основной, составляющий большую часть матки, имеющий среднюю эхогенность, и наружный, отделенный от среднего зоной сосудистых сплетений, имеющих вид ан- и гипоэхогенных включений. Обязательными при проведении эхографии матки являются: оценка положения, формы тела и шейки матки, размеров (три линейных размера), анализ эхоструктуры миометрия, эндометрия (послойно), полости матки, шейки матки, цервикального канала, эндоцервикса. Выявление патологических процессов в матке должно сопровождаться фиксацией изменений строения миометрия, обычно имеющих диффузный или очаговый характер. При описании этих процессов используются обычные термины - эхонегативный и эхопозитивный. В последнем случае гипо-, изо- или гиперэхогенность структуры определяется путем визуального сравнения эхогенностью неизмененного миометрия матки, выступающего в качестве своеобразного эталона. При обнаружении в малом тазу новообразований используется стандартизованный алгоритм их описания, учитывающий их локализацию, подвижность, определение трехлинейных размеров с последующим расчетом объема, форму, контур, особенности строения и толщины стенок, звукопроводимость, внутреннюю эхоструктуру. Дополнительную диагностическую информацию получают в ходе допплерометрии.
При проведении ультразвукового исследования органов малого таза у женщин обычно изучают тело матки, эндометрий, шейку матки, яичники, позадиматочное пространство и мочевой пузырь. Дополнительно может потребоваться исследование сосудов малого таза, лимфатических узлов и обзорное сканирование органов брюшной полости и забрюшинного пространства. При использовании эхографии с контрастированием (эхогистероскопия) становится возможным детальная оценка полости матки и оценка проходимости маточных труб.
Исследование всегда следует начинать с трансабдоминальной эхографии (ТА) по общепринятой методике при наполненном мочевом пузыре для определения топографии органов малого таза, определения размеров и строения выявленных патологических объемных образований и при необходимости оценки состояния органов брюшной полости и забрюшинного пространства. Оптимальным считается такое наполнение мочевого пузыря, когда он перекрывает дно тела не увеличенной матки. Исследование осуществляется путем анализа серии продольных, поперечных, а также косых сечений.
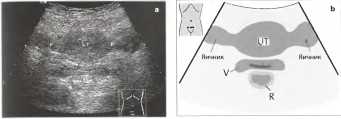
Рис. 2. а, b Снимок женских половых органов в нижней поперечной плоскости брюшной полости. UT - матка, V- шейка матки и влагалище, R - прямая кишка, Р - параметрий.
К преимуществам ТА исследования, бесспорно, относится возможность проведения для всех категорий пациентов (включая детей), полное отсутствие инвазивности, «панорамный» обзор всей полости малого таза, оценка мочевого пузыря и возможность использования стандартных конвексных датчиков. Недостатки метода связаны с необходимостью наполнения мочевого пузыря значительным объемом жидкости, что приводит некоторому изменению ультразвуковой анатомии исследуемых органов - «сплющиванию», оттеснению за пределы фокусной зоны датчика, что в свою очередь может вызывать ухудшение визуализации. Кроме того, на качество изображения при ТА эхографии большое влияние оказывают толщина передней брюшной стенки, перистальтика кишечника и наличие спаечного процесса. С целью нивелирования некоторых из указанных факторов рекомендуется подготовка пациенток к исследованию путем 2-3-дневной диеты с исключением газообразующих продуктов и приема препаратов, уменьшающих проявления метеоризма.
Этапы проведения ТА исследования
Датчик ставится вдоль белой линии живота в его нижних отделах. Получают изображение матки и шейки в сагиттальной плоскости, располагая датчик таким образом, чтобы метка трансдьюсера была ориентирована вверх, а метка направления сканирования на экране находилась сверху и слева. При такой установке матка располагается в левой части экрана, а шейка - в правой.
Проводят оценку состояния миометрия, эндометрия, полости и шейки матки, эндоцервикса. Измеряют длину и переднезадний размер тела матки, толщину удвоенного слоя эндометрия; при необходимости проводят аналогичные измерения шейки матки и эндоцервикса. Также осуществляется оценка позадиматочного пространства
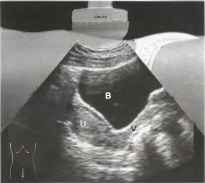
Рис. 3. В направлении спереди назад определяются: передняя стенка брюшной полости, мочевой пузырь (В) и матка (U), сверху которой определяется дно матки, а снизу - влагалище (V).
Затем поворачивают датчик на 90° меткой против часовой стрелки, осматривают и измеряют матку в поперечной плоскости на уровне
трубных углов, сбоку от матки получают изображения придатковых зон с обеих сторон. Несколько поворачивая датчик и изменяя угол сканирования получают сбоку от матки изображение яичников. В качестве ориентира используют подвздошные сосуды.
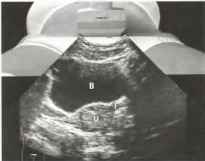
Рис. 4. Следующие структуры определяются в направлении спереди назад: передняя стенка брюшной полости, мочевой пузырь (В) и матка (U), по бокам от которой располагаются маточные трубы (Т).
Яичники осматривают и измеряют поочередно с каждой стороны. При необходимости для проведения дифференциальной диагностики и уточнения состояния изучаемых структур применяют цветовое допплеровское картирование и импульсную допплерографию.
Расположение матки в малом тазу определяется по углу между телом матки и шейкой. Если дно матки отклонено кпереди и образует тупой угол с шейкой, открытый в сторону мочевого пузыря, то положение матки называется anteflexio.
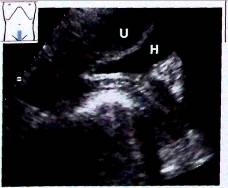
Рис. 5. Выраженный загиб матки кпереди (продольное сечение): U - матка, Н - мочевой пузырь;
Если дно матки отклонено кзади и образует тупой угол с шейкой, открытый в сторону крестца, то положение матки называется retroflexio.
Размеры матки значительно отличаются в зависимости от возраста пациентки, анамнеза и используемого при ультразвуковом исследовании доступа.
Измерение длины и толщины матки осуществляется при ее продольном сканировании. При этом длина измеряется от наиболее удаленной точки дна тела матки до проекции внутреннего зева, расположенного в области угла между телом и шейкой. Измерение переднезаднего размера (толщины) проводится в средней части тела между наиболее удаленными точками задней и передней стенок. В этой же плоскости аналогично осуществляется измерение удвоенного слоя эндометрия, нередко называемого М-эхо матки. Ширина матки измеряется на поперечных эхограммах на уровне трубных углов. Это сечение перпендикулярно тому, при котором производится измерение толщины.
При проведении трансабдоминального сканирования эндометрий может в ряде случаев не определяться, например, у девочек или в раннюю пролиферативную фазу, а также у женщин с длительной продолжительностью постменопаузального периода.
Измерение толщины М-эхо следует проводить при продольном сканировании матки с одновременной визуализацией цервикального канала. Измерение толщины М-эхо следует проводить при продольном сканировании матки с одновременной визуализацией цервикального канала. За толщину принимается максимальное значение переднезаднего размера М-эхо. Измерение необходимо осуществлять по наружным контурам М-эхо перпендикулярно продольной оси матки, не включая в измерение ободок сниженной эхогенности, который обычно появляется по периферии. Толщина эндометрия зависит от фазы менструального цикла. Различают несколько фаз менструального цикла, находящих свое отражение при эхографическом исследовании эндометрия. Сразу после окончания менструации эндометрий представляется в виде тонкой эхогенной линии. Первая фаза цикла, включающая в себя подфазы десквамации, регенерации и пролиферации, длится 12-17 дней. В фазу десквамации слизистая матки представлена неоднородной структуры срединным комплексом с включениями повышенной и сниженной эхогенности. В фазу регенерации и ранней пролиферации эндометрий представлен полоской однородной эхоструктуры сниженной эхогенности толщиной 2-4 мм. Далее по мере увеличения толщины эндометрия на фоне его сниженной эхогенности появляется повышенной эхогенности тонкая
полоска на границе эндометрия и миометрия и гиперэхогенная линия
смыкания переднего и заднего слоев эндометрия. На практике часто используется термин «периовуляторный эндометрий». Этот термин относится к описанию слизистой в конце пролиферативной и в начале секреторной фаз и характеризуется неравномерным повышением эхогенности трехслойного эндометрия, начинающимся с базальной зоны
В момент овуляции эндометрий отделен от миометрия эхогенным кольцом. Секреторная фаза начинается с момента овуляции и длится до начала менструации. В эту фазу происходит постепенное повышение эхогенности эндометрия, исчезает трехслойность, появляется тонкая гипоэхогенная полоска миометрия, прилежащего к базальному слою. К концу секреторной фазы в структуре слизистой иногда появляются мелкие ан- и гипоэхогенные включения, представляющие собой расширенные протоки желез. После овуляции срединное эхо постепенно исчезает в претерпевающем секреторные изменения эндометрии, пока не останется только эхогенный слой эндометрия.
Нормальный миометрий является гомогенной гипоэхогенной структурой. Он может пересекаться анэхогенными кровеносными сосудами. Нормальная структура миометрия во всех возрастных группах характеризуется однородностью и низкой или средней эхогенностью. В ряде случаев в толще стенки матки между средним (циркулярным) и наружным слоями миометрия можно визуализировать небольшие (от 1 до 2 мм в диаметре) сосуды. У пациенток старшей возрастной группы в этой области нередко обнаруживаются кальцинаты в аркуатных артериях. Внутренний слой миометрия имеет небольшую толщину и низкую эхогенность. При МРТ данная область вокруг полости матки носит название «соединительной зоны». Средний слой миометрия является самым толстым, и его гладкие мышечные волокна ориентированы циркулярно. Изменения взаиморасположения мышечных пучков миометрия друг относительно друга могут обусловливать неоднородность эхогенности отдельных областей миометрия, что также может наблюдаться при его локальных сокращениях. Важно дифференцировать такие физиологические особенности от формирующихся миоматозных узлов.
Эхогенность тела и шейки матки одинакова. В постменопаузальном возрасте толщина эндометрия не должна превышать 15 мм, а в постменопаузальном возрасте8 мм, если пациентка не получает гормонозаместительной терапии. С окончанием репродуктивного периода прекращается циклическая выработка половых гормонов, происходит уменьшение толщины эндометрия. Эхоструктура эндометрия в этот период характеризуется повышенной эхогенностью, однородностью, четкостью базального слоя. В постменопаузе у некоторых пациенток наблюдается скопление незначительного количества серозной жидкости в полости матки, называемое серозометрой, что может быть связано с частичной окклюзией цервикального канала. При этом следует обращать внимание на четкость и ровность контуров полости матки, анэхогенность содержимого, однородность и равномерность толщины эндометрия. Измерение толщины эндометрия должно проводиться на продольном сечении матки, когда направление ультразвукового пучка строго перпендикулярно продольной оси полости органа. Другие плоскости являются косыми, поэтому показатель толщины окажется завышенным.
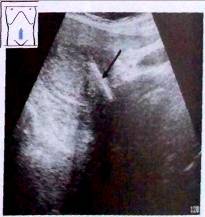
Рис.6. Внутриматочная спираль (v).
Ультразвуковое исследование позволяет легко обнаруживать внутриматочные средства (ВМС). Они дают сильное отражение, образуя позади себя акустическую тень, и располагаются в полости матки вблизи дна. Расстояние от верхнего края ВМС до верхней границы полости матки не должно превышать 5 мм, а до дна матки 20 мм. Увеличение этих размеров позволяет предполагать смещение ВМС в сторону шейки матки и ослабление контрацептивного эффекта.
Для проведения обследования с использованием трансвагинального доступа мочевой пузырь не должен быть заполнен. Вначале следует получить изображение тела матки в продольной плоскости (по длинной оси), смещая датчик справа налево путем изменения угла его наклона. Затем получают изображения в поперечных плоскостях (по короткой оси). Косвенно о положении матки можно будет судить по ориентации датчика, при котором матка визуализируется лучше всего. Так, например, если оптимальное изображение наблюдается при наклоне датчика кзади, то матка, вероятно, находится в положении retroflexio.
С внедрением в широкую клиническую практику трансвагинального сканирования с высокой разрешающей способностью существенно возросла роль ультразвукового исследования в оценке шейки матки.
Прежде чем перейти к описанию размеров и контуров матки, необходимо остановиться на особенностях отображения ее различных анатомических областей, среди которых выделяют три основных отдела: дно, тело и шейку. Сегмент, располагающийся выше устьев маточных труб, обозначается как дно матки. Сегмент между дном и границей на уровне внутреннего зева обозначается как тело матки. Хотя нижнюю часть тела матки иногда обозначают как независимый сегмент, называемый перешеек матки, такое выделение является достаточно спорным, поскольку он не имеет четкого функционального или анатомического обособления и представляет собой переходную область от гладкой мускулатуры стенки тела к стенке шейки матки, которая состоит преимущественно из соединительной ткани.
Размеры шейки матки в репродуктивном возрасте в норме составляют: длина 20-45 мм (в среднем - 30 мм), переднезадний размер
30-40 мм, ширина - до 40 мм. В то же время известно, что нормальные размеры матки у нерожавших женщин в репродуктивном периоде составляют: длина 7 см, ширина 4 см и переднезадний размер 4 см. Стенки матки становятся относительно более толстыми в области дна, а пропорциональная длина шейки становится меньше. У многорожавших женщин, в отличие от не имевших роды, все размеры в среднем увеличиваются на 1-2 см.
Соотношение длина тела матки/длина шейки матки равно 2/1 при нормальном развитии органов начиная с позднего пубертатного периода. До начала полового созревания это соотношение равно 1 /3. В репродуктивном возрасте соотношение переднезадний размер тела матки/ переднезадний размер шейки матки равно 1,5/1. В постменопаузе размеры матки уменьшаются по сравнению с нормальными для женщин фертильного возраста. В среднем ее длина уменьшается до 3,5-6,5 см, а переднезадний размер - до 1,2-1,8 см.
Эндометрий с помощью трансвагинального исследования отчетливо определяется у подавляющего большинства пациенток. При этом он всегда имеет вид различной, но равномерной по толщине полосы, расположенной в центральной части тела матки. Поскольку иногда, особенно в постменопаузальном периоде, невозможно четко разграничить два слоя эндометрия, оценка его толщины производится на основании измерения обоих слоев вместе.
Поэтому нередко вместо термина удвоенный слой эндометрия употребляются термины - М-эхо матки или срединная эхоструктура матки.
Контуры эндометрия четкие, ровные. Толщина эндометрия и его объем варьируют в зависимости от дня цикла или продолжительности
постменопаузального периода.
Толщина неизмененного эндоцервикса в репродуктивном возрасте оставляет в среднем 2-5 мм (максимально - 6 мм) и практически не меняется по фазам цикла. Цервикальный канал в норме может быть расширен до нескольких миллиметров в периовуляторный период за счет слизи, имеющей вид анэхогенного содержимого. В отличие от тела матки в период постменопаузы шейка практически не уменьшается в размерах, а эндоцервикс может не визуализироваться.
В полости малого таза яичники располагаются позади широких связок матки и фиксируются к ним посредством коротких брыжеек. К углу матки яичник прикрепляется собственной связкой, а к терминальной линии боковой связки таза – воронко-тазовой связкой. Непосредственно над яичниками располагаются ампулярный и фимбриальный отделы маточных труб. Расположение и визуализация яичников в малом тазу зависит от эхографического доступа, наличия объемных образований, наполнения кишечника и мочевого пузыря, а также от фазы менструального цикла или количества лет постменопаузы и перенесенных гинекологических заболеваний. Симметричность расположения яичников также определяется вышеперечисленными факторами. При трансабдоминальном УЗИ ориентирами при типичной локализации яичников являются трубные углы, дно и боковые поверхности матки, а при трансвагинальном яичники чаще располагаются рядом с внутренней подвздошной веной. У женщин репродуктивного возраста яичники имеют вид небольших овальной формы образований средней эхогенности (немного ниже эхогенности матки) с характерными эхонегативными включениями (обычно от 5 до 7-8 включений), представляющими эхографическое изображение фолликулярного аппарата - созревающих или атрезирующих фолликулов. Именно фолликулярный аппарат является эхографическим маркером яичника Его определение возможно с 8-9 лет (единичные фолликулы в виде
округлых эхонегативных включений диаметром до 5 мм). После хирургического удаления тела матки яичники чаще всего обнаруживаются в непосредственной близости от культи. После гистерэктомии расположение яичников более вариабельно, что связано с различными методами зашивания купола влагалища.
Яичники - парные гормонопродуцирующие органы, расположенные по заднему листку широкой связки матки и фиксированные к ней посредством
собственной связки, идущей к трубным углам матки, а также брыжейки, прикрепляющейся ниже ампулы маточной трубы. Форма яичников уплощенно овоидная. Непосредственно над яичниками располагается ампулярный (фимбриальный) отдел маточных труб. Положение яичников в малом тазу во многом зависит от степени наполнения мочевого пузыря, содержимого кишечника, а также наличия объемных образований (генитальных и экстрагенитальных).
Яичник состоит из соединительнотканной стромы, включающей корковый и мозговой слои, фолликулярного аппарата и капсулы. В корковом слое, содержащем, т.н., герминальную паренхиму, находятся фолликулы, а в более глубоком, мозговом, располагаются кровеносные и лимфатические сосуды, а также нервные волокна. У здоровой женщины репродуктивного возраста при нормальном менструальном цикле в среднем только 5-6 фолликулов из 10-20 развивающихся достигают стадии визуально определяемых. После 8-9-го дня менструального цикла обычно появляется доминантный фолликул, размеры которого в это время уже превышают 12-15 мм в диаметре. Развитие остальных фолликулов останавливается, и они, достигнув примерно 8-10 мм в диаметре, подвергаются атретическим изменениям.
Эхографически строма представляет собой однородную ткань, эхогенность которой равна эхогенности неизмененного миометрия. Фолликулы визуализируются как мелкие анэхогенные включения округлой формы, четко отграниченные от окружающей стромы, расположенные преимущественно по периферии, т.е. в кортикальном слое. Количество выявляемых фолликулов зависит от возраста пациентки: чем моложе женщина, тем больше определяется анэхогенных структур, однако в одном срезе. Эхографически созревший фолликул (зрелый фолликул) накануне овуляции представлен однокамерным анэхогенным образованием средним диаметром не менее 17 мм, с фрагментарным утолщением и неровностью стенки. Зрелый фолликул характеризуется появлением двойного контура вокруг него и, до 80% случаев, наличием пристеночной дупликатуры.
Доминантный фолликул продолжает увеличиваться в среднем на 2-3 мм в день и к моменту овуляции достигает 18-24 мм, составляя в среднем 20 мм.
Под действием гонадотропинов, протеолитических ферментов, а также благодаря рефлекторному влиянию окситоцина стенка созревшего фолликула разрывается. Далее яйцеклетка попадает в брюшную полость, т.е. происходит овуляция, являющаяся окончанием фолликулярной фазы менструального цикла. При УЗИ во время овуляции, продолжительность которой составляет 15-60 мин, а также в первые-вторые сутки после нее в строме яичника визуализируется анэхогенное или гипоэхогенное включение неправильной формы, с четким, но неровным контуром, средним диаметром 10-15 мм.
В периовуляторный период в позадиматочном пространстве и параовариальной области определяется небольшое количество свободной жидкости. Эта жидкость образуется вследствие частичного истечения из фимбриального отдела маточных труб, рефлекторной экссудативной реакции брюшины и собственно фолликулярной жидкости.
После овуляции под воздействием преимущественно лютеинизирующего гормона происходит разрастание гранулезных клеток и накопление липидов. Это приводит к образованию желтого тела, которое является гормональным органом, поддерживающим беременность ранних сроков. Желтое тело имеет меньшие, чем зрелый фолликул, размеры и фрагментарно утолщенные стенки без четкого внутреннего контура. Внутреннее строение желтого тела характеризуется многообразием ультразвуковой картины, но чаще – эхопозитивное или гипоэхогенное с различными вариантами включений. Если беременность не наступает, то к менструации желтое тело претерпевает обратное развитие и после нее превращается в белое тело. При цветовом допплеровском картировании нормальное желтое тело имеет выраженный цветовой ореол по периферии. Численные значения параметров кровотока указывают на его интенсивность: индекс резистентности до 0,47, максимальная скорость кровотока - до 25 см/с. Обнаружение таких показателей, с одной стороны, является прогностически благоприятным для полноценности желтого тела, однако создает определенные трудности в дифференциальной диагностике яичниковых новообразований, имитируя неопластический процесс. С наступлением перименопаузы происходит постоянная регрессия фолликулярного аппарата и уменьшение размеров яичников. В первые 5 лет отсутствия менструаций допустимо наличие мелких (2-3 мм) единичных фолликулов первого порядка, однако размер их никогда не достигает преовуляторного фолликула, овуляция не происходит, желтое тело не формируется. В постменопаузе более 5 лет в строме яичника фолликулы не определяются. Любое анэхогенное включение в яичнике должно рассматриваться как подозрительное на развитие онкологического процесса.
Измерение яичников необходимо проводить в трех взаимно перпендикулярных плоскостях. Сначала каждый из яичников выводится по длине, на этом же срезе измеряется толщина. После этого плоскость сканирования меняется на 90 градусов, и производится измерение ширины.
Размеры яичников значительно варьируют и зависят от возраста, а для женщин репродуктивного периода – от фазы менструального цикла. Более точным является определение их объема, который в норме у женщин репродуктивного возраста не должен превышать 9-10 см. куб.
Размеры яичников у женщин репродуктивного возраста:
- Длина – 20-40 мм,
- Передне - задний размер – 10-25 мм,
- Ширина – 15-30 мм.
Однако в зависимости от фазы менструального цикла их размеры могут варьировать в следующих пределах: длина - от 25 до 40 мм, ширина - от 15 до 30 мм, толщина - от 10 до 20 мм. Более качественной оценкой размеров яичников является их объем. Его можно рассчитать по формуле эллипса: 0,523 х Длина (см) х Толщина (см) х Ширина (см). В норме объем яичников не превышает 9-10 см3.
С наступлением климактерического периода размеры яичников уменьшаются, что значительно затрудняет их визуализацию. Чем больше длительность менопаузы, тем реже они определяются. Следует подчеркнуть, что выявление у женщин в глубокой постменопаузе яичников объемом более 5 см3, является признаком патологии.
При менопаузе более 20 лет яичниковая ткань идентифицируется не чаще, чем 3-4% случаев. Разница в объеме правого и левого яичника не должна превышать 1:1,5. Асимметричное увеличение одного из яичников более чем в 2 раза - у женщин в постменопаузе это является одним из признаков малигнизации.
Маточные (фаллопиевы) трубы являются парным трубчатым органом, осуществляющим функции транспортировки яйцеклетки и сперматозоидов,
создания благоприятной среды для процесса оплодотворения, развития зиготы и продвижения ее в матку
Трубы начинаются от устьев в полости матки и имеют следующие отделы: интерстициальный (маточный или интрамуральный), заключенный в толще миометрия, длиной 10-30 мм и с диаметром просвета, не превышающего 1 мм За пределами тела матки начинается перешеечный (истмический) отдел, длина которого 30-40 мм, идущий горизонтально к стенкам малого таза между листками широкой связки матки Следующая за перешейком часть называется ампулой, которая занимает примерно половину всей длины трубы и заканчивается воронкой с длинными, узкими фимбриями, прикрывающими брюшное отверстие (устье) трубы. Самая длинная фимбрия, называемая яичниковой, прикрепляется к нему. Длина маточной трубы у женщин репродуктивного возраста составляет в среднем10-12 см, а толщина0,5 см. Правая труба обычно несколько длиннее левой. Снаружи трубы покрыты серозной оболочкой. Мышечный слой представлен тремя слоями гладкой мускулатуры: наружный и внутренний, идущие в продольном направлении, и средний в поперечном, что позволяет совершать перистальтические
движения. Подслизистый слой отсутствует.
Неизмененные маточные трубы, как правило, не видны при трансабдоминальном ультразвуковом исследовании. Исключение составляют случаи, когда отмечается скопление большого количества жидкости в полости малого таза, например, при асците. Иногда при ультразвуковом исследовании при поперечном сканировании матки видны линейные трубчатые образования, отходящие от маточных углов.
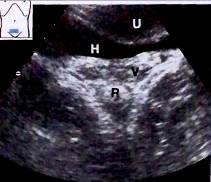
Рис. 7 Поперечное сечение. Дно матки (U) располагается кпереди от мочевого пузыря (Н), сзади от мочевого пузыря находится влагалище (V), за ним прямая кишка (R).
Следует помнить, что эти образования могут быть маточными
трубами, но в действительности они чаще являются связками. Кроме
того, за маточные трубы иногда ошибочно принимаются расширенные вены малого таза, которые легко идентифицируются при допплеровском исследовании. Дополнительным отличием служит расположение маточных труб: они имеют связь с трубным углом матки, располагаются сбоку от матки и фимбриальный конец направлен в сторону позади маточного пространства.
При трансвагинальном ультразвуковом исследовании с использованием высокоразрешающей эхографии у части пациенток удается визуализировать неизмененные маточные трубы. При скоплении жидкости в просвете маточных труб, например, при воспалительном процессе, они становятся доступными для ультразвуковой визуализации.
Воспалительная и неопластическая патология матки
Воспалительные заболевания половых органов (ВЗПО) у женщин занимают 1-е место в структуре гинекологической патологии и составляют 60—65% обращаемости в женские консультации. Возможно, число заболевших больше, так как нередко при стертых формах больные к врачу не обращаются. Рост числа ВЗПО во всех странах мира является следствием изменения полового поведения молодежи, нарушения экологии и снижения иммунитета.
. По данным ВОЗ, частота воспалительных заболеваний половых органов при половом пути передачи составила 1% от общего числа населения и 2-3% от числа сексуально активной части населения. В промышленных странах Европы и США ежегодно частота сальпингита у женщин в возрасте от 15 до 39 лет составляет 10-13 на 1000 женщин; среди больных 75% – женщины моложе 25 лет, из них 75% – нерожавшие.
Воспалительные заболевания хламидийной этиологии у подростков 15-19 лет составляют 16%, в возрасте 25-29 лет – 6%, старше 30 лет – 2,5%. Микоплазмы, уреаплазмы и коринебактерии как причина воспалительных заболеваний половых органов чаще наблюдаются в группе молодых женщин (до 20 лет).
В возрастной группе старше 30 лет первое место среди возбудителей воспалительных процессов занимают анаэробные микроорганизмы. Острые воспаления придатков матки чаще наблюдаются в возрастной группе 20-24 года; хронические процессы и их последствия (бесплодие, эктопическая беременность) встречаются у женщин 25-34 лет. Кроме того, возрастает роль микст-инфекции, которая является серьезной проблемой, ибо в этом случае увеличивается патогенность каждого из возбудителей. В таких случаях воспаление вызывает выраженную реакцию тканей (слизистой оболочки влагалища, эктоцервикса, выводных протоков больших вестибулярных желез, мочеиспускательного канала, мочевого пузыря, прямой кишки, матки, маточных труб, яичников), сопровождающуюся повреждением эпителия, деструкцией и дисплазией. Это приводит к развитию не только кольпита, эндоцервицита, цистита и проктита, но может играть существенную роль в формировании эктопий шейки матки, по свой сути являющихся фоновыми предраковыми заболеваниями, тубоовариальных гнойных образований, миомы матки, грозящих женщинам радикальными операциями с возможной потерей некоторых специфических функций женского организма.
Общие инфекционные заболевания, сопровождающиеся снижением иммунитета, эндокринные нарушения, использование гормональных и внутри маточных контрацептивов, прием цитостатиков нарушают качественный и количественный состав микрофлоры влагалища, что облегчает инвазию патогенных микроорганизмов и может приводить к развитию воспалительных процессов, вызванных условно-патогенными бактериями.
Цервикальный канал служит барьером между нижними и верхними отделами половых путей, а границей является внутренний зев матки. В цервикальной слизи содержатся биологически активные вещества в высокой концентрации. Цервикальная слизь обеспечивает активацию неспецифических факторов защиты (фагоцитоз, синтез опсонинов, лизоцима, трансферрина, губительных для многих бактерий) и иммунных механизмов (система комплемента, иммуноглобулины, Т-лимфоциты, интерфероны). Гормональные контрацептивы вызывают сгущение цервикальной слизи, которая становится труднопроходимой для инфекционных агентов.
Распространению инфекции также препятствуют отторжение функционального слоя эндометрия во время менструации вместе с попавшими туда микроорганизмами. При проникновении инфекции в брюшную полость пластические свойства тазовой брюшины способствуют отграничению воспалительного процесса областью малого таза.
Пути распространения инфекции. Распространение инфекции из нижних отделов половых путей в верхние может быть пассивным и активным. К пассивному относятся распространение через цервикальный канал в полость матки, в трубы и брюшную полость, а также гематогенный или лимфогенный путь. Микроорганизмы могут также активно транспортироваться на поверхности двигающихся сперматозоидов и трихомонад.
Распространению инфекции в половых путях способствуют:
• различные внутриматочные манипуляции, при которых происходит занос инфекции из внешней среды или из влагалища в полость матки, а затем инфекция попадает через маточные трубы в брюшную полость;
• менструация, во время которой микроорганизмы легко проникают из влагалища в матку, вызывая восходящий воспалительный процесс;
• роды;
• операции на органах брюшной полости и малого таза;
• очаги хронической инфекции, обменные и эндокринные нарушения, недостаточность или несбалансированность питания, переохлаждения, стрессы и др.
Классификация воспалительных процессов гениталий в зависимости от вида возбудителя
По данному признаку ВЗПО делятся на специфические и неспецифические.
К специфическим относятся: сифилис, гонорея, трихомониаз, туберкулез, хламидиоз, уреаплазмоз, микоплазмоз, вирусные заболевания – генитальный герпес, папилломавирусная инфекция, цитомегаловирусная инфекция.
Неспецифические – вызванные условно-патогенной флорой – бактероиды, пептострептококки, эубактерии, энтерококки, кишечная палочка и др.
Классификация воспалительных заболеваний гениталий по локализации
В зависимости от локализации воспалительные процессы гениталий делятся на воспалительные заболевания нижних и верхних отделов половых органов. Границей между ними служит внутренний маточный зев.
К воспалительным заболеваниям нижних отделов женских половых органов относят: вульвит, бартолинит, вестибулит, кольпит (вагинит),
Заболевания верхних отделов половых органов включают: цервицит (эндоцервицит), эндометрит, эндомиометрит, панметрит, периметрит, сальпингит, оофорит; параметрит, пельвиоперитонит, мешотчатые тубоовариальные образования).
Классификация воспалительных заболеваний гениталий по течению
По течению воспалительные процессы делятся на острые, подострые и хронические. Хронические процессы могут быть следствием перенесенных острых воспалительных процессов. Кроме того, воспалительный процесс может носить изначально первично хронический характер. Хроническая стадия процесса определяется на основании ее длительности (месяцы, годы). Течение воспалительного процесса в значительной степени зависит от выраженности общей и местной реакции, что и предопределяет дальнейшую тактику ведения и лечения больных.
Данная классификация достаточно условна, т.к. выраженность воспалительного процесса и его длительность статистически значимой корреляции (взаимной зависимости) в целом не имеют и зависят от вирулентности возбудителя, особенности реакции нервной системы и иммунологической реактивности организма.
Классификация воспалительных заболеваний внутренних гениталий по стадиям:
- острая – до двух недель;
- подострая – 6-8 недель;
- хроническая – фазы обострения и ремиссии;
- рубцово-спаечная форма.
Выделяются два варианта обострения хронического воспалительного процесса:
1) Обострение с признаками, характерными для острого или подострого процесса (возрастание агрессивности возбудителя, выраженность общей или очаговой реакции, экссудативные изменения в очаге воспаления.)
2) Обострение без признаков, присущих острому воспалительному процессу (выражена очаговая реакция без фазы экссудации в очаге). Такая симптоматика характерна для рубцово-спаечной формы воспалительного процесса.
Среди инструментальных методов диагностики воспалительных заболеваний органов малого таза у женщин применяют лапароскопию, гистеросальпингографию, томографию и эхографию.
Диагностическая ценность лапароскопии достигает 96-98 %. Однако, риск возможных осложнений, особенно у больных с осложненными формами гнойного воспаления, выраженный спаечный процесс, а также ожирение III-IV степени являются противопоказаниями для операции. Применение гистеросальпингографии возможно только после купирования клинических симптомов воспалительного процесса для определения проходимости маточных труб. Компьютерная и магнитно-резонансная томография позволяют с точностью до 100% дифференцировать опухолевидные образования придатков, но эти способы диагностики не всегда доступны. Эхография, особенно с применением ТВ сканирования, является наиболее распространенным методом инструментальной диагностики в гинекологии. По данным А.Н. Стрижакова и соавт., а также В.И. Краснопольского и соавт. информативность ультразвуковой диагностики гнойных воспалительных
заболеваний внутренних половых органов достигает 92%, а тубоовариальных образований92,5% В.Н. Демидов и Б.И. Зыкин отмечают, что точность определения нозологической принадлежности придаткового образования составляет 72%.
Эндоцервицит - воспаление слизистой оболочки цервикального канала, возникает в результате травмы шейки матки при родах, абортах, диагностических выскабливаниях и других внутриматочных вмешательствах. Тропность к цилиндрическому эпителию канала шейки матки особенно характерна для гонококков, хламидий. Эндоцервицит часто сопутствует другим гинекологическим заболеваниям как воспалительной (кольпит, эндометрит, аднексит), так и невоспалительной (эктопия, эктропион шейки матки) этиологии. В острой стадии воспалительного процесса больные жалуются на слизисто-гнойные или гнойные выделения из половых путей, реже на тянущие тупые боли внизу живота. Осмотр шейки матки с помощью зеркал и кольпоскопия выявляют гиперемию и отек слизистой оболочки вокруг наружного зева, иногда с образованием эрозий, серозно-гнойные или гнойные выделения из цервикального канала. Хронизация заболевания приводит к развитию цервицита с вовлечением в воспалительный процесс мышечного слоя. Хронический цервицит сопровождается гипертрофией и уплотнением шейки матки, появлением небольших кист в толще шейки (наботовы кисты ovulae Nabothii).
Диагностике эндоцервицита помогают бактериологическое и бактериоскопическое исследование выделений из цервикального канала, а также цитологическое исследование мазков с шейки матки, которое позволяет обнаружить клетки цилиндрического и многослойного плоского эпителия без признаков атипии, воспалительную лейкоцитарную реакцию.
Достоверных ультразвуковых признаков стадий течения воспалительного процесса слизистой цервикального канала, а также эхографических особенностей в зависимости от вида возбудителя не существует.
Эхографические признаки эндоцервицита следующие:
• Утолщение М-эха более 5 мм;
• Неоднородная структура эндоцервикса;
• Гиперэхогенные включения в эндоцервиксе;
• Неровная граница между слизистой и мышечным
слоем;
• Множественные кисты шейки;
• Анэхогенное содержимое в просвете цервикального канала вне периовуляторной фазы;
• Гиперэхогенные включения малых размеров с
акустическим феноменом, характерным для пузырьков газа;
• Васкуляризация эндоцервикса;
• Обильная васкуляризация подлежащих тканей.
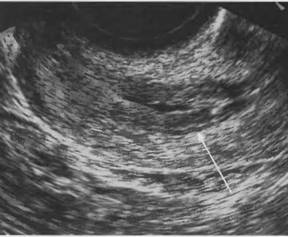
Рис. 8. Эндоцервицит, ТВ сканирование, эндоцервикс четко отграничен от миометрия гиперэхогенной тонкой полосой (указано стрелкой), эндоцервикс гипоэхогенный, неоднородный, в цервикальном канале анэхогенное содержимое
В отличие от эндометрия, эхографическая карты на эндоцервикса не меняется в зависимости от фазы цикла, и нормой является однородная структура с гиперэхогенной линией смыкания листков слизистой.
В связи с тем, что соединительнотканная оболочка эндоцервикса переходит в мышечный слой без четких границ, эта зона не имеет четкого контура. Такие особенности нормального строения шейки усложняют диагностику воспалительного процесса.
Граница между слизистой и мышечным слоем при воспалительном процессе становится неровной, но может быть и чрезмерно выражена. Линия смыкания слизистой цервикального канала также может быть или неопределяемой, или же гиперэхогенной, утолщенной.
Неоднородная структура слизистой возникает вследствие участков повышенной и сниженной эхогенности, а также гиперэхогенных включений в ней, которые, возможно, представляют собой участки фиброза и микрокальциноза. Отмечается большое количество кист как в эндоцервиксе, так и в мышечном слое.
Ретенционные кисты шейки при воспалении имеют гиперэхогенные стенки неоднородной толщины, внутренняя поверхность - неровная, содержимое неоднородное, вплоть до гиперэхогенного. Имеется сообщение о применении интерна цервикального сканирования с помощью датчика частотой 20 МГц для оценки патологических изменений эндоцервикса. По мнению авторов, использование этого метода улучшает визуализацию слизистой, но имеет ограничение глубины сканирования, которая не превышает 7 мм. В связи с экссудацией в просвете цервикального канала визуализируется анэхогенное содержимое. Расширение канала может быть, как на всем протяжении, так и фрагментарно.
В просвете цервикального канала, а также в слизистой можно визуализировать мелкие гиперэхогенные включения, дистальный (по отношению к датчику) полюс которых имеет треугольную форму. Иногда регистрируется перемещение этих образований в жидкости, заполняющей цервикальный канал, что дает основание расценивать их как пузырьки газа.
Процессы экссудации и пролиферации ведут к увеличению толщины М-эха.
В случае распространения воспаления на мышечный слой, структура шейки становится неоднородной.
При использовании цветового картирования вы являются сосуды в эндоцервиксе и гиперваскуляризация подлежащего мышечного слоя. Применяя спектральную допплерографию, определяется преимущественно венозный кровоток.
Необходимо отметить, что отсутствуют достоверные эхографические признаки воспалительного процесса в шейке матки. Для того, что бы выявить эндоцервицит, при том, что у пациентки могут при сутствовать не все маркеры одновременно, необходимо наличие 3и более эхографических признаков, и чем больше их обнаружено, тем точнее диагностика. При подозрении на эндоцервицит необходимо лабораторное исследование содержимого цервикального канала.
Эндометрит - воспаление слизистой оболочки матки с поражением как функционального, так и базального слоя. Острый эндометрит, как правило, возникает после различных «внутриматочных манипуляций аборта, выскабливания, введения внутриматочных контрацептивов (ВМК), а также после родов. Воспалительный процесс может быстро распространиться на мышечный слой (эндомиометрит), а при тяжелом течении поражать всю стенку матки (панметрит). Заболевание начинается остро с повышения температуры тела, появления болей внизу живота, озноба, гнойных или сукровично-гнойных выделений из половых путей. Острая стадия заболевания продолжается 8—10 дней и заканчивается, как правило, выздоровлением. Реже происходит генерализация процесса с развитием осложнений (параметрит, перитонит, тазовые абсцессы, тромбофлебит вен малого таза, сепсис) или воспаление переходит в подострую и хроническую форму.
При гинекологическом осмотре определяются гноевидные выделения из цервикального канала, увеличенная матка мягковатой консистенции, болезненная или чувствительная, особенно в области ребер (по ходу крупных лимфатических сосудов). В клиническом анализе крови выявляются лейкоцитоз, сдвиг лейкоцитарной формулы влево, лимфопения, повышение СОЭ. При ультразвуковом сканировании определяются увеличение матки, нечеткость границы между эндометрием и миометрием, изменение эхогенности миометрия (чередование участков повышения и понижения эхоплотности), расширение полости матки с гипоэхогенным содержимым и мелкодисперсной взвесью (гной), а при соответствующем анамнезе наличие ВМК или остатки плодного яйца Эндоскопическая картина при гистероскопии зависит от причин, вызвавших эндометрит. В полости матки на фоне гиперемированной отечной слизистой оболочки могут определяться обрывки некротизированной слизистой оболочки, элементы плодного яйца, остатки плацентарной ткани, инородные тела (лигатуры, ВМК и др.).
При нарушении оттока и инфицирования выделений из матки вследствие сужения цервикального канала злокачественной опухолью, полипом, миоматозным узлом может возникнуть пиометра вторичное гнойное поражение матки. Возникают резкие боли внизу живота, гнойно-резорбтивная лихорадка, озноб. При гинекологическом исследовании отделяемое из цервикального канала отсутствует, обнаруживается увеличенное, округлой формы, болезненное тело матки, а при УЗИ расширение полости матки с наличием в ней жидкости с взвесью (по эхоструктуре соответствует гною).
Хронический эндометрит возникает чаще вследствие неадекватного лечения острого эндометрита, чему способствуют неоднократные выскабливания слизистой оболочки матки по поводу кровотечений, остатки шовного материала после кесарева сечения, ВМК. Хронический эндометрит понятие клинико-анатомическое; роль инфекции в поддержании хронического воспаления весьма сомнительна, вместе с тем есть морфологические признаки хронического эндометрита: лимфоидные инфильтраты, фиброз стромы, склеротические изменения спиральных артерий, наличие плазматических клеток, атрофия желез или, наоборот, гиперплазия слизистой оболочки с образованием кист и синехий (сращений). В эндометрии снижается число рецепторов к половым стероидным гормонам, результатом чего становится неполноценность превращений слизистой оболочки матки в течение менструального цикла. Клиническое течение латентное. К основным симптомам хронического эндометрита относят, нарушения менструального цикла мено- или менометроррагии вследствие нарушения регенерации слизистой оболочки и снижения сократительной способности матки. Больных беспокоят тянущие, ноющие боли внизу живота, серозно-гнойные выделения из половых путей. Нередко в анамнезе есть указания на нарушения генеративной функции бесплодие или самопроизвольные аборты. Хронический эндометрит можно заподозрить на основании данных анамнеза, клинической картины, гинекологического осмотра (небольшое увеличение и уплотнение тела матки, серозно-гнойные выделения из половых путей). Существуют ультразвуковые признаки хронического воспаления слизистой оболочки матки: внутриматочные синехии, определяемые как гиперэхогенные септы между стенками матки, нередко с образованием полостей.
Корреляции между ультразвуковыми и клиническими признаками эндометрита, а также зависимости от вида возбудителя не существует. По справедливому замечанию A.M. Стыгара и других исследователей, нередко даже на фоне выраженной клинической симптоматики эхографическое изображение матки может быть в пределах нормы
Эхографические признаки эндометрита (эндомиометрита) следующие:
· неоднородная структура эндометрия;
· смешанная (повышенная) эхогенность;
· асимметрия толщины стенок эндометрия;
· нечеткая линия смыкания листков слизистой;
· несоответствие структуры и эхогенности эндометрия фазе менструального цикла;
· утолщение или атрофия эндометрия;
· расширение полости матки за счет жидкостного содержимого;
· гиперэхогенные включения с акустическим феноменом, характерным для пузырьков газа;
· неровный контур М-эхо с гиперэхогенными включениями по периферии;
· увеличение размеров матки;
· неоднородная структура миометрия, особенно субэндометриального слоя;
· гиперваскуляризация субэндометриального слоя;
· расширение аркуатного и параметрального сплетения.
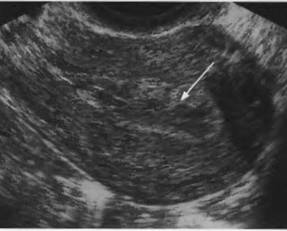
Рис. 9. Эндометрит: на фоне гипоэхогенного эндометрия в передней стенке имеются участки повышенной эхогенности (указано стрелкой);
При воспалительном процессе в эндометрии происходит отек и лимфоидная инфильтрация, что приводит к утолщению и неоднородной структуре. А.Н. Стрижаков и соавт. считают, что снижение эхогенности эндометрия соответствуют острому эндометриту . Вместе с тем, как при остром, так и при хроническом течении встречается повышенная или неоднородная эхогенность, что нарушает типичное изображение эндометрия, соответствующее фазе цикла. Воспаление это, как правило, диффузный процесс, но некоторые участки могут иметь неодинаковую реакцию, что приводит к локальным изменениям, которые, в свою очередь при ультразвуковом исследовании проявляются разной толщиной слизистой передней и задней стенок. При воспалительном процессе может не визуализироваться линия смыкания листков эндометрия, особенно, если он имеет неоднородную структуру.
Нарушение микроциркуляции сопровождается экссудацией как ткани эндометрия и подлежащего миометрия, так и скоплением экссудата в полости матки. В.Н. Демидов и соавт. расценивают этот признак, проявляющийся в первые 3 дня после окончания менструации, а затем исчезающий, как один из наиболее достоверный для диагностики эндометрита. Авторы считают, что это время, а также 23 дня накануне менструации являются оптимальным для исследования при подозрении на воспали тельный процесс полости матки У 17-20% больных появление жидкости в полости матки может быть единственным маркером острого эндометрита. Обычно скопившаяся жидкость имеет анэхогенную структуру и расширение полости не превышает 7 мм. Воспаление, возникшее после выскабливания полости матки по поводу прерывания беременности, приводит к гораздо большему зиянию полости, содержимое ее гетерогенное, с большим количеством гиперэхогенных включений, которые являются остатками элементов плодного яйца, сгустков крови и фибрином. Иногда в полости матки удается идентифицировать костные фрагменты эмбриона или плода.
У женщин постменопаузального возраста эндометрит может возникать на фоне физиологической серозометры и атрофичного эндометрия, что приводит к скоплению гнойного содержимого в полости матки (пиометра). Кроме этого, пиометра может сопутствовать карциноме эндометрия, особенно при ее распаде. Гной в полости матки визуализируется как эхогенное однородное или неоднородное содержимое. При высокой эхогенности гноя границы полости могут не определяться.
Жизнедеятельность персистирующей патогенной флоры, в том числе анаэробной, приводит к образованию пузырьков газа. Они визуализируются как отдельные мелкие гиперэхогенные включения, дистальный контур которых имеет треугольную форму за счет реверберации ультразвуковой волны и появления акустического феномена, называемого «хвост кометы». Этот признак, так же как и жидкость в полости матки, В.Н. Демидов и соавт. причисляют к наиболее достоверным для диагностики эндометрита
Так как при воспалительном процессе изменения происходят не только в функциональном слое, но и в базальном, пролиферация его визуализируется как зона неоднородно высокой или сниженной эхогенности с нечетким периферическим контуром М-эха. В этих случаях можно предположить вовлечение в процесс подлежащего миометрия. Кроме этого эндомиометрит характеризуется также увеличением размеров матки и неоднородной ее структурой, выраженной преимущественно множественными участками неравномерно сниженной эхогенности с гиперэхогенными включениями в субэндометриальном слое.
При цветовом картировании отмечается вас куляризация эндометрия и субэндометриальной зоны. Для выявления этого признака исследование лучше проводить в 1фазу цикла, когда нормой является аваскуляризация эндометрия и единичные цветовые локусы, получаемые от базальных артерий. У некоторых пациенток единственным признаком эндометрита, выявленном при ультразвуковом исследовании, может быть аваскуляризация слизистой и гиперваскуляризация подлежащего слоя миометрия Количественные допплерометрические показатели соответствуют нормативным параметрам, ИР 0,50 ± 0,08. Имеются сведения, что при хроническом процессе ИР в исследуемой зоне повышается, а прогностически неблагоприятным признаком является отсутствие кровотока при динамическом наблюдении.
Чувствительность и специфичность в диагностике эндометрита может достигать 86 и 92% соответственно, и точность повышается при обнаружении нескольких из перечисленных признаков, однако, ведущими в диагностике являются клинико-лабораторные данные. Косвенным признаком может быть положительная динамика на фоне проведения противовоспалительной терапии.
Гиперпластические процессы эндометрия возникают на фоне повышенной концентрации эстрогенов (классических и неклассических стероидов), реализующих пролиферативный эффект, воздействуя на рецепторы эстрогенов в ткани эндометрия. Частота выявления рецепторов эстрогенов и прогестерона, а также их концентрация варьируют в зависимости от вида патологии эндометрия и уменьшаются по мере прогрессирования пролиферативных процессов эндометрия:
- железистые полипы эндометрия
- железисто-фиброзные полипы
- железистая гиперплазия
- атипические гиперплазия и полипы эндометрия
- рак.
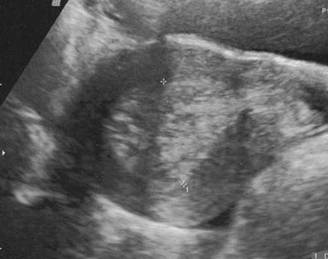 |
Рис.10.Гиперплазия эндометрия. Толщина М-эхо матки - 31,9 мм. Трансабдоминальное сканирование
Гиперэстрогенемия в пре- и постменопаузе может быть обусловлена:
• ановуляцией и недостаточностью лютеиновой фазы (в пременопаузе);
• избыточной периферической конверсией андрогенов в эстрогены при ожирении, особенно висцеральном;
• гормонпродуцирующими структурами в яичнике (текоматоз, опухоли);
• патологией печени с нарушением инактивационной и белково-синтетической (снижение синтеза белков-носителей стероидных гормонов) функций;
• патологией надпочечников;
• гиперинсулинемией (при сахарном диабете), приводящей к гиперплазии и стимуляции стромы яичника.
В постменопаузе как доброкачественные, так и злокачественные гиперпластические процессы эндометрия могут клинически проявляться кровяными выделениями из половых путей, но нередко остаются бессимптомными. Женщины в постменопаузе 2 раза в год должны проходить скрининговое обследование с УЗИ, а при необходимости (в группах риска по раку эндометрия) с аспирационной биопсией эндометрия. При эхографическом скрининге патология эндометрия в постменопаузе выявляется у 4,9% женщин при отсутствии жалоб. При ультразвуковых признаках патологии эндометрия выполняют гистероскопию и раздельное диагностическое выскабливание слизистой оболочки матки с последующим гистологическим исследованием соскобов. Осмотр полости матки при гистероскопии всегда позволяет выявить изменения эндометрия и проконтролировать удаление патологического очага.
|
| |
|
Рис. 11. Полип эндометрия (стрелки) маленьких размеров. ТВ сканирование.
|
Рис. 12. Крупный полип эндометрия (стрелки). ТВ сканирование. |
Эхографические признаки полипов эндометрия (как в пре-, так и в постменопаузе): локальное утолщение М-эха, включения повышенной эхогенности в его структуре, иногда с визуализацией цветовых эхо-сигналов кровотока в проекции включения. Диагностические трудности возможны при железистых полипах эндометрия, звукопроводимость с которых близка к таковой ободочки матки. Гиперплазия эндометрия в постменопаузе вызывает утолщение М-эха более 4—5 мм с сохранением четких контуров, частыми мелкими жидкостными включениями в структуре М-эха. При раке эндометрия эхографическая картина полиморфна.
По данным морфологического исследования выделяют доброкачественные (фиброзные, железисто-фиброзные, железистые полипы, железистая гиперплазия), предраковые пролиферативные процессы эндометрия (атипическая гиперплазия и полипы эндометрия с атипией клеток), рак эндометрия. Однако прогноз при гиперпластических процессах коррелирует не только с видом патологии эндометрия, но и с пролиферативным потенциалом ткани эндометрия. Высоковероятны рецидив, прогрессирование и малигнизация при атипических формах гиперплазии и полипах эндометрия с высокой пролиферативной активностью клеток.
Причиной рецидивов пролиферативных процессов эндометрия являются как опухолевые, так и неопухолевые (текоматоз) гормон продуцирующие структуры яичников, сохраняющиеся нейрообменные нарушения.
Миома матки является наиболее частой доброкачественной опухолью. Миому матки характеризует массовое распространение в женской популяции, медленный рост, относительная редкость осложнений, практически абсолютная доброкачественность течения. Она обнаруживается примерно у 20% женщин после 35 лет.
Обычное ультразвуковое исследование в подавляющем большинстве
случаев позволяет поставить правильный диагноз, но может не дать
точной информации о количестве, размерах и взаимоотношении миоматозных узлов с полостью матки. При эхографическом исследовании миоматозные узлы определяются в виде округлых или овальных образований с ровными контурами. В настоящее время в связи с повышением разрешающей способности ультразвуковых приборов воз можно диагностировать миоматозные узлы диаметром от 5 мм. Миома матки не вызывает увеличения размеров матки в тех случаях, когда миоматозные узлы имеют небольшие размеры или располагаются «на тонкой ножке». Обычно миома имеет округлую (или овоидную) форму с ровными контурами. Эхогенность обычно несколько сниженная. У миомы нет анатомической капсулы, что, как правило, можно заметить при эхографии небольших узлов без нарушения трофики. При росте узла образуется его псевдокапсула за счет сдавливания его периферических мышечных волокон.
Выделяют три основных локализации миоматозных узлов: субмукозная, интерстициальная, субсерозная. Диагностика субмукозной миомы, как причины кровотечения, является, наверное, одной из самых важных и тонких задач гинекологической эхографии. Субмукозные миомы деформируют полость матки (М-эхо) не менее чем на половину своего диаметра. Дифференциальная диагностика проводится прежде всего с полипами эндометрия. Одним из исходов длительного существования субмукозного узла является постепенное "выдавливание" его из полости матки, завершающееся "рождением" узла. Основание узла при этом превращается в длинную и тонкую ножку. Ультразвуковая диагностика рождающегося узла не очень сложна, но требует определенных навыков, в частности внимательного исследования шейки матки и цервикального канала. Шеечная миома составляет 8-10% от всех локализаций миомы. При диагностике этой патологии в первую очередь обращает на себя внимание увеличение за счет узла и деформация шейки матки. Визуализация 3-х и более миоматозных узлов позволяет сделать вывод о множественной миоме матки.
|
| |
|
Рис.13. Субсерозный миоматозный узел на широком основании (стрелки). ТВ сканирование. |
Рис.14. Множественные интерстициальные миоматозные узлы (стрелки). ТА сканирование. |
Субсерозно расположенные миоматозные узлы всегда приводят не только к увеличению матки, но и к существенной деформации ее контура. Субсерозный узел на узком и длинном основании - миома на ножке, или межсвязочная миома, нередко представляет диагностическую проблему ввиду значительно затрудненной дифференциации с новообразованиями яичников. Дифференциальная диагностика эхографической картины таких узлов усложняется тем, что при этом в большинстве случаев удается измерить все три стандартных размера тела матки, которые могут быть в пределах нормы. В таких случаях необходимо добиться визуализации интактных яичников и найти связь субсерозного миоматозного узла с маткой, т.е. идентифицировать ножку образования. Этому могут способствовать бимануальные манипуляции при ТВ ультразвуковом исследовании.
Кроме этого, существуют две промежуточные локализации: интерстициосубсерозная и интерстициальная с центрипетальным ростом (интерстициосубмукозная).
Интерстициально-субсерозная миома представляет из себя промежуточный вариант межмышечной миомы с тенденцией к наружному росту. Интерстициально-субсерозные миоматозные узлы деформируют наружный контур матки, а интерстициальные узлы с центрипетальным ростом отклоняют полость матки в контралатеральном направлении и могут приводить к ее незначительной деформации.
Межмышечная миома с центрипетальным ростом - промежуточный вариант межмышечной миомы с тенденцией к внутреннему росту. Растущий узел в итоге деформирует полость матки. Интерстициальные, интерстициальные с центрипетальным ростом и интерстициально-субсерозные миоматозные узлы обычно отграничены от окружающего неизмененного миометрия четкими контурами, создающими впечатление капсулы.
В большинстве случаев миоматозные узлы локализуются в теле матки.
Собственно говоря, известно, что миома матки - всегда мультилокусное заболевание, и решающим для определения врачебной тактики является не количество узлов, а общий размер комплекса матка-узлы, локализация и состояние узлов, а также, конечно - жалобы и состояние женщины.
Взаимоотношение узлов с полостью матки лучше определяется при
ТВ ультразвуковом исследовании, начиная с середины цикла, когда
лучше визуализируется М-эхо. Хотя эхография обладает высокой точностью в диагностике субмукозных миоматозных узлов, далеко не во всех случаях удается их правильно дифференцировать с полипами эндометрия, имеющими идентичную эхографическую структуру. Очень информативным дополнительным методом в дифференциальной диагностике внутриполостных образований является эхогистероскопия.
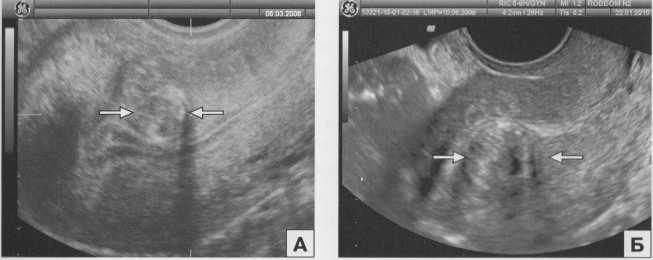
Рис. 15 Субмукозные миоматозные узлы (стрелки), деформирующие М-эхо матки и исходящие из передней (А) и задней (Б) стенки матки. ТВ сканирование.
При ТВ эхогистероскопии субмукозный миоматозный узел обычно визуализируется как образование средней эхогенности, округлой формы, с ровной поверхностью. При дифференциальной диагностике между полипом эндометрия и субмукозным миоматозным узлом необходимо учитывать форму выявленного образования: миоматозный узел чаще всего округлый, а полип стремится принять форму полости матки и поэтому обычно имеет вытянутую форму. Следует подчеркнуть, что при миомах образование пролабирует в полость матки и имеет четкую взаимосвязь с миометрием, в то время как при полипах в большинстве случаев определяется четкая граница между ними и стенками полости матки. Субмукозные миоматозные узлы бывают как на широком основании, так и на ножке. Последние могут экспульсироваться из полости матки.
При обнаружении субмукозных миоматозных узлов необходимо оценить степень пролабирования наибольшего диаметра опухолевого узла в полость матки так как это может оказать существенное влияние на выбор метода оперативного лечения. Тип О характеризуется полным расположением фиброматозного узла в полости матки («на ножке») без внутримиометрального распространения. При типе 1 фиброматозный узел имеет «сидячий» вид и его наибольший диаметр >50% занимает внутриполостную локализацию. При типе 2 внутриматочное расположение фиброматозного узла занимает <50%.
Цветовое допплеровское картирование (ЦДК) только иногда может оказать помощь в дифференциальной диагностике: для узлов миомы характерно наличие «огибающего» сосуда, а для полипа – сосуда в «ножке», но кровоток может вообще не определяться при малых размерах образований и особенностях их локализации.
По эхогенности миоматозные узлы чаще бывают средней или сниженной эхогенности, хотя бывают и узлы, имеющие повышенную эхогенность. Эхоструктура узлов зависит от соотношения в них соединительной и мышечной ткани, а также особенностей кровотока. При выраженной васкуляризации и превалировании мышечного компонента узел выглядит гипоэхогенным по сравнению с нормальным миометрием.
В миоматозных узлах могут определяться вторичные изменения в виде включений и/или зон повышенной или пониженной эхогенности.
Нарушения кровообращения возникают в 20-40% миоматозных узлов. Первым этапом нарушения питания узла является его отек, который проявляется существенным снижением эхогенности и диффузно неоднородной эхоструктурой узла. При дальнейшем ухудшении кровообращения в узле развиваются некротические изменения, визуализируемые как эхонегативные участки, обычно имеющие неправильную и весьма разнообразную форму. Исходом асептического некроза миоматозного узла может стать процесс гиалиноза, при котором некротические массы замещаются однородным гиалиновым содержимым. Гиалиноз, некроз или кистозные изменения обнаруживаются в виде гипо- или анэхогенных включений или зон в миоматозных узлах. Участки постнекротического гиалиноза обычно эхонегативны, в ряде случаев их содержимое может напоминать мелкодисперсную несмещаемую взвесь. Контуры этих образований четкие, неровные, имеют повышенную эхогенность за счет склероза и фиброза. Гиперэхогенные включения с дистальным акустическим эффектом поглощения (тенью) наиболее часто соответствуют кальцинированным или фиброзным изменениям. Часто участки обызвествления создают своеобразную картину гиперэхогенного ободка узла. Изредка некротические изменения в узле завершаются липоматозной дистрофией ткани и отложением жира в узле, что проявляется повышением эхогенности. Неравномерное повышение эхогенности узла в сочетании с его неровными контурами, отсутствием дальнейшего роста (либо тенденцией к уменьшению) свидетельствует о дегенеративных изменениях в узле.
Фибромы обычно имеют гомогенную или слоистую концентрическую эхоструктуру с четко очерченной гладкой наружной поверхностью. Они также могут содержать кальцификаты с акустической тенью или центральные некрозы. При повторных исследованиях необходимо всегда определять размеры узлов. Их быстрый рост позволяет предположить и своевременно диагностировать возможную, хотя и редкую, саркоматозную трансформацию
Эндометриоз - это медленно прогрессирующее заболевание, для которого характерно распространение эндометриоподобной ткани за пределы слизистой оболочки матки.
Частота эндометриоза, по данным различных авторов колеблется от 10 до 80%, что связано с разными методами диагностики и верификации. По мнению большинства исследователей эндометриоз встречается примерно с такой же частотой, как и миома матки, уступая только воспалительным заболеваниям органов малого таза. Эндометриоз наиболее распространен среди женщин 30-40 лет, однако, в 38,3-65% случаев он был выявлен при лапароскопии у подростков и женщин до 20 лет с хроническими тазовыми болями. Несмотря на то, что большинство авторов не усматривают связи с профессиональными и этническими факторами, имеются указания на то, что преимущественно болеют жительницы крупных городов (77,9%), работающие в сфере умственного труда (68-83,7%).
Эндометриоз - процесс развития ткани, идентичной эндометрию, за пределами полости матки. Принято различать наружный эндометриоз, поражающий влагалище, влагалищную часть шейки матки, ретроцервикальную область, придатки, брюшину и внутренний, связанный с поражением тела матки и верхней части шейки.
Факторами риска развития эндометриоза являются
· абсолютная или относительная гиперэстрогения;
· нарушения иммунного статуса (применение антибиотиков, гормональных препаратов, прививки;
грипп, ОРВИ, воспалительные процессы внутренних половых органов, общесоматическая и аллергическая патология; курение, злоупотреблением алкоголем и наркотиками);
· травматические повреждения эндометрия (аборты, диагностические выскабливания, хирургические вмешательства);
· раннее или позднее начало половой жизни, ее не-
регулярность, отсутствие половой гармонии, позднее материнство;
· генетическая предрасположенность;
· угнетение процесса апоптоза, активация пролиферации;
· хронические психо-эмоциональные стрессы в быту,
на производстве;
· нарушение метаболических процессов (липидов,
углеводов, фосфоинозитинов).
Существует несколько теорий этиопатогенетических факторов формирования заболевания, объединенная система которых представлена R.W. Shaw Очаги эндометриоза морфологически представляют собой кистозные или инфильтративно-рубцовые участки, состоящие из стромального и железистого компонентов эндометриоидоподобной ткани, которые могут быть в различных сочетаниях. Под влиянием гормонов яичников в очагах происходят циклические изменения, степень выраженности которых зависит не только от количественных соотношений клеточных компонентов, но и от рецепторного аппарата гетеротопий
Генитальный эндометриоз подразделяется на:
• внутренний (тело матки и перешеек, интерстициальные отделы маточных труб);
• наружный (влагалище, влагалищная часть шейки
матки, ретроцервикальная область, яичники, маточные трубы, брюшина).
Различают диффузную, очаговую и узловую формы эндометриоза матки. Внутренний эндометриоз чаще всего представлен диффузной формой. По данным В.Н. Демидова и соавт. (1996), наиболее характерными эхографическими признаками диффузной формы внутреннего эндометриоза являются:
1. округлая форма матки за счет увеличения переднезаднего
размера;
2. асимметрия толщины стенок матки, при этом более вероятно
утолщение задней стенки матки;
3. наличие участка/участков повышенной эхогенности в миомерии с прерывистым контуром и нередко с гипоэхогенными включениями;
4. наличие гипо- или анэхогенных мелких (1 -5 мм) включений по
всему объему матки;
5. визуализация в зонах миометрия с неоднородной структурой
полос повышенной и пониженной эхогенности, направленных перпендикулярно плоскости сканирования;
6. неровный, нечеткий контур эндометрия
.
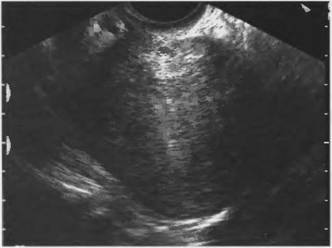
Рис. 16. Внутренний эндометриоз, диффузная форма. Округлая форма матки. (ТВ сканирование)
Для узловой формы заболевания характерно:
1. появление в стенке матки зоны повышенной эхогенности
округлой, овальной или неправильной формы, напоминающей миоматозный узел;
2. наличие в ней небольших (диаметром 2-6 мм) анэхогенных
включений или кистозных полостей (диаметром 7-32 мм), содержащих мелкодисперсную взвесь;
3. нечеткие контуры образования;
4. эндометриоидный узел всегда расположен интерстициально,
но при больших размерах может вызывать смещение М-эхо, без выраженной деформации полости матки;
5. отмечается повышенная эхогенность возле переднего контура
образования и пониженная - возле дальнего;
6. выявление в патологическом очаге близкорасположенных полос средней и низкой эхогенности, ориентированных перпендикулярно к плоскости сканирования.
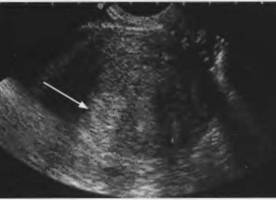
Рис. 17. Эндометриоз тела матки, узловая форма интерстициальный узел небольших размеров (указано стрелкой);
Эхографические признаки очаговой формы внутреннего эндометриоза:
1. появление в одном из участков миометрия зоны/зон повышенной неоднородной эхогенности с нечеткими и неровными контурами;
2. наличие внутри этой зоны отдельных кистозных включений
округлой и овальной формы диаметром 2-6 мм и кистозных полостей
диаметром 7-15 мм;
3. преимущественное увеличение одной стенки матки по сравнению с другой.
4. Дифференциальная диагностика узловой и очаговой форм внутреннего эндометриоза с точки зрения эхографии бывает затруднена, так как эти формы имеют сходные характеристики, в изолированном виде встречаются редко, чаще сочетаются с диффузным поражением миометрия или с миомой матки и сами по себе не оказывают выраженного влияния на тактику ведения пациентки.
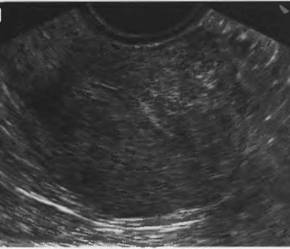
Рис. 18.Эндометриоз тела матки, очаговая форма два рядом расположенных эндометриоидных узла в задней стенке; (ТВ сканирование)
Существует несколько классификаций эндометриоза, основывающиеся как на клинических симптомах заболевания, так на глубине анатомического поражения органов и степени распространенности патологического процесса, выявляемых при хирургическом лечении. Кроме этого, имеется балльная оценка эндометриоза для прогнозирования восстановления фертильности
Наиболее распространенной в практике врачей ультразвуковой диагностики является классификация Б.И. Железнова и А.Н. Стрижакова, которая приводится далее:
Степени распространения внутреннего эндометриоза диффузной формы:
1 степень - поражение ближайших к эндометрию слоев миометрия на глубину 2-3 мм.
2 Степень в патологический процесс вовлекается до половины толщины стенки матки.
3 Степень - поражается весь миометрий до серозного покрова.
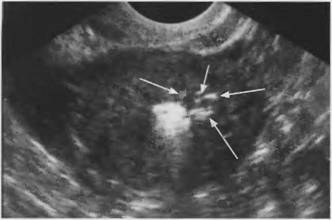
Рис. 19. Внутренний эндометриоз 1 степени распространения, при введении Эховиста-200 визуализируются эндометриоидные ходы (указано стрелками). (ТВ сканирование)
Авторы предлагают узловую или диффузную форму 2-3 степени обозначать как аденомиоз, при этом основным критерием здесь является гиперплазия мышечных волокон, а также различный подход к лечению, заключающийся в том, что консервативные методы могут быть успешными при1-2 степени распространения, а для более тяжелого течения, т.е. аденогмиоза хирургическое вмешательство
Допплерометрия при эндометриозе матки не выявляет зон неоваскуляризации, не характерно также наличие «огибающего» сосуда, чаще определяются точечные цветовые локусы кровоснабжения со средними значениями индекса резистентности; 0,58±0,06. Эндометриоидные гетеротопии представляют собой аваскулярные образования. При II - III степени распространения процесса происходит снижение скорости кровотока и повышение сосудистого сопротивления в маточных артериях, где индекс резистентности может составлять 1,0.
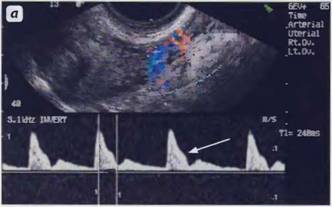
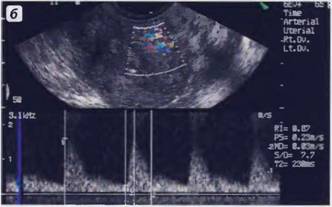
Рис. 20. Спектральная допплерометрия при внутреннем эндометриозе. а — маточная артерия: зубец S указан стрелкой; б —измерение индекса Hatle, показатель которого составляет 240 мс; в — артерия в зоне поражения: ИР 0,87, индекс Hatle 230 мс.(ТВ сканирование)
Точность ультразвуковой диагностики внутреннего эндометриоза
значительно возрастает при визуализации нескольких основных эхо-
графических признаков заболевания. Для качественной диагностики
эндометриоза необходимо использовать ТВ эхографию, проводить
обследование как в первую, так и во вторую фазы цикла, а также обязательно учитывать наличие клинической симптоматики.
Рост эндометриоидных очагов сопровождается расстройством микроциркуляции, повышением проницаемости сосудов, застойным полнокровием и отеком ткани миометрия, что приводит к гипоксии, которая, в свою очередь, усугубляет расстройство микроциркуляции. В очагах с преимущественным содержанием железистого эпителия циклические изменения не аналогичны таковым в эндометрии, даже во II фазе цикла наблюдается пролиферация различной степени выраженности, секреторная трансформация отмечена только в 6,8%, а малигнизация у 1% больных. Этиопатологическими факторами формирования эндометриоза являются
Получены убедительные данные о малигнизации у 11,4% больных эндометриозом тела матки и яичников
- Наследственность
- Менструальный рефлюкс
- Гормональные нарушения
- Иммунологические нарушения
- Имплантация
- Эндометриоидный трансплантат
- Прогрессирование и инвазия
- Гематогенная и лимфогенная диссеминация
Эндометриоз способен к инфильтративному росту и диссеминации, распространяясь по кровеносным и лимфатическим сосудам, что объединяет его со злокачественными опухолями. Эндометриоидные гетеротопии не имеют соединительнотканной капсулы, но, в отличие от злокачественных процессов, большинством авторов не отмечается клеточной атипии и прогрессивного автономного роста. Кроме этого, беременность благотворно сказывается на клиническом течении эндометриоза вследствие длительного воздействия гормонов желтого тела и плаценты, что также отличает эндометриоз от злокачественных опухолей, которые, как известно, значительно прогрессируют при беременности. В связи с неоднозначной позицией в отношении возможности малигнизации эндометриоза, некоторых похожих клинических и эхографических признаков следует иметь онконастороженность. Необходимо тщательно проводить дифференциальную диагностику со злокачественными новообразованиями, а в сомнительных случаях в первую очередь исключить онкологический процесс.
Рак шейки матки относится к наиболее распространенным злокачественным опухолям малого таза. Рак шейки чаще возникает у женщин 45-55 лет, однако, за последние 20 лет в России отмечается стойкая тенденция к росту этой патологии у молодых (до 29 лет), и среднегодовой темп прироста составляет 2,1%
Визуализация опухолевого узла при раке шейки матки возможна только при 1Б стадии, когда опухоль достигает 2-3 мм, ограничена шейкой матки с инвазией более 3 мм.
Классификация рака шейки матки по стадиям
(Минздрав СССР, 1985)
О стадия — преинвазивный (внутриэпителиальный) рак, Са in situ.
Ia стадия — опухоль ограничена шейкой матки,
инвазия не глубже 3 мм, диаметр опухоли не более
1 см (микроинвазивный рак).
16 стадия — опухоль ограничена шейкой матки,
инвазия глубже 3 мм.
IIа стадия — инфильтрация опухоли во влагалище, но не переходит на нижнюю треть и/или распространяется на тело матки.
IIб стадия — опухоль инфильтрирует параметрий с одной или обеих сторон, но не переходит на стенки таза.
IIIa стадия — инвазия нижней трети влагалища
и/или имеются метастазы в придатках; регионарные
метастазы отсутствуют.
Шб стадия — инфильтрация параметрия с одной
или обеих сторон до стенки таза, и/или имеются регионарные метастазы в лимфатические узлы таза и/или определяется гидронефроз и нефункционирующая почка, обусловленная стенозом мочеточника.
IVa стадия — инфильтрация мочевого пузыря
и/или прямой кишки.
IV6 стадия — отдаленные метастазы за пределами малого таза.
Как правило, опухолевый процесс начинается в зоне перехода многослойного плоского эпителия (эктоцервикса) и цилиндрического эпителия (эндоцервикса), которая находится на уровне наружного зева. По направлению опухолевого роста различают экзофитную (32-55,6%), эндофитную (33,3-52%) и смешанную форму (16%)
К характерным эхографическим признакам рака шейки матки относятся (Б.И. Зыкин и соавт., 2002):
1) утолщение М-эхо шейки матки;
1. увеличение размеров шейки матки (особенно передне- заднего размера и ширины) и ее неправильная форма, возможны нечеткие контуры;
1) изменение структуры шейки и эндоцервикса за счет хаотично расположенных мелких гиперэхогенных включений, образующих скопления, или анэхогенных включений диаметром 2-5 мм с неровными контурами;
4) исчезновение изображения эндоцервикса;
5) жидкость в цервикальном канале и полости матки;
6) изменения гемодинамики;
7) на поздних стадиях - вовлечение в процесс соседних органов (матки, мочевого пузыря, мочеточников, прямой кишки).
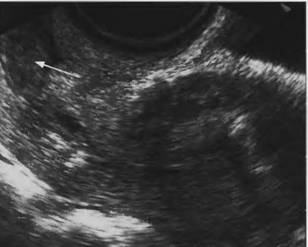 i
i
Рис. 21. Рак шейки матки: расположение гипоэхогенной опухоли в передней губе (указано стрелкой); ТВ сканирование)
Экзофитная опухоль характеризуется отсутствием четких контуров шейки матки в области наружного зева, неправильной формой и беспорядочными отражениями повышенной интенсивности. Для эндофитной опухоли в большей степени типична бочкообразная форма шейки матки неоднородной структуры с отражениями повышенной интенсивности.
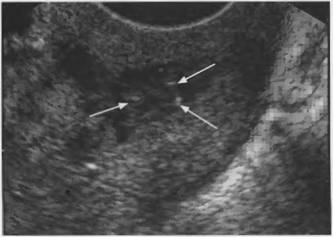
Рис.22. Рак шейки матки, гиперэхогенные включения (указаны стрелками) в ткани опухоли, (ТВ сканирование)
Возможна деформация перешейка, изменение угла между телом матки и шейкой. При смешанной форме в области шейки матки определяется бугристое образование, волнистый контур которого выявляется только на границе с телом матки, характер отражений различный: ближе к наружному зеву - отражения повышенной интенсивности, а выше - отражения пониженной интенсивности. Инфильтративный процесс вызывает нечеткость и неровность контуров опухоли.
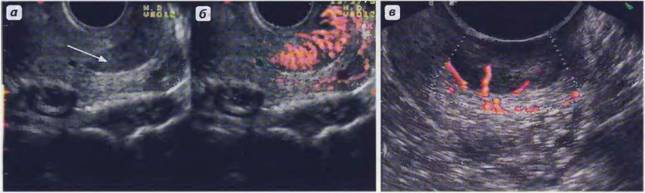
Рис.23. Неоваскуляризация визуализируемой карциномы шейки матки: а — В-режим, опухоль указана стрелкой; б — гипернеоваскуляризация опухоли (эхограммы из архива М.Н. Буланова); в — неоваскуляризация, по сравнению с предыдущей эхограммой отмечается меньшее количество сосудов в опухоли. (ТВ сканирование)
В ходе ЦДК выявляются: гиперваскуляризация шейки (снижение численных значений индекса резистентности в сосудах шейки менее 0,6), хаотично расположенные внутриопухолевые извитые сосуды с низкорезистентным и высокоскоростным характером кровотока (индекс резистентности при инвазивных формах и поздних стадиях процесса составляет 0,25-0,35; пиковая систолическая скорость кровотока > 20 см/с).При IIА стадии (рак, инфильтрирующий только влагалище и/ или тело матки) шейка матки имеет неправильную форму, бугристые контуры. Использование ТВ эхографии позволяет в большинстве случаев выявить распространение опухоли на стенки влагалища. Ультразвуковое исследование не всегда позволяет диагностировать инфильтрацию параметрия (IIБ стадия). Косвенным признаком инфильтративного процесса в параметрии может являться обструкция мочеточников с образованием гидронефроза. Эхография не является абсолютно надежным методом обнаружения метастазов в лимфоузлах у больных раком шейки матки, но поражение регионарных (тазовых) лимфоузлов свидетельствует о IIIБ стадии опухолевого процесса. С помощью ТВ эхографии может быть диагностирована инфильтрация мочевого пузыря (IV стадия), а в случаях фиксированного расположения кишечных петель заподозрено распространение процесса на кишечник.
Рак эндометрия (рак тела матки)
Рак эндометрия относится к гормонально-зависимым опухолям и чаще всего возникает на фоне рецидивирующих гиперплазии и полипов эндометрия в сочетании с эндокринно-обменными нарушениями.
В последнее время среди женщин, заболевших раком тела матки, до 42% составляют пациентки репродуктивного и перименонаузального возраста.
Существуют различные стадии рака эндометрия, характеризующиеся той или иной тяжестью заболевания.
Существуют два патогенетических варианта рака тела матки — гормонально-зависимый и автономный.
Гормонально-зависимый рак матки встречается примерно в 70% наблюдений, в патогенезе этого варианта рака играет роль длительная гиперэстрогения. Последняя может быть как абсолютной, так и относительной и возникать в результате ановуляции, феминизирующих опухолей яичника, избыточной периферической конверсии андрогенов в эстрогены (при ожирении, сахарном диабете), эстрогенных влияний (при заместительной гормональной терапии эстрогенами, лечении рака молочной железы тамоксифеном с образованием метаболитов с эстрогенной активностью) и т.д. Гормонально-зависимому раку тела матки предшествует последовательное возникновение гиперпластических и предраковых процессов эндометрия. Как правило, это высоко дифференцированная аденокарцинома, чувствительная к гормональной терапии. К факторам риска гормонально-зависимого рака тела матки относят бесплодие, отсутствие родов в анамнезе, позднюю менопаузу, ожирение, сахарный диабет, АГ, наследственную отягощенность по раку с эндокринно-метаболическим патогенезом (рак молочной железы, эндометрия, яичников, толстой кишки), гормонпродуцирующие опухоли яичника, заместительную монотерапию эстрогенами в постменопаузе, применение тамоксифена при лечении рака молочной железы.
Классификация рака тела матки
стадия — преинвазивная карцинома (атипическая гиперплазия эндометрия).
стадия — опухоль ограничена телом матки, регионарные метастазы не определяются.
1а — опухоль ограничена эндометрием.
16 — инвазия в миометрий до 1 см.
1в — инвазия в миометрий более 1 см, но отсутствует прорастание серозного покрова матки.
стадия — опухоль поражает тело и шейку матки, регионарные метастазы не определяются.
стадия — опухоль распространяется за пределы матки, но в пределах малого таза.
III a — опухоль инфильтрирует серозную оболочку матки и/или имеются метастазы в придатках матки и/или в регионарных лимфатических узлах таза.
III б — опухоль инфильтрирует клетчатку таза
и/или имеются метастазы во влагалище.
IV стадия — опухоль распространяется за пределы малого таза и/или имеется прорастание мочевого пузыря и прямой кишки.
IVa — опухоль прорастает мочевой пузырь и/или прямую кишку.
IV6 — опухоль любой степени местного и регионарного распространения с определяемыми отдаленными метастазами.
В ретроспективных исследованиях получены сведения о зависимости риска развития рака матки и выраженности гиперпластического процесса эндометрия. Рак матки возникает у 1% больных с железистой гиперплазией, у 3% — с железисто-кистозной, у 8% — с простой атипической гиперплазией и у 29% — со сложной атипической гиперплазией. Однако в постменопаузе этот риск выше, чем в другом возрасте.
Автономный патогенетический вариант рака эндометрия встречается менее чем в 30% наблюдений, возникает на фоне атрофии эндометрия при отсутствии гиперэстрогении у пациенток без обменно-эндокринных нарушений. Считается, что в развитии автономного варианта рака эндометрия играет роль выраженная депрессия Т-системы иммунитета на фоне нарушений адаптационного гомеостаза и гиперкортицизма. Изменения иммунитета состоят в значительном снижении абсолютного и относительного количества Т-лимфоцитов, угнетении всех субпопуляций Т-лимфоцитов и их теофиллин-чувствительных форм, большом количестве лимфоцитов с блокированными рецепторами.
Автономный рак тела матки развивается в более старшем возрасте. Для данного варианта не установлены факторы риска. Как правило, он появляется у худых пожилых женщин без предшествующих гиперпластических процессов. В анамнезе может отмечаться кровотечение в постменопаузе на фоне атрофии эндометрия. Опухоль имеет низкую дифференцировку, низкую чувствительность к гормонотерапии, происходят ранняя инвазия в миометрий и метастазирование
Данное заболевание можно диагностировать с помощью ультразвукового метода начиная с 0 стадии, однако опухоль должна быть макроскопических размеров.
Эхографическими признаками карциномы эндометрия являются:
• утолщение М-эха;
• нечеткая и неровная граница М-эха;
• неоднородная структура;
• повышенная (сниженная) эхогенность;
• средняя или несколько повышенная звукопроводимость;
• наличие гипер- гипо- и анэхогенных включений различной формы и величины;
• полиповидные разрастания, чаще локализуемые в области трубных углов и дна полости матки;
• жидкостное содержимое в полости матки;
• васкуляризация опухоли (и подлежащего мио-метрия) с низкорезистентным типом кровотока;
• неравномерное истончение миометрия, исчезновение четкого наружного контура матки.
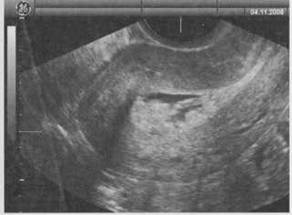
Рис. 24. Рак эндометрия. ТВ сканирование.
Известно, что больные с гиперпластическими процессами эндометрия, особенно на фоне нейро-эндокринно-обменных нарушений, относятся к высокой группе риска развития рака эндометрия. Сложность распознавания злокачественных процессов эндометрия и опухолей тела матки заключается в их значительной схожести с доброкачественными гиперпластическими процессами и опухолями у женщин репродуктивного и постменопаузального периодов.
Ультразвуковые характеристики опухоли в некоторой степени зависят от ее размеров. Эхогенность визуализируемой опухоли выше, чем неизмененного миометрия, и сочетается с неоднородной внутренней структурой. Отмечено, что при небольших размерах (до 15 мм в диаметре) эхогенность высокая, а структура — однородная. По мере увеличения размеров эхогенность снижается, становится смешанной, «пятнистой». Учитывая такую трансформацию, целесообразно у женщин репродуктивного возраста проводить исследование в раннюю пролиферативную фазу цикла. М.В. Медведев и соавт. сообщают о зависимости эхогенности опухоли от степени ее дифференцировки . Авторы отмечают, что высокодифференцированному раку соответствует повышенная эхогенность, в то время как для низкодифференцированного — более характерна смешанная.
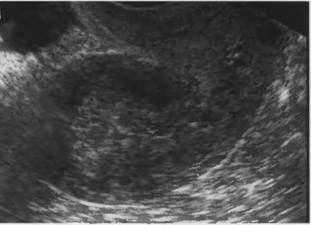
Рис.25. Карцинома эндометрия: нечеткий и неровный контур передней и задней стенки, истончение миометрия. (ТВ сканирование)
На инвазию в миометрий указывает отсутствие четкой и ровной границы между мышечным слоем и слизистой. Необходимо согласиться с мнением Л.Е. Терегуловой, что «все случаи с нечеткими границами между эндометрием и миометрием должны рассматриваться как подозрительные на рак эндометрия». Следует обращать внимание на гипоэхогенную субэндометриальную зону, которая при наличии инвазии имеет прерывистый контур, при неотчетливой границе между опухолью и миометрием. Вместе с тем, при ультразвуковом исследовании достоверность правильной оценки степени инвазии не превышает 77%, что требует применения других уточняющих методов диагностики.
САРКОМА МАТКИ
Саркома матки встречается достаточно редко, составляя 1-3% от всех злокачественных опухолей матки. Эхографическая картина саркомы и миомы матки практически идентична. Косвенными признаками, позволяющими заподозрить саркому, являются наличие в «миоматозной» матке зоны пониженной эхогенности без признаков акустического усиления и без четких контуров, дольчатое строение, отсутствие изображения полости матки и эндометрия, наличие участков сниженной эхогенности в центре узла, появление кистозной дегенерации опухоли и ее быстрый рост или увеличение в постменопаузальном периоде.
В качестве дополнительного метода дифференциальной диагностики миомы и саркомы матки может использоваться ЦДК. В случаях саркомы матки отмечается выраженная васкуляризация опухоли в 100% случаев, визуализируются расширенные сосуды миометрия, при динамическом обследовании появляются зоны неоваскуляризации. Характерным является визуализация в ходе ЦДК нерегулярных, тонких, хаотично разбросанных сигналов от сосудов или зон высокой васкуляризации в узле, особенно в центре, а также регистрация низкорезистентного кровотока в опухолевых артериях. В отличие от саркомы для миомы матки в целом характерен периферический тип кровотока. Внутриопухолевые цветовые локусы обычно определяются в больших узлах, примерно в половине наблюдений удается визуализировать «огибающий» сосуд, повторяющий контуры узла.
Согласно полученным нами данным, средние значения индекса резистентности при простой миоме составляют 0,61, при пролиферирующей миоме - 0,45, а при саркоме матки - 0,35. В то время как максимальная систолическая скорость кровотока при простой миоме составляет в среднем 14 см/с, при пролиферирующей миоме - 30 см/с, а при саркоме матки - 67 см/с.
Сальпингит и оофорит, опухоли яичников
Сальпингоофорит
Сальпингоофорит (СО) относится к числу самых частых локализаций ВЗОМТ. Каждой пятой женщине, перенесшей СО, угрожает бесплодие.
Одной из частых причин возникновения сальпингоофорита является использование внутриматочных контрацептивов. При этом риск возникновения тяжелых форм воспалительных заболеваний придатков матки возрастает в 3-9 раз. Возникновение воспалительных заболеваний придатков матки зависит от времени использования внутриматочного контрацептива и от типа последнего. Он наиболее высок с течение первого месяца использования, и объясняется комплексом следующих факторов:
- возможность заноса инфекции при введении спирали;
- распространение бактерий по нитям ВМК, свисающим во влагалище;
- нарушение внутриматочным контрацептивом процессов слущивания эндометрия во время менструации, подавление фагоцитоза и других факторов иммунной защиты;
- ВМК способствует появлению микроэрозий и перифокальной воспалительной реакции стромы.
Среди гинекологов дискутируется вопрос о возможностях эхографии в диагностике воспалительных заболеваний придатков матки. В.И. Краснопольский и соавт. считают, что эхография существенно не дополняет пальпаторные данные.Л.В. Василевская и соавт. предостерегают о возможности введения в заблуждение врача результатами ультразвукового исследования, однако, авторы отмечают, что в случаях формирования сактосальпинкса или тубоовариального образования эхография становится более информативной. Такая точка зрения объяснима отсутствием специфических ультразвуковых признаков при некоторых формах воспалительных процессов придатков.
Ультразвуковая диагностика острого сальпингита возможна только при достаточном скоплении воспалительного экссудата, когда начинает визуализироваться образование, прилегающее к заднебоковой стенке матки.
Острый сальпингоофорит (ОСО), как указывает G. Monif (1982), характеризуется следующими стадиями:
I – острый эндометрит и сальпингит без признаков воспаления тазовой брюшины;
II – острый эндометрит и сальпингит с признаками раздражения брюшины;
III – ОСО с окклюзией маточных труб и развитием тубоовариального образования;
IV – разрыв тубоовариального образования.
В клинической картине острого сальпингита можно выделить две фазы: первая – токсическая, характер клинических проявлений при которой определяет преобладающая аэробная флора; в течение второй фазы к аэробной флоре присоединяется анаэробная, что приводит к утяжелению симптомов заболевания и развитию осложнений. Именно во второй фазе сальпингита формируется тубоовариальное образование с гнойным содержимым, угрожающее перфорацией.
При трансвагинальном (ТВ) исследовании нередко удается проследить связь образования с трубным углом матки. Маточная труба при остром сальпингите может иметь овальную или изогнутую веретенообразную форму с расширенным ампулярным отделом, может быть представлена двухкамерным образованием в форме «8» (иногда определяется большее число камер за счет выраженной ротации трубы). Стенки маточной трубы неравномерно утолщены до 5 мм и более, эхогенность их повышена. Содержимое трубы в большинстве случаев анэхогенное, однородное, но может определяться мелкая взвесь и утолщенные неполные эхогенные перегородки («зубчатое колесо»). Могут визуализироваться пристеночные включения, внутрипросветные пузырьки газа.
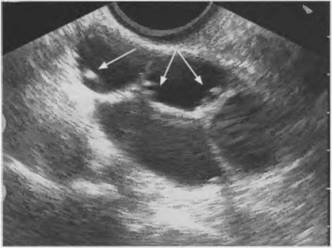
Рис.26 Сактосальпинкс, пузырьки газа в просвете трубы (указано стрелками), расположенные на внутритубарных спайках, ТВ сканирование
При наличии выраженных двусторонних сактосальпинксов они могут «сливаться», образуя единый конгломерат в позадиматочном пространстве. В отличие от свободной жидкости, содержимое сактосальпинксов не перемещается при изменении положения тела пациентки. Острый сальпингит часто сочетается с острым оофоритом. В позадиматочном пространстве нередко визуализируется жидкость. При допплерометрии отмечается усиление васкуляризации стенок трубы (индекс резистентности <0,6).
О хроническом воспалительном процессе свидетельствует расширенная маточная труба, заполненная ан- или гипоэхогенным содержимым (рис. 4.2). Толщина стенки трубы менее 5 мм, могут также определяться неполные перегородки, чаще тонкие. У 10% пациенток отмечается умеренное количество свободной жидкости в малом тазу. При допплерометрии отмечается снижение кровоснабжения стенок трубы, индекс резистентности превышает 0,6. Отсутствие кровотока в стенках маточной трубы служит неблагоприятным признаком прогноза излечения, так как может свидетельствовать о деструктивных изменениях труб.
Гидросальпинкс может симулировать эхографическую картину варикозного расширения вен малого таза, мегауретера, а при больших размерах - кистомы яичника. Дифференциальная диагностика с образованиями яичникового генеза основывается на визуализации интактного яичника с одноименной стороны, а также на изменении формы образования при сканировании в различных плоскостях. Заболевания вен малого таза устанавливаются при помощи режима цветового допплеровского картирования (ЦДК). При подозрении на мегауретер необходимо искать сообщение расширенного участка мочеточника с лоханкой почки или с мочевым пузырем.
Гематосальпинкс может образоваться при разрыве трубы, вследствие прервавшейся внематочной беременности, при трубном аборте из-за отслойки хориальной ткани и при забросе крови из матки. Содержимое гематосальпинкса чаще имеет среднюю или повышенную эхогенность, возможная гетероэхогенная структура (рис. 4.3).
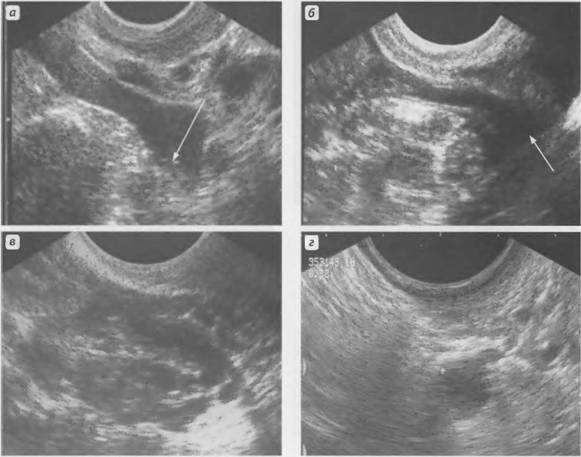
Рис. 27. Ятрогенный гидросальпинкс: а — окклюзия фимбриального отдела (указано стрелкой); б— окклюзи перешеечного отдела (указано стрелкой); в — окклюзия ампулярного отдела, отмечается утолщение стенок трубы; г — окклюзия ампулярного отдела. (ТВ сканирование)
Пиосальпинкс чаще бывает двусторонним. Эхографическая картина у пациенток с пиосальпинксом отличается выраженным полиморфизмом в зависимости от степени выраженности патологического процесса. В отличие от гидросальпинкса пиосальпинкс чаще имеет вид многокамерного образования вследствие изменения стенок маточной трубы. При небольших размерах пиосальпинкс практически неотличим от гидросальпинкса. Существенную помощь в идентификации пиосальпинкса оказывает только оценка его содержимого, которое характеризуется неоднородной эхоструктурой за счет гиперэхогенной взвеси, морфологически представленной гнойным содержимым (рис. 4.4). Стенки пиосальпинкса всегда гиперэхогенные и утолщенные.
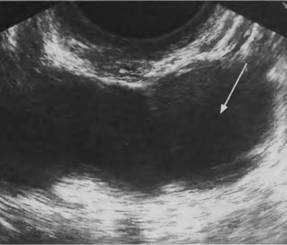
Рис. 28.Пиосальпинкс с жидким гноем (указан стрелками), ТВ сканирование.
При прогрессировании пиосальпинкса возможно формирование тубоовариального образования и абсцесса. При распространении инфекционного процесса на яичник происходит формирование тубоовариального образования, которое обычно располагается сбоку от матки и в позадиматочном пространстве. Контур, как правило, нечеткий, форма - овальная или неправильная. Яичник и труба могут смыкаться, но определяются как отдельные структуры. В некоторых случаях при ТВ исследовании удается их «раздвинуть» путем надавливания датчиком, однако следует помнить, что такие манипуляции могут вызвать резко выраженные болевые ощущения и привести к перфорации образования.
Абсцесс является следующей стадией воспалительного процесса, при этом происходит «стирание» границ между маточными трубами и яичниками. При ультразвуковом исследовании тубоовариальный абсцесс характеризуется наличием в области придатков образования сложной эхоструктуры с преобладанием кистозного компонента. Кистозные полости могут быть множественными, различными по величине и форме. В структуре конгломерата могут встречаться гиперэхогенные включения с тенью - пузырьки газа, перегородки, взвесь. При ТА эхографии контуры абсцесса могут выглядеть размытыми, в большинстве случаев яичник четко не идентифицируется. В этих случаях ТВ эхография имеет решающее значение в установлении точного диагноза.
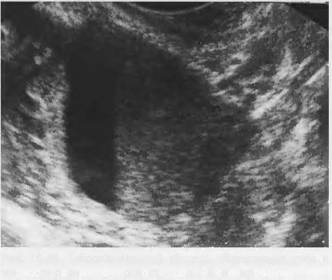
Рис. 29. Тубоовариальный абсцесс, образование уровня
жидкости разных по плотности сред, (ТВ сканирование)
Примерно в 20% наблюдений удается визуализировать контур образования, найти стенку и определить в ней кровоток. В острой фазе воспаления отмечается интенсивное кровоснабжение со снижением индекса резистентности в пределах 0,4-0,6. В дальнейшем кровоснабжение уменьшается, индекс резистентности повышается. Размеры одностороннего абсцесса в среднем составляют 50-70 мм, но могут достигать и 150 мм. При двусторонней локализации тубоовариального абсцесса не всегда удается установить даже условные границы между органами малого таза. В этих наблюдениях воспалительные образования визуализируются в виде единого конгломерата неправильной формы, с утолщенной капсулой, множественными внутренними перегородками и неоднородным содержимым. Интерпретация эхограмм у пациенток с подозрением на тубоовариальный абсцесс должна проводиться в соответствии с клинической симптоматикой заболевания. Дифференциальный диагноз следует проводить с аппендикулярным абсцессом, нагноившейся эндометриоидной кистой, опухолями яичников сложного строения и прервавшейся внематочной беременностью
При ультразвуковом исследовании изолированный оофорит встречается в 6-10% случаев среди всех больных с воспалительными заболеваниями придатков. Диагностика основывается на следующих эхографических признаках оофорита:
- шарообразная форма яичников;
- увеличение размеров яичника;
- нечеткий контур яичника;
- утолщение белочной оболочки;
- снижение эхогенности стромы;
- невозможность полноценной визуализации фолликулов;
- неоднородная структура стромы;
- пузырьки газа;
- свободная жидкость в малом тазу;
- боль при ТВ исследовании.
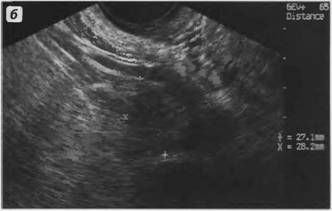
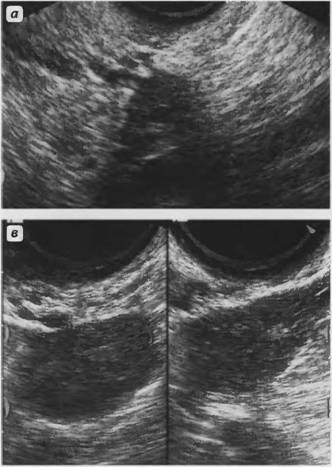
Рис. 30, Оофорит в репродуктивном возрасте, гипоэхогенная строма: а — визуализация фолликулов затруднена, яичник шаровидной формы, контур его нечеткий; б — нечеткий и неровный контур яичника, имеющего шаровидную форму; в — затруднение визуализации фолликулов в обоих яичниках. (ТВ сканирование)
Морфологические изменения при периоофорите и оофорите проявляются нарушением микроциркуляции, отеком и инфильтрацией, что эхографически определяется как увеличение размеров, шарообразная форма и изменение (снижение) эхогенности.
Рак яичников в подавляющем большинстве случаев возникает из предшествующих доброкачественных или пограничных эпителиальных опухолей, а первичный рак составляет 4-5%. При скрининговом обследовании женщин при отсутствии жалоб частота патологии яичников, выявляемой при эхографии, составляет 3,2%. Среди всех опухолей женской половой сферы опухоли яичника занимают 2-е место, при этом доля доброкачественных опухолей составляет 70—80%, злокачественных 20—30%.
Различают серозную, папиллярную и муцинозную цистаденокарциному, поверхностную папиллярную карциному, злокачественную цистаденофиброму и другие морфологические типы.
Рак яичников стабильно занимает третье место после рака тела и шейки матки. В то время как смертность от него стоит на первом месте и составляет 49%, а средний показатель пятилетней выживаемости больных не превышает 20-28%. Рак яичников встречается у женщин всех возрастных групп, но пик заболеваемости отмечается между 60 и 70 годами. Учитывая актуальность ранней диагностики рака яичников и длительное отсутствие клинических признаков, при ультразвуковом исследовании органов малого таза необходимо учитывать минимальные изменения яичников для последующего углубленного обследования с целью исключения злокачественного новообразования.
Эхографические признаки, позволяющие заподозрить рак яичника:
· выраженная асимметрия размеров яичников;
· частичное исчезновение контура увеличенного яичника;
· наличие образования, характерного для фолликула или ретенционной кисты, любого размера у женщин в постменопаузе;
· появление патологических зон гиперваскуляризации в яичнике;
· наличие свободной жидкости в позадиматочном пространстве вне овуляции или у женщин в постменопаузе.
При выявлении одного из перечисленных признаков необходимо динамическое эхографическое наблюдение в течении 1-2 мес. Если имеется два или более признаков, требуется срочная консультация онкогинеколога.
Использование допплерографии позволяет добиться существенного увеличения точности дифференциации доброкачественных и злокачественных новообразований яичников. Основа метода заключается в том, что для злокачественного роста характерен феномен неоваскуляризации, при котором опухоль сама индуцирует рост своих капилляров, а последние способствуют ее росту. Существенной особенностью новообразованных злокачественных сосудов является недостаток гладкомышечной ткани, и соответственно, низкая резистентность стенок. Другая особенность - это множественные шунты, способствующие высокой скорости внутриопухолевого кровотока. Вместе с тем, морфология и, соответственно, физиология сосудов в доброкачественных опухолях приближается к нормальным. Именно благодаря этой разнице и становится возможным дифференциальный диагноз "добра и зла" в опухолях яичников при допплерографии.
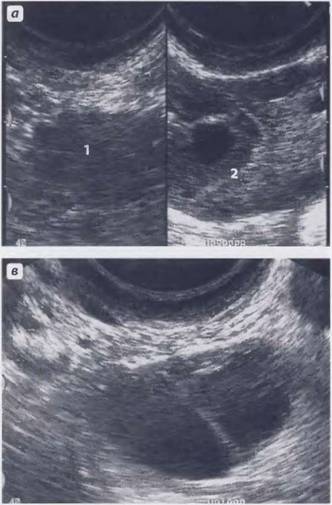
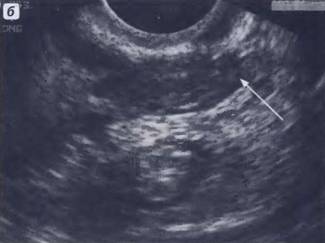
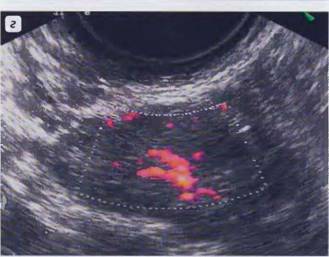
Рис.31. Эхографические маркеры, позволяющие заподозрить рак яичника: а — асимметрия размеров и эхогенности яичников у пациентки в постменопаузе: 1 — правый яичник; 2 — левый яичник с локальным изменением, имитирующим желтое тело; б —исчезновение четкого контура яичника (указано стрелкой); в — ретенционные кисты яичника малого размера у пациентки в постменопаузе; г — зона гиперваскуляризации яичника у пациентки в постменопаузе. (ТВ сканирование)
Примерно в 80% случаев диагноз ставится во II-III стадиях. Столь позднее выявление рака связано с длительным бессимптомным течением и отсутствием у врачей онкологической настороженности. Злокачественная опухоль характеризуется быстрым ростом, ранним, обширным метастазированием и прорастанием в соседние органы.
Классификация рака яичника FIGO (без учета подстадий):
- I стадия – опухоль ограничена яичником (яичниками);
- II стадия – распространение на рядом расположенные органы (матку, маточные трубы и т.д.);
- III стадия - распространение за пределы малого таза и (или) метастазы в забрюшинные лимфатические узлы;
- IV стадия – отдаленные метастазы.
Необходимо отметить, что начиная с I стадии, опухоль может прорастать капсулу, что ведет к возникновению асцита. На агрессивность течения и, следовательно, прогноз заболевания влияет также степень дифференцировки опухоли:
- Grade I– высокодифференцированная,
- Grade II – умереннодифференцированная,
- Grade III – низкодифференцированная.
В 70% случаев заболевание протекает бессимптомно и лишь у 30% больных выявляется скудная и непатогномоничная симптоматика. Даже при осложненном течении заболевания (разрыв опухоли, перекрут ножки) болевые ощущения у пожилых больных, как правило, не выражены. Диагностика патологии яичника в постменопаузе затруднена в связи с частым ожирением, опущением внутренних половых органов, атонией кишечника, спаечным процессом.
Эхографические признаки рака яичников:
- многокамерное (однокамерное) образование,
- контуры неровные (ровные), нечеткие (четкие),
- строение кистозное, кистозно-солидное, солидное,
- множественные перегородки различной толщины с фрагментарными утолщениями,
- пристеночные разрастания,
- наличие жидкости в позадиматочном пространстве, раннее возникновение асцита,
- богатая васкуляризация солидного компонента, перегородок и капсулы.
Из приведенных ультразвуковых признаков вытекает, что рак яичников – чрезвычайно полиморфное образование, которое может иметь и вид фолликулярной кисты, и неоднородную внутреннюю структуру, включающую всевозможные компоненты. Однако перечисленные эхографические симптомы соответствуют поздним стадиям, когда прогноз для жизни больной неблагоприятный. К сожалению, для начальных стадий заболевания достоверных эхографических признаков не существует.
Опухоли стромы полового тяжа представлены в основном гормонопродуцирующими новообразованиями. В эту группу входят:
- феминизирующие (гранулезоклеточная, тека-клеточная),
- маскулинизирующие (андробластома и др.) опухоли,
- гормональная индифферентная фиброма.
Гранулезоклеточная опухоль. Гранулезоклеточная опухоль (фолликулома) возникает из гранулезных клеток фолликула и из остатков клеток полового тяжа. Встречается во всех возрастных группах – от детского до преклонного возраста, но наиболее часто в возрасте от 40 до 60 лет. Средний возраст при доброкачественных формах 50 лет, при злокачественных - 39 лет. Злокачественные формы наблюдаются у 4-25% больных.
Опухоль является гормонально активной и продуцирует эстрогены. В 50-85 % случаев сочетается с гиперпластическими процессами эндометрия (полипы, железисто-кистозная и атипическая гиперплазия) и в 25 % с раком эндометрия. Отмечается также частое сочетание с миомой матки, внутренним эндометриозом и серозными цистаденомами. При наличии новообразования у девочек возникает преждевременное половое созревание, у молодых женщин развитие опухоли сопровождается временной аменореей, которая сменяется ациклическими кровотечениями и невынашиванием беременности. В постменопаузе возникают маточные кровотечения и психофизиологическое «омоложение».
Эхографические признаки гранулезоклеточной опухоли неспецифичны. Размеры образования в среднем составляют 10 см. Оно имеет дольчатое солидное строение с кистозными включениями различного размера. Встречаются и кистозные варианты, имитирующие серозные цистаденомы.
Выделяют следующие эхографические типы:
· кистозные однокамерные с тонкой капсулой;
· кистозно-солидные с крупными полостями;
· солидные.
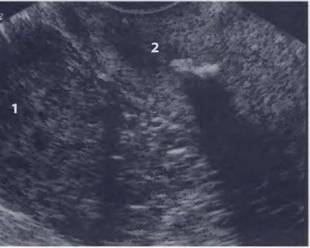
Рис. 32. Гранулезоклеточная опухоль, а: 1 — опухоль, 2 — шейка и облитерация цервикального канала; (ТВ сканирование)
Злокачественные гранулезоклеточные опухоли чаще двухсторонние, прорастают капсулу и сопровождаются выраженным спаечным процессом. Опухоль метастазирует в большой сальник, матку, маточные трубы, мочевой пузырь, печень. При злокачественном характере опухоли проявления гормональной активности уменьшаются, что связано со снижением дифференцировки опухолевых клеток при малигнизации.
При допплерографии выявляется гиперваскуляризация солидного компонента, особенно центральной части, с мозаичным типом кровотока. ИР находится в пределах 0,36-0,59, что в среднем составляет 0,46.
В постановке диагноза помогают: сочетание с эстрогензависимой патологией эндометрия и миометрия, отсутствие инволюции матки в постменопаузальном периоде, а также клинико-анамнестические данные.
Тека-клеточная опухоль. Тека-клеточная опухоль (текома) возникает из тека-клеток яичника и относится к эстрогенпродуцирующим. Они составляют 3,8% всех новообразований яичников и преимущественно возникают у женщин старше 50 лет.
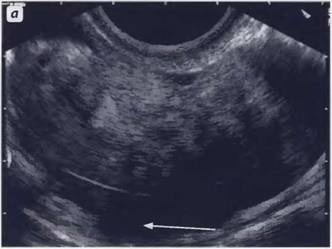
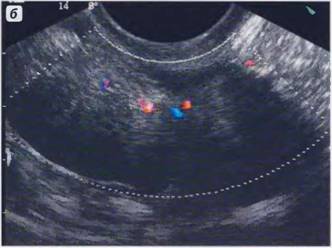
Рис. 33. Текома яичника: а — опухоль солидного строения, в малом тазу имеется свободная жидкость (указана стрелкой); б —ЦДК, умеренная васкуляризация опухоли (ТВ сканирование)
Опухоль обычно доброкачественная, озлокачествление наблюдается в 4-5% случаев. При любой форме она может сопровождаться асцитом, гидротораксом и анемией (триада Мейгса), которые исчезают после удаления опухоли. Как правило, новообразование одностороннее. Эхографические признаки неспецифичны, строение аналогично гранулезоклеточной опухоли.
Андробластома (аденобластома, опухоль клеток Сертоли и Лейдига, маскулинома) развивается из элементов мужской гонады, обладает андрогенной активностью, составляет от 0,4 до 2% новообразований яичников и преимущественно наблюдается в возрасте 20-35 лет, но встречается и у девочек. Чаще опухоль бывает доброкачественной, однако, до 30% андробластом в пре пубертатном возрасте имеет злокачественное течение. Для клинических симптомов характерны явления дефеминизации и маскулинизации.
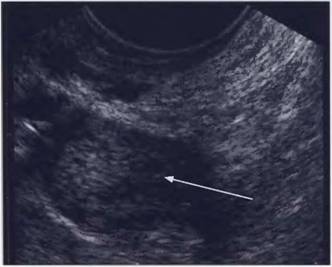
Рис.34. Андробластома (указана стрелкой). Опухоль неспецифического, кистозно-солидного строения, ТВ сканирование.
Эхографические признаки андробластомы неспецифичны, ультразвуковое изображение аналогично эстрогенпродуцирующим опухолям. Эти
опухоли васкуляризированы в 100% случаев, имеются множественные цветовые локусы в центральной части с ИР 0,40-0,52 и средним значением.
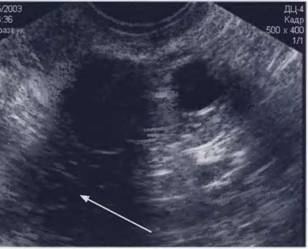
Рис. 35. Фиброма яичника: нетипичное изображение опухоли низкой эхогенности, за которой также формируется акустическая тень. (ТВ сканирование)
Перекрут кисты яичника
Клинические проявления: внезапно возникшая острая коликообразная боль с возрастающей интенсивностью, появляющаяся после резкого изменения положения тела.
Диагностика:
На заметку: своевременная постановка этого диагноза крайне важна.
Ректальное или влагалищное исследование: резко болезненное образование.
· Ультразвуковое исследование, трансвагинальное УЗИ.
· Лапароскопия с подготовкой для возможной лапаротомии.
· Ультразвуковые данные:
· Увеличение яичника с одной стороны и наличие в нем кистозного образования.
· Во многих случаях удается визуализировать перекрученную ножку опухоли, которая имеет вид эхогенной полоски.
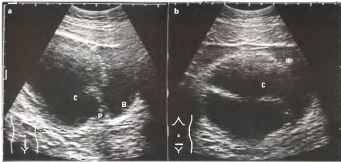
Рис. 36. а, b Перекрут кисты яичника: анэхогенная киста (С), прилегающая к мочевому пузырю (В). Ножка кисты (Р) имеет вид эхогенной полоски.
Точность ультразвуковой диагностики: ультразвуковое исследование позволяет диагностировать кисты с большой достоверностью, однако не всегда дает возможность определить вид кисты. Диагноз устанавливается на основании ультразвукового исследования в комбинации с клинической картиной и исключением беременности.
Диагностика беременности на ранних сроках Биометрические измерения при беременности.
Повышенное содержание в сыворотке крови или моче р-ЧХГ является индикатором возможной беременности, что можно подтвердить ультразвуковым исследованием. Кроме того, сонография способна выявить многоплодную беременность, что не всегда возможно при определении уровня гормонов, а также позволяет исключить эктопическую (внематочную) беременность (ЭБ).
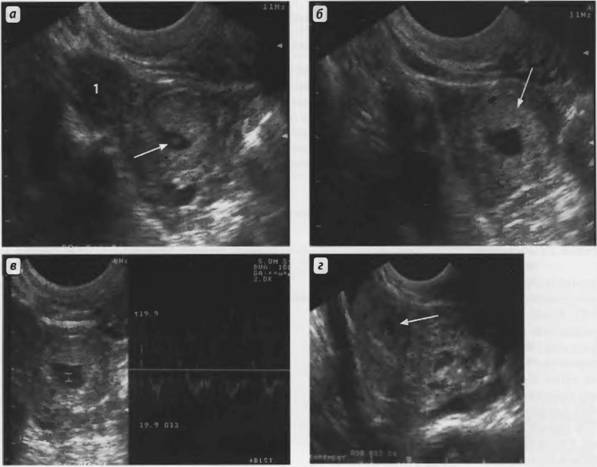
Рис. 37. Трубная беременность: а — плодное яйцо с желточным мешком (указан стрелкой): 1 — правый яичник; б — хорион (указан стрелкой); в — допплерография в проекции желточного мешка; г — плодное яйцо без эмбриона (указано стрелкой) (ТВ сканирование)
Трансвагинальная сонография способна обнаружить маточную беременность в ранних сроках, когда величина плодного мешка (полости хориона) составляет всего 2—3 мм. Такие размеры обычно соответствуют сроку 4 недели плюс еще 3 дня после последней менструации, т.е. примерно 14 дню после зачатия. Эта первоначально маленькая полость увеличивается со скоростью около 1.1 мм в сутки, постепенно превращаясь в амниотическую полость, в которой позднее виден эмбрион
Если плодный мешок (полость хориона) выявляется вне полости матки, это означает наличие эктопической беременности.
Сердечная деятельность плода может регистрироваться начиная с 6-й недели беременности. В это время частота сердечных сокращений плода в норме составляет 80— 90 в минуту.
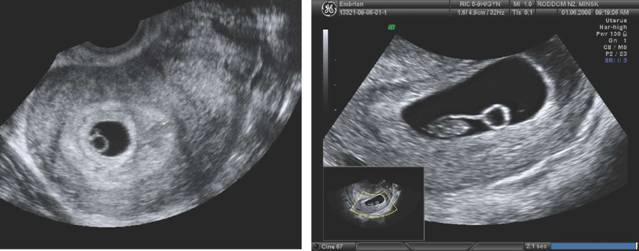
Рис.38. Плодное яйцо в полости матки Рис.39. Эмбрион, желточный проток, желточный мешок
Биофизические ограничения. Согласно рекомендациям Американского института по изучению применения ультразвука в медицине (АИУМ), энергия ультразвуковых колебаний ниже 100 мВт/см или менее 50 Дж/см не оказывает подтвержденного биологического эффекта и может считаться безопасной. При стандартных сонографических исследованиях в режиме реального времени ультразвуковое воздействие намного меньше вышеуказанных параметров, поэтому никакого повреждения тканей не происходит ни термического, ни кавитационного.
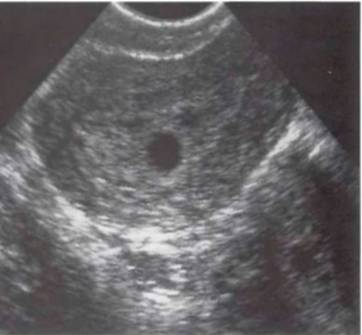
Рис. 40. Трансвагинальная эхограмма плодного яйца диаметром 7-8 мм в 5 нед, локализованного в полости матки.
Биологическое воздействие при других методах ультразвуковых исследований цветном доплеровском картировании и пульс-допплерографии, иное. Эти исследования длительны по времени и поэтому сопутствующие им лучевые нагрузки близки, а иногда и превышают критические значения. До настоящего времени, однако, нет никаких сообщений о повреждающих эффектах, полученных при проведении данных исследований. Несмотря на это, не следует проводить доплеровское (цветное) обследование в период наиболее чувствительной фазы органогенеза (в первом триместре), не имея веских оснований.
Биометрические измерения в первом триместра
Основное назначение биометрических измерений заключается в диагностике задержки внутриутробного развития плода, а также обнаружении аномалий развития. В конце книге приведены таблицы с указанием нормальных биометрических величин, соответствующих разным срокам внутриутробного развития, и границы их колебаний в процентилях.
Диаметр плодного мешка (полости хориона) (ДПМ). Полость хориона становится видимой с 14 дня после зачатия. Сначала она полностью анэхогенна, но вскоре появляется окружающий эхогенный ободок функционального эндометрия. Если при уровнях сывороточного ЧХГ выше 750—1000 ЕД/л не удается обнаружить плодный мешок в полости матки, следует предположить наличие эктопической беременности и принять все меры для ее подтверждения или исключения.
Желточный мешок представляет собой эхогенную кольцевидную структуру, которая становится видимой на 5-й неделе беременности, и к 10-й неделе его размер составляет 5 мм. Если диаметр желточного мешка в этом сроке менее 3 или более 7 мм, это означает повышенную вероятность аномалий развития плода. Обнаружение желточного мешка в полости матки полностью исключает возможность существования эктопической беременности, поскольку он является неотъемлемой составляющей внутренних структур плодного мешка. Показан желточный мешок, прилегающий к позвоночнику (плода, при сроке беременности 7 недель и 6 дней).
Копчико-теменной размер (КТР). Нормально развивающийся плод становится видимым в сроке беременности 6 недель и 3 дня. В это время его КТР составляет примерно 5 мм, а размеры амниотической полости15т 18 мм. С этого момента и до 12 недель срок беременности следует определять именно по величине КТР» а не ДПМ, поскольку первый показатель более точен (отклонения не превышают несколько дней). После 12 недель беременности более точным параметром становится бипариетальный размер (БПР) головки плода.
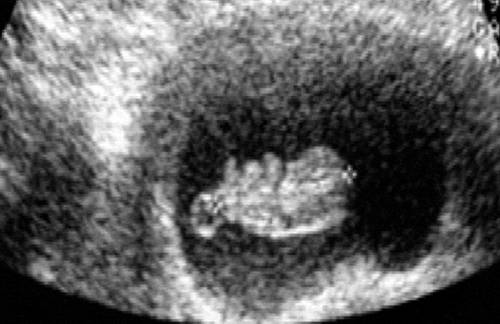
Рис. 41. Копчико-теменной размер эмбриона.
Иногда плод, который уже должен быть виден в определенном сроке, в действительности не обнаруживается. В этой случае следует еще раз проверить правильность предшествующего определения предполагаемого срока беременности. Если повторное ультразвуковое исследование снова выявит пустой плодный мешок, размеры которого к тому же не будя соответствовать нужным параметрам, это будет означать анэмбрионию, т.е. отсутствие зародыша. Данное состояние возникает приблизительно в 5% случаев всех зачатий.
Биометрические измерения во втором и третьем триместрах
Бипариетальный размер (БПР). Начиная с 12 недели внутриутробного развития плода БПР становится более удобным в плане измерения и точным биометрическим показателем, чем КТР. В этом сроке в головном мозге уже видно сосудистое сплетение в виде двусторонней эхогенной структуры. Для получения точных и достоверных результатов необходимо всегда соблюдать одни и те же условия измерений БПР.
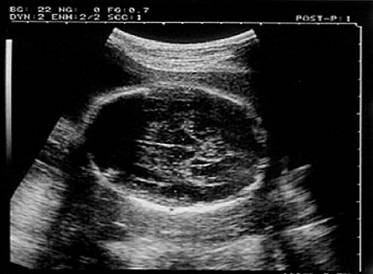
Рис 42. измерение бипариетального размера и окружности головы;
Плоскость сканирования должна обеспечивать визуализацию полного контура окружности головки, обычно имеющей форму овала. Необходимо, чтобы срединное М-эхо, образованное отражением эхосигналов от межполушарных структур, располагалось строго в центре. В передней трети М-эха должна находиться полость прозрачной перегородки. Мозжечок и глазные орбиты в этой плоскости не видны. Их визуализация означает, что плоскость сканирования проходит слишком низко. Одновременно с определением БПР можно измерять значения лобно-затылочного размера (ЛЗР) и окружности головки (ОГ).
Длина бедра (ДБ). Оссифицированный диафиз бедренной кости хорошо визуализируется. Следует измерять ножку плода, расположенную выше и ближе к датчику. При этом ее продольная ось должна быть перпендикулярна оси датчика.
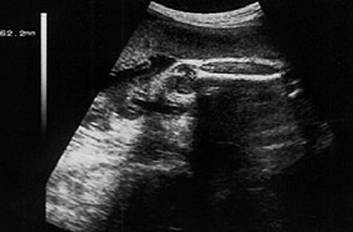
Рис. 43. Определение длины бедренной кости
Иногда для диагностики возможной задержки развития плода или иных аномалий необходимо прибегать к измерению других трубчатых костей. Это приходиться делать, если показатель ДБ не соответствует нормативу или при повторных измерениях меняется процентиль.
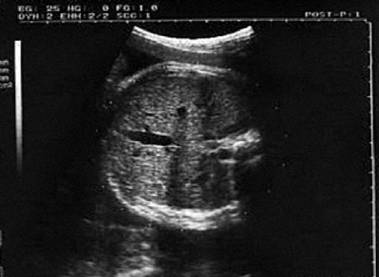
Рис. 44. Определение окружности живота
Окружность живота (ОЖ). Данный показатель должен определяться при сканировании живота в плоскости, проходящей на уровне печени. В этой плоскости может быть видна дорсальная треть пупочной и воротной вен. Подтверждением того, что плоскость сканирования проходит перпендикулярно продольной оси туловища плода, является симметричное двустороннее расположение ребер.
Расположение плаценты и определение пол плода. Диагностика аномалий развития плода
Нормальным является расположение плаценты вблизи дна матки на ее передней или задней стенке. Приблизительно в 20% случаев в толще плаценты выявляются единичные или множественные однокамерные кисты или кистевидные структуры. Они, как правило, не имеют существенного значения, но при этом следует помнить, что подобные структуры могут возникать при сахарном диабете у матери или при резус-конфликте. Вплоть до завершения второго триместра локализацию плаценты нельзя определять окончательно. Это связано с тем, плацента постепенно меняет свое положение. Предлежание плаценты, имевшее место в ранних сроках беременности, может сменяться низким расположением (менее 5 см от внутреннего зева) или (чаще) переходить в норма. В зависимости от взаимоотношений плаценты и шея матки предлежание может быть нескольких типов. Полное предлежание означает перекрывание всего внутреннего зева цервикаиного канала. При частичном предлежании плацента закрывает часть внутреннего зева, а при краевом располагается по его краю. Изучение структуры плаценты для оценки ее функция стало менее значимым с появление доплеровского метода сонографии. OF позволяет изучать особенности плацетарной и фетальной перфузии с более точностью.
Локализация плаценты в различные сроки беременности изменяется из-за «миграции» от нижнего сегмента к дну матки. При обнаружении предлежания плаценты до 20 нед беременности УЗИ необходимо повторять каждые 4 нед. Окончательное заключение о расположении плаценты следует делать в конце беременности.
Важный показатель состояния плаценты — её толщина. Для толщины плаценты характерна типичная кривая роста по мере развития беременности. К 36–37 нед рост плаценты прекращается. В дальнейшем при физиологическом течении беременности её толщина уменьшается или остаётся на том же уровне, составляя 3,3–3,6 см. Ультразвуковые признаки изменений в плаценте в разные сроки беременности определяют по степени её зрелости по P. Grannum (табл. 1).
Таблица табл. 1. Ультразвуковые признаки степени зрелости плаценты
|
Степень зрелости плаценты |
Хориальная мембрана |
Паренхима |
Базальный слой |
|
0 |
Прямая, гладкая |
Гомогенная |
Не идентифицируется |
|
I |
Слегка волнистая |
Небольшое количество эхогенных зон |
Не идентифицируется |
|
II |
С углублениями |
Линейные эхогенные уплотнения |
Линейное расположение небольших эхогенных зон (базальный пунктир) |
|
III |
С углублениями, достигающими базального слоя |
Округлые уплотнения с разрежениями в центре |
Большие и отчасти слившиеся эхогенные зоны, дающие акустическую тень |
Изменения структуры плаценты могут быть в виде кист, которые визуализируются как эхонегативные образования различной формы и величины.
Ультразвуковая диагностика ПОНРП основывается на выявлении эхонегативного пространства между стенкой матки и плацентой.
УЗИ используют также для диагностики состоятельности послеоперационного рубца на матке. О состоятельности рубца свидетельствуют однородная структура тканей и ровные контуры нижнего сегмента матки, толщина его не менее 3–4 мм. Несостоятельность рубца на матке диагностируют на основании выявления дефекта в виде глубокой ниши, истончения в области предполагаемого рубца, наличия большого количества гиперэхогенных включений (соединительная ткань).
При наличии многоплодной беременности следует определять расположение плаценты каждого плода. В одних случаях плоды могут иметь общую плаценту, в других - раздельные. Будущие родители (и наблюдающие за временностью специалисты акушеры) должны быть заранее уведомлены о наличии многоплодной беременности, чтобы иметь возможность подготовиться к рождению двойни, а иногда и тройни.
Если родители очень интересуются полом будущего ребенка, им можно его сообщить, но только в том случае, если эта информация достоверна. В ранних сроках беременности можно легко ошибиться, приняв за пенис пуповину или гипертрофированный клитор, или «половые губы» за мошонку. О поле будущего ребенка родителям следует сообщать тогда, когда они сами хотят его узнать.
Отеки у беременных
· Клинические проявления: генерализованные отеки и избыточная прибавка массы тела во время беременности.
· Диагностика: Следует исключить такие причины, как застойная сердечная недостаточность, последствия приема лекарственных средств, тромбоз глубоких вен нижних конечностей, заболевания почек. Очень важно вовремя диагностировать развивающийся поздний гестоз (протеинурия, повышение артериального давления).
· Ультразвуковые данные:
· Нормальная ультразвуковая картина венозных сосудов, которые хорошо подаются компрессии.
· Отсутствие скопления жидкости в анатомических полостях (плевральная, брюшная полости).
· Почки имеют нормальную структуру.
· Нормальные результаты эхокардиографии.
· Точность ультразвукового диагноза: простые отеки беременности не диагностируются при ультразвуковом исследовании. Тем не менее, следует исключать другие возможные причины отеков у беременных, в чем УЗИ может оказаться полезным.
Диагностика аномалий развития плода
Утолщение воротникового пространства (ВП). В конце 1-го и начале 2-го триместров может выявляться расширение подкожного пространства на лице и шее плода, превышающее 3 мм. Это является результатом нарушенного лимфообращения. Примерно в У3 случаев данный феномен сочетается с разного рода хромосомными аномалиями моносомией X (синдромом Тернера), трисомией 21 (синдромом Дауна) и трисомией 18.
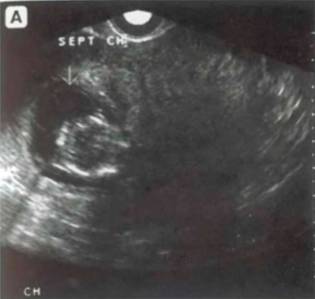
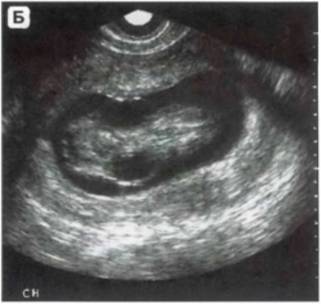
Рис. 45. Оценка толщины воротникового пространства в первом триместре беременности для скрининга хромосомных аномалий. Трансвагинальные эхограммы, демонстрирующие вид кистозной гигромы шеи в первом триместре беременности у плодов с кариотипом 45,ХО. (А) Поперечная плоскость сканирования плода в области шеи. В полости кистозной гигромы определяется неполная перегородка, разделяющая ее на две части. (Б) Фронтальная плоскость сканирования плода. Отчетливо определяется выраженность боковых отделов кистозной гигромы, локализующейся вокруг шеи.
Чтобы отличить кожную складку от амниотической оболочки, которая может располагаться вблизи шеи плода, осмотр следует проводить повторно. Ему должно предшествовать видимое исследователем движение плода, приводящее к изменению его положения. Надо помнить, что при сканировании кожи в косой проекции может формироваться изображение, напоминающее двойной контур. Его высота обычно не превышает 3 мм. Кем толще кожная складка и больше возраст матери, тем выше вероятность хромосомных аномалий.
Сердце и сосуды. Сердечно-сосудистая система является первой функционирующей системой плода. Сердечные сокращения становятся видимыми начиная с 6-й недели беременности. Отсутствие сердцебиений и задержка внутриутробного развития в сочетании с нечеткостью наружных контуров плода свидетельствуют о его гибели. Это, как правило, является показанием к расширению цервикального канала и инструментальному опорожнению полости матки. Ввиду того, что доплеровские методы исследования сопряжены с высокой ультразвуковой нагрузкой, их применение должно быть строго обосновано. Показаниями к таким видам обследования могут быть подозрение на задержку внутриутробного развития или анатомические аномалии сердца плода.
В первую очередь необходимо установить позицию сердца. Она определяется при поперечном сканировании грудной клетки плода. Относительно ее срединной плоскости сердце должно располагаться на одну треть вправо и на ли трети влево. Проводя осмотр в сагиттальной плоскости надо добиться визуализации дуги аорты и отходящей от нее брахиоцефальных ветвей важен четырехкамерный срез сердца, когда одновременна видны и оба предсердия, и оба желудочка. При этом видны клапаны сердца и можно исключить вероятные дефекты межжелудочковой (ДМЖП) и межпредсердной (ДМПП) перегородок. Слегка покачивая датчик в четырехкамерной плоскости, можно получите так называемый пятикамерный срез сердца этом срезе визуализируется поток крови, попадающий левый желудочек через митральный клапан и выходящий из желудочка через аортальный клапан. Именно в этой плоскости сканирования лучше всего видны дефекты мембранозной части межжелудочковой перегородки.
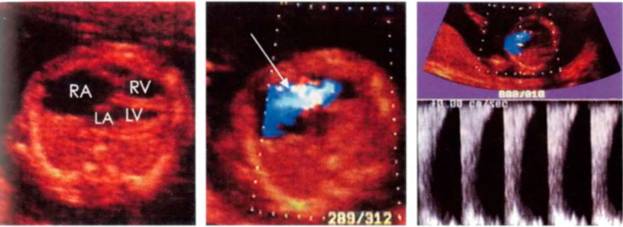
Рис. 46. Значительное увеличение полости правого предсердия (ЯА) у плода, выявленное в 17 нед. беременности. При осмотре трикуспидального клапана с использованием ЦДК и имульсно - волновой допплерометрии регистрировалась массивная струя регургитации, свидетельствующая о его тяжелой недостаточности. 1_.\/ - левый желудочек; 1_А - левое предсердие; Р\/ - правый желудочек.
Диагностика мелких ДМПП, ДМЖП или аномалий, связанных со сбросом крови справа налево, трудна. С наибольшей точностью их можно выявить при помощи цветной эхокардиографии, выполняемой высококвалифицированным специалистом. В четырехкамерной плоскости сканирования можно заподозрить транспозицию магистральных сосудов (ТМС). Чтобы уточнить наличие или отсутствие данной патологии, надо осмотреть выносят тракты сердца по короткой оси, а также легочный и аортальный клапаны.
При поперечном сканировании через заднюю мозговую ямку визуализируется мозжечок. На нем должна быть видна задняя выемка. Если она отсутствует, мозжечок имеет форму банана (симптом «банана»). Это говорит о смещении мозжечка к спинномозговому каналу, что может означать наличие дефекта неавральной трубки. По этой же причине контуры головки на поперечном срезе через область мозжечка утрачивают форму овала и приобретают форму разрезанного лимона (симптом «лимона»). При этом возникают двусторонние выпячивания париетальных костей. В некоторых случаях видно гиперэхогенное хориоидное сосудистое сплетение.
Цереброспинальные жидкостные пространства. В хориоидном сосудистом метении могут содержаться мелкие односторонние кисты (N), не имеющие какого-либо патологического значения. Двусторонние кисты бывают признаком трисомии по 18 паре хромосом или сочетается с аномалиями почек или сердца. Гидроцефалия возникает в результате сужения водопровода мозга или сопутствует spina bifida. Термин spina bifida объединяет широкий спектр дефектов — от клинически незначимого отсутствия отдельного фрагмента позвонка до незаращения целых отделов позвоночника. Закрытые дефекты составляют 15% всех дорсальных spina bifida. Обычно при этих дефектах нет других ассоциированных аномалий ЦНС.
Spina bifida часто сочетается с типичной внутричерепной патологией, включая вентрикуломегалию, гипоплазию структур задней черепной ямки.
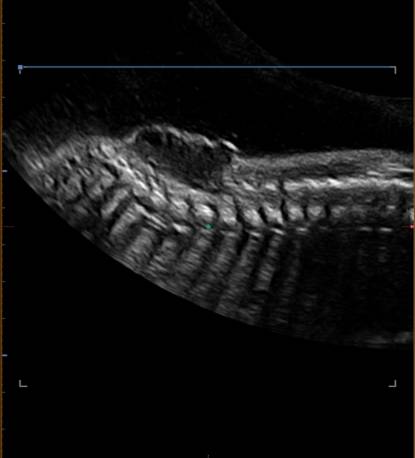
Рис .47. Сонограмма spina bifida плода
В 70—90% случаев она сочетается с другими внутренними и наружными анатомическими аномалиями мозга. После 20 недель беременности для оценки размеров желудков используется индекс соотношения ширины желудочков к половине диметра полушарий (т.н. желудочковый индекс). Величина индекса 0.5 и более называет на наличие гидроцефалии. На уровне лобных рогов этот индекс КИПР) немного ниже, чем на уровне затылочных рогов (ЖИЗР). Измерения диаметров желудочков и полушарий бывают затруднены тем, что стенки боковых желудочков не всегда четко отграничиваются от паренхимы мозга.
При такой аномалии развития, как spina bifida, имеется неполное закрытие спинномозгового канала, обусловленное дефектами дуг позвонков разной степени выраженности. Позвоночник хорошо виден в продольной и коронарной плоскостях сканирования. Для детального изучения строения позвоночника следует, двигаясь в кранио-каудальном направлении, осматривать в поперечной плоскости каждый позвонок. Это позволяет наиболее точно выявлять любое нарушение непрерывности в цепочке задних структур позвонков, включая их задние отростки. При поперечном сканирован должны быть видны точки окостенения каждом из трех сегментов. Располагаясь близко друг к другу, они образуют форму треугольника. Впереди тел позвонков видна аорта плода
При spina bifida обе задние точки окостенения отклоняются наружу, и спинномозговой канал оказывается открытым сзади Определяя содержание в крови матери афетопротеина, можно выявлять только открытые формы дефектов, когда полость канала зияет. Распознать же скрытые формы, когда полость прикрыта какой-либо тканью, таким способом невозможно. Симптомы «банана» и «лимона», описанные, выше, являются косвенными признаками данной аномалии развития.
Кости лица и шея плода. При сканировании лица в поперечной и коронарной плоскостях определяется расстояние между глазными орбитами. Уменьшение этого расстояния именуется гипертелоризмом, а увеличение гипертелоризмом. Исследование в продольной плоскости дает возможность видеть нарушения профиля лица. Расщелины губы и твердого неба, как правило, обнаруживаются при сканировании в продольной плоскости в виде дефекта верхней губы, которая в норме представляет собой непрерывную эхогенную структуру.
Отек плода. Причиной повышенного скопления жидкости в серозных полостях и плаценте могут быть следующие факторы: сердечная недостаточность, нарушения обмена веществ, инфекционно-воспалительные процессы, врожденная анемия плода, резус-сенсибилизация и хромосомные аномалии.
При монохориальной двойне отек одного из плодов может возникать в результате фето -фетального сброса крови по артериовенозным шунтам.
Помимо асцита при ультразвуковом исследовании можно обнаружить скопления жидкости в плевральной и перикардиальной полостях, а также возможный генерализованный отек кожи.
Диагностические критерии водянки плода:
• Асцит
• Плевральный выпот
• Перикардиальный выпот
• Генерализованный отек кожи
Ультразвуковое исследование желудочно-кишечного тракта дает возможность подтвердить или исключить различные его аномалии. Одной из них является атрезия или стеноз двенадцатиперстной кишки. В этом случае визуализируются две анэхогенные полости (признак «двойного пузырька»). Одна полость является расширенным желудком, а другая расширенной двенадцатиперстной кишкой. Обе полости заполнены жидкостью. Находка может оказаться ложноположительной в результате двойного сканирования желудка в косой плоскости. Для исключения данного артефакта осмотр должен проводиться в нескольких плоскостях. Следует помнить, что до 11 недель беременности рядом с пуповиной в норме существует грыжеподобное выпячивание передней брюшной стенки. Его легко спутать с истинным омфалоцеле.
Разного рода аномалии почек после 15 недель беременности косвенно проявляются уменьшением количества амниотической жидкости (олигогидрамнионом) или полным ее отсутствием (ангидрамнионом), поскольку количество околоплодных вод в данном сроке зависит от объема выделяемой мочи. При продольном сканировании нормальная паренхима почки предстает в виде гипоэхогенных пирамид и анэхогенных собирательных участков.
Нарушение проходимости собирательной системы, обусловленное стенозом мочеточника в области малого таза, распознается сравнением ворот обеих почек в поперечной плоскости.
Различают три вида поликистоза почек (Поттер I, II, III). Тип Поттер I характеризуется наличием гиперэхогенной почки с множеством очень мелких (12 мм) микрокист. Тип Поттер II диагностируется также внутриутробное, при этом меры кист больше и почки имеют характерный вид. Тип Поттер III проявляйся уже во взрослом возрасте. У плода последний тип болезни может проявляться повышенной диффузной эхогенностью одной или обеих почек, но при этом количество околоплодных вод остается в пределах и мочевой пузырь наполнен и хорошо виден.
Костная система. Во втором и третьем триместрах следует осматривать верхние и нижние конечности для оценки завершенности формирования центров окостенения фаланговых пястных и плюсневых костей. Это позволяет выявлять или исключать синдактилию, как часть других врожденных аномалий развития. Кроме того, при исследовании может обнаруживаться избыточное количество фаланговых костей, например, гексадактилия. Полидактилия может сочетаться с гипоплазией легки) сопутствующим укорочением ребер и изменением фор мы грудной клетки (в виде колокола).
Для выявления косолапости необходимо осматривать стопы. Причиной данной аномалии может быть также укорочение трубчатых костей. Нарушение процессов окостенения, как составная часть ахондроплазии, нередко распознается только в третьем триместре беременности. В этом случае характерными особенностями являются короткие трубчатые кости и непропорционально большие размеры головки